Ilt er et kemisk grundstof. Det har symbolet O og atomnummer 8. Det er det tredje mest almindelige grundstof i universet efter hydrogen og helium.
Ilten udgør mere end en femtedel af Jordens atmosfære i volumen. I luften er der normalt to iltatomer, som går sammen og danner dioxygen (O
2), en farveløs gas. Denne gas kaldes ofte bare ilt. Den har ingen smag eller lugt. Den er lyseblå, når den er flydende eller fast.
Oxygen er en del af chalcogen-gruppen i det periodiske system. Det er et meget reaktivt ikke-metal. Det danner oxider og andre forbindelser med mange grundstoffer. Oxygen i disse oxider og i andre forbindelser (hovedsagelig silikatmineraler og calciumcarbonat i kalksten) udgør næsten halvdelen af Jordens skorpe, målt i masse.
De fleste levende væsener bruger ilt til at trække vejret. Mange molekyler i levende væsener indeholder ilt, f.eks. proteiner, nukleinsyrer, kulhydrater og fedtstoffer. Ilt er en del af vand, som alt kendt liv har brug for for at leve. Alger, cyanobakterier og planter fremstiller jordens iltgas ved hjælp af fotosyntese. De bruger solens lys til at få brint fra vand og afgiver ilt.
I toppen af Jordens atmosfære findes ozon (O
3), i ozonlaget. Det absorberer ultraviolet stråling, hvilket betyder, at mindre stråling når ned til jordoverfladen.
Iltgas anvendes til fremstilling af stål, plast og tekstiler. Den har også medicinske anvendelser og bruges til at trække vejret, når der ikke er god luft (f.eks. af dykkere og brandmænd), og til svejsning. Flydende ilt og iltrige forbindelser kan anvendes som raketdrivmiddel.
Egenskaber og fysisk-kemiske data
Ilt har atomnummer 8 og en gennemsnitlig atommasse på cirka 15,999 u. Den elektroniske konfiguration er 1s2 2s2 2p4, hvilket giver fire valenselektroner og forklarer dets høje reaktivitet. På standardbetingelser er dioxygen (O2) en farveløs, lugtfri gas med et volumenindhold i tør luft på cirka 20,95 %.
Vigtige fysiske data (omtrentlig):
- Smeltepunkt (O2): −218,79 °C
- Kogepunkt (O2): −182,96 °C
- Væske og fast ilt er lyseblå.
- O2 er paramagnetisk (har to upræparrede elektroner) og tiltrækkes af magnetfelter.
- Elektronegativitet (Pauling): omkring 3,44.
Allotroper og isotoper
Den mest almindelige allotrop er dioxygen (O2), som er nødvendig for almindelig aerob respiration. En anden vigtig allotrop er ozon (O3), som i stratosfæren beskytter mod UV-stråling, men ved jordoverfladen er det en skadelig luftforurenende gas.
De stabile isotoper er 16O (≈99,76 %), 17O og 18O. Radioaktive isotoper som 15O anvendes i medicinsk billeddannelse (PET-scanning), men har kort halveringstid.
Biologisk rolle og kredsløb
Ilt er centralt i organismers stofskifte: under aerob respiration fungerer O2 som den terminale elektronacceptor i elektrontransportkæden, hvilket frigiver energi (ATP) fra føde. Uden tilstrækkelig ilt kan organismer skifte til mindre effektive anaerobe processer.
Fotosyntese hos alger, cyanobakterier og planter omdanner CO2 og vand til organiske stoffer og frigiver O2. Denne proces førte til iltning af Jordens atmosfære (den såkaldte Great Oxidation Event) for milliarder af år siden, og den opretholder i dag atmosfærens iltindhold.
I havene opløses ilt i overfladevandet; opløseligheden falder med stigende temperatur og salinitet. Lavt opløst ilt i kystområder kan føre til “døde zoner” (hypoxi), der skader marint liv.
Fremstilling
Industrielt fremstilles ilt primært ved fraktioneret destillation af flydende luft, hvor luften køles ned og de enkelte bestanddele adskilles. Mindre anlæg og medicinsk ilt laves ofte ved tryk-svingende adsorption (PSA), som separerer O2 fra luft ved hjælp af molekylsigte. Der findes også elektrolyse af vand (især til industrielle brint/ilt-processer) og kemiske generatorer (f.eks. til nødsituationer).
Anvendelser
- Industri: stål-produktion (basic oxygen process), fremstilling af kemikalier, oxidationsprocesser.
- Svejsning og skæring: oxy-fuel teknikker og ilttilførsel til plasmaskæring.
- Raketmotorer: flydende ilt som oxidationsmiddel i kombination med brændstof (f.eks. flydende hydrogen).
- Medicinsk: iltterapi, respiratorunderstøttelse, hyperbar oxygenbehandling.
- Dykning og brandvæsen: iltgiverapparater til at sikre åndedræt i iltfattige eller forurenede omgivelser (dykkere, brandmænd).
- Miljø: iltning af spildevand, akvakultur og andre processer, hvor opløst ilt er kritisk.
Sikkerhed og miljømæssige aspekter
Ilt er ikke brændbar, men er et stærkt oxidationsmiddel og øger hastigheden og intensiteten af forbrænding. Materialer, der normalt brænder langsomt i luft, kan antændes voldsomt i iltrige omgivelser. Håndtering af flydende ilt kræver forsigtighed på grund af ekstrem kulde og risiko for sprødhed i materialer.
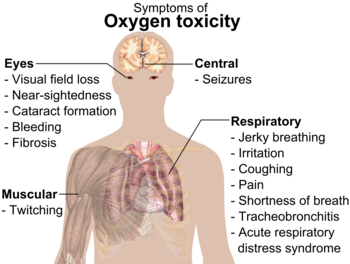
Ved høje ilttryk kan mennesker få iltforgiftning (pulmonal eller CNS-iltforgiftning), især ved dykning med højt omgivende tryk. Også langvarig eksponering for forhøjede iltkoncentrationer bruges kun under kontrol.
Miljømæssigt er tab af opløst ilt i havet og vandløb et voksende problem pga. opvarmning og eutrofiering. Ozon ved jordoverfladen er skadelig for sundhed og vegetation, mens ozon i stratosfæren er beskyttende.
Historie
Oxygen blev opdaget i 1770'erne af flere forskere uafhængigt: Carl Wilhelm Scheele (først, men publicerede senere) og Joseph Priestley (1774) lavede tidlige eksperimenter. Antoine Lavoisier forklarede gasens rolle i forbrænding og navngav stoffet "oxygène" (ilt, bogstaveligt "syre-danner", ud fra en fejlagtig teori om syrers natur), og han banede vejen for moderne kemi.
Praktiske bemærkninger
Når man taler om iltkoncentration i praktiske sammenhænge, er det nyttigt at kende partialtryk (pO2), især inden for medicin og dykning, hvor pO2 bestemmer risiko for hypoxi eller iltforgiftning. Også sensorer (iltmålere) bruges bredt til at overvåge atmosfærisk O2 og opløst ilt i vand.
Samlet set er ilt et af de mest vigtige grundstoffer for kemi, industri og liv på Jorden: fra at understøtte forbrænding og respiration til at forme planetens geokemi og beskytte mod skadelig stråling gennem ozonlaget.