Kemisk reaktion: Definition, typer, reaktionshastighed og eksempler
Få klar forståelse af kemiske reaktioner: definition, typer, reaktionshastighed og konkrete eksempler — rust, forbrænding, eksoterme/endoterme processer.
En kemisk reaktion sker, når en eller flere kemikalier ændres til en eller flere andre kemikalier. Eksempler:
- jern og ilt danner sammen rust
- eddike og bagepulver, der tilsammen danner natriumacetat, kuldioxid og vand
- ting, der brænder eller eksploderer
- mange reaktioner, der finder sted i levende væsener
- elektrokemiske reaktioner ved af- og genopladning af batterier
Nogle reaktioner er hurtige, og andre er langsomme. Nogle sker med forskellig hastighed, afhængigt af temperatur eller andre ting. Træ reagerer f.eks. ikke med luft, når det er koldt, men hvis det gøres varmt nok, begynder det at brænde. Nogle reaktioner afgiver energi. Det er eksoterme reaktioner. Ved andre reaktioner optages der energi. Det er endotermereaktioner.
Atomreaktioner er ikke kemiske reaktioner. Kemiske reaktioner involverer kun atomernes elektroner, mens atomreaktioner involverer protonerne og neutronerne i atomkerner.
Typer af kemiske reaktioner
- Sammensætningsreaktion (syntese): To eller flere stoffer reagerer og danner et enkelt produkt. Eksempel: A + B → AB.
- Nedbrydningsreaktion (dekomposition): Et stof brydes ned til to eller flere produkter. Eksempel: AB → A + B.
- Udskiftningsreaktion (enkelt-/dobbeltudskiftning): Et atom eller en ion i et molekyle erstattes af et andet. Eksempel på enkeltudskiftning: A + BC → AC + B. Eksempel på dobbeltudskiftning: AB + CD → AD + CB.
- Forbrændingsreaktion: Et brændbart stof reagerer typisk med ilt og danner CO2 og H2O (ved fuldstændig forbrænding). Den afgiver normalt meget energi.
- Redox-reaktioner (oxidation–reduktion): Elektroner overføres mellem stoffer. Mange vigtige processer som rustdannelse, respiration og batterier er redox-reaktioner.
- Syre–base-reaktion (neutralisation): En syre reagerer med en base og danner salt og vand.
- Polymerisation: Små molekyler (monomerer) binder sig sammen til store kæder eller netværk (polymerer), fx fremstilling af plastik.
- Fældningsreaktion: To opløsninger blandes, og et uopløseligt stof (et bundfald) dannes.
Reaktionshastighed og faktorer der påvirker den
Reaktionshastighed beskriver, hvor hurtigt reaktanterne omdannes til produkter. Hastigheden afhænger af flere faktorer:
- Koncentration: Højere koncentration af reaktanter øger antallet af kollisioner mellem partikler og øger ofte reaktionshastigheden.
- Temperatur: Højere temperatur giver partikler mere bevægelsesenergi, hvilket øger både antallet og energien af kollisioner, så flere kollisioner fører til reaktion.
- Partikelstørrelse/surface area: Mindre partikler eller større overfladeareal (fx revet metal) giver større kontaktflade og hurtigere reaktion for heterogene systemer.
- Katalysatorer: Et stof, der øger reaktionshastigheden ved at sænke aktiveringsenergien, uden selv at blive forbrugt. Enzymer er biologiske katalysatorer.
- Tryk (især for gasser): Øget tryk svarer ofte til højere koncentration og kan øge hastigheden for gasreaktioner.
- Opløsningsmiddel og pH: Kemisk miljø (polart/apolart, surhed) kan påvirke reaktionsmekanismer og hastigheder.
- Inhibitorer: Stoffet der sænker hastigheden ved at forstyrre reaktionens mekanisme eller blokere aktive steder på en katalysator.
På et mere matematisk niveau beskrives hastigheden ofte ved en hastighedslov (rate law) der kan være afhængig af reaktanternes koncentrationer i en bestemt potens (reaktionsordenen). Mange reaktioner kræver også en aktiveringsenergi—den energi, der skal til, for at reaktanterne når en overgangstilstand før de bliver til produkter.
Energi og termodynamik
- Eksoterme reaktioner: Afgiver varme til omgivelserne (ΔH < 0). Eksempel: forbrænding af træ eller benzin.
- Endoterme reaktioner: Optager varme fra omgivelserne (ΔH > 0). Eksempel: opløsning af ammoniumnitrat i vand føles kold.
- Aktiveringsenergi: Den energi, reaktanterne skal have for at reagere—katalysatorer sænker denne barriere.
- Spontanitet: Ikke det samme som hastighed. Spontane processer vurderes ved Gibbs fri energi: ΔG = ΔH - TΔS. En negativ ΔG indikerer, at en proces er termodynamisk favorabel ved en given temperatur.
Kemiske ligninger og støkiometri
Kemiske reaktioner udtrykkes med kemiske ligninger, hvor reaktanter skrives til venstre og produkter til højre. Koefficienter bruges til at balancere ligningen, så masse og atomantal bevares (lov om massebevarelse). Støkiometri handler om forholdet mellem mængder af reaktanter og produkter og er vigtig for at beregne hvor meget af hvert stof, der forbruges eller dannes. Begreber som begrænsende reagent og udbytte er centrale i praktiske beregninger.
Reversible reaktioner og kemisk ligevægt
Mange reaktioner er reversible: reaktanter danner produkter, og produkterne kan tilbagedannes til reaktanter. I et lukket system kan der opstå en dynamisk ligevægt, hvor hastigheden af den fremadgående og bagudgående reaktion er lige. Ligevægtspositionen beskrives af ligevægtskonstanten (K). Ifølge Le Chateliers princip vil ligevægten forandre sig for at modvirke ændringer i koncentration, tryk eller temperatur.
Katalysatorer og enzymer
Katalysatorer øger reaktionshastigheden ved at tilbyde en alternativ reaktionsvej med lavere aktiveringsenergi. De forbruges ikke i den samlede reaktion. Der findes:
- Heterogene katalysatorer: Forskellige fase fra reaktanterne (fx fast katalysator i en gasreaktion).
- Homogene katalysatorer: Samme fase som reaktanterne (fx katalyse i opløsning).
- Enzymer: Biologiske katalysatorer, ekstremt specifikke og effektive under milde betingelser i levende organismer.
Kemiske reaktioner i hverdag og industri
Kemiske reaktioner er overalt: madlavning (bruning og fordøjelse), rengøring (sæbe og blegemidler), energiproduktion (forbrænding, brændselsceller), fremstilling af materialer (plastik, medicin), og elektrisk energi i batterier. Industrien udnytter kontrollerede reaktioner for at fremstille stoffer i stor skala under hensyntagen til sikkerhed, effektivitet og miljøpåvirkning.
Sikkerhed og miljø
Kemiske reaktioner kan være farlige (giftige, brændbare, eksplosive eller korrosive). Grundlæggende sikkerhedsforanstaltninger omfatter korrekt mærkning, brug af personlig beskyttelsesudstyr (handsker, briller, åndedrætsværn), ventilation og korrekt affaldshåndtering. Miljøhensyn omfatter reduktion af farlige biprodukter, genbrug og energieffektivitet.
Forskellen mellem kemiske og atomreaktioner (nukleare reaktioner)
Som nævnt ovenfor er atomreaktioner (nukleare reaktioner) ikke det samme som kemiske reaktioner. Kort sagt:
- Kemiske reaktioner involverer primært ændringer i atomers elektronkonfiguration og dannelse eller brud af kemiske bindinger.
- Nukleare reaktioner involverer ændringer i atomkernens partikler (protoner og neutroner) og kan ændre et grundstof til et andet. Disse processer frigiver ofte meget større mængder energi pr. nukleon end kemiske reaktioner.
Samlet set beskriver kemiske reaktioner en meget bred vifte af processer, fra simple synteser og nedbrydelser til komplekse biologiske kædereaktioner. Forståelse af typer, energi, hastighed og kontrol af reaktioner er centralt både i undervisning og i praktisk anvendelse inden for forskning, industri og dagligliv.

Rustende jern

Et bål er et eksempel på redox
Fire grundlæggende typer
Syntese
I en syntesereaktion kombineres to eller flere simple stoffer for at danne et mere komplekst stof.
A + B ⟶ A B {\displaystyle A+B\longrightarrow AB}
"To eller flere reaktanter giver et produkt" er en anden måde at identificere en syntesereaktion på. Et eksempel på en syntesereaktion er kombinationen af jern og svovl til jern(II)sulfid:
8 F e + S 8 ⟶ 8 F e S {\displaystyle 8Fe+S_{8}\longlightarrow 8FeS}
Et andet eksempel er simpel brintgas, der kombineres med simpel iltgas for at danne et mere komplekst stof, f.eks. vand.
Nedbrydning
En nedbrydningsreaktion er, når et mere komplekst stof nedbrydes til de mere simple dele. Den er således det modsatte af en syntesereaktion og kan skrives som:
A B ⟶ A + B {\displaystyle AB\longrightarrow A+B}
Et eksempel på en nedbrydningsreaktion er elektrolyse af vand til ilt- og brintgas:
2 H 2 O ⟶ 2 H 2 + O 2 {\displaystyle 2H_{2}O\longrightarrow 2H_{2}+O_{2}}}
Enkelt udskiftning
I en enkelt erstatningsreaktion erstatter et enkelt ukombineret grundstof et andet i en forbindelse; med andre ord bytter et grundstof plads med et andet grundstof i en forbindelse Disse reaktioner har den generelle form af:
A + B C ⟶ A C + B {\displaystyle A+BC\longrightarrow AC+B}
Et eksempel på en enkelt fortrængningsreaktion er, når magnesium erstatter hydrogen i vand for at danne magnesiumhydroxid og hydrogengas:
M g + 2 H 2 O ⟶ M g ( O H ) 2 + H 2 {\displaystyle Mg+2H_{2}O\longrightarrow Mg(OH)_{2}+H_{2}}}
Dobbelt udskiftning
Ved en dobbelt udskiftningsreaktion bytter anioner og kationer i to forbindelser plads og danner to helt forskellige forbindelser. Disse reaktioner har den generelle form:
A B + C D ⟶ A D + C B {\displaystyle AB+CD\longrightarrow AD+CB}
For eksempel, når bariumklorid (BaCl2 ) og magnesiumsulfat (MgSO4 ) reagerer, 42−bytter SO-anionen plads med 2Cl-anionen−, hvilket giver forbindelserne BaSO4og MgCl . 2
Et andet eksempel på en dobbelt fortrængningsreaktion er reaktionen af bly(II)nitrat med kaliumjodid, hvorved der dannes bly(II)jodid og kaliumnitrat:
P b ( N O 3 ) 2 + 2 K I ⟶ P b I 2 + 2 K N O 3 {\displaystyle Pb(NO_{3})_{2}+2KI\longrightarrow PbI_{2}+2KNO_{3}}
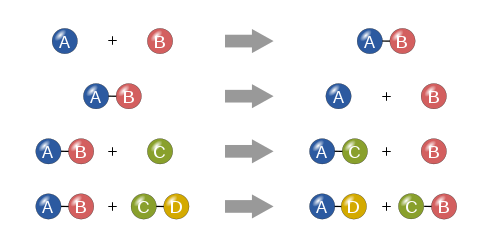
De fire grundlæggende kemiske reaktionstyper: syntese, nedbrydning, enkelt udskiftning og dobbelt udskiftning
Ligninger
En kemisk reaktion vises ved hjælp af en ligning:
A + B ⟶ C + D {\displaystyle \mathrm {A+B\longrightarrow C+D} }
Her reagerer A og B med C og D i en kemisk reaktion.
Dette er et eksempel på en forbrændingsreaktion.
C + O 2 ⟶ C O 2 {\displaystyle \mathrm {C+O_{2}\longrightarrow CO_{2}} }
Relaterede sider
- Organisk reaktion
- Redox
Spørgsmål og svar
Spørgsmål: Hvad er en kemisk reaktion?
A: En kemisk reaktion sker, når en eller flere kemikalier ændres til en eller flere andre kemikalier.
Spørgsmål: Kan du give eksempler på kemiske reaktioner?
A: Ja, nogle eksempler på kemiske reaktioner er jern og ilt, der kombineres til rust, eddike og bagepulver, der kombineres til natriumacetat, kuldioxid og vand, ting, der brænder eller eksploderer, og mange reaktioner, der sker inde i levende væsener, f.eks. fotosyntese.
Spørgsmål: Er alle kemiske reaktioner hurtige?
A: Nej, nogle reaktioner er hurtige, og andre er langsomme. Nogle sker med forskellig hastighed, afhængigt af temperaturen eller andre ting.
Spørgsmål: Hvad er en exoterm reaktion?
A: En exotermisk reaktion er en reaktion, der afgiver energi.
Spørgsmål: Hvad er en endotermisk reaktion?
A: En endotermisk reaktion er en reaktion, der optager energi.
Spørgsmål: Bliver kernereaktioner betragtet som kemiske reaktioner?
A: Nej, atomreaktioner er ikke kemiske reaktioner. Kemiske reaktioner involverer kun atomernes elektroner, mens atomreaktioner involverer protonerne og neutronerne i atomkernerne.
Spørgsmål: Kan temperaturen påvirke hastigheden af en kemisk reaktion?
A: Ja, afhængigt af temperaturen eller andre ting kan nogle reaktioner foregå med forskellig hastighed. F.eks. reagerer træ ikke med luft, når det er koldt, men hvis det gøres varmt nok, begynder det at brænde.
Søge









