Isotoper: Definition og eksempler på stabile og radioaktive varianter
Lær om isotoper: klar definition, forskelle mellem stabile og radioaktive varianter samt illustrative eksempler og deres rolle i natur og forskning.
Atomerne i et kemisk grundstof kan forekomme i flere udgaver, som opfører sig næsten ens kemisk, men har forskellig masse. Disse udgaver kaldes isotoper af grundstoffet. Atomer af samme grundstof har samme antal protoner, mens forskellige isotoper har forskelligt antal neutroner. Det er netop forskellen i neutronantal, der giver forskel i masse: forskellige isotoper af et grundstof vejer ikke det samme. Masse beskriver, hvor meget stof noget indeholder, og ting med forskellig masse har typisk også forskellig vægt.
Nogle isotoper er stabile og ændrer sig ikke over tid, mens andre er ustabile og omdannes til andre isotoper eller helt andre grundstoffer ved radioaktivt henfald. De ustabile kaldes radioaktive isotoper, mens de, der ikke henfalder, betegnes stabile isotoper.
Atomnummer, massetal og notation
Et atom af et givet grundstof har altid det samme antal protoner; dette antal kaldes atomnummeret. Isotoperne adskiller sig ved antallet af neutroner, og summen af protoner og neutroner kaldes massetallet. Når man navngiver en isotop, angiver man normalt grundstoffet og massetallet. For eksempel er symbolet for kulstof C, og alle kulstofatomer har 6 protoner. Den mest almindelige isotop af kulstof har også 6 neutroner, hvilket giver et massetal på 12, og den skrives kulstof-12 eller12 C. Isotopen af kulstof, der har 8 neutroner, skrives kulstof-14 eller C.14
Hvorfor nogle isotoper er ustabile
Stabiliteten af en isotop afhænger især af forholdet mellem neutroner og protoner og af atomkernenes interne kræfter. For lette grundstoffer er der ofte næsten lige så mange neutroner som protoner i stabile isotoper; for tungere grundstoffer kræves flere neutroner for at stabilisere kernen. Hvis en kerne har for mange eller for få neutroner i forhold til protonerne, kan den være radioaktiv og forsøge at opnå en mere stabil sammensætning ved at udsende stråling (alpha-, beta- eller gamma-stråling).
Halveringstid og henfaldstyper
Ustabile isotoper beskrives ofte ved deres halveringstid, den tid det tager, før halvdelen af en given mængde isotopen er omdannet. Halveringstider spænder fra brøkdele af et sekund til milliarder af år afhængigt af isotopen. Typiske henfaldstyper er:
- Alfa-henfald: udsendelse af en heliumkerne (2 protoner + 2 neutroner).
- Beta-henfald: omdannelse af en neutron til en proton (eller omvendt) med udsendelse af en elektron eller positron og en neutrino.
- Gamma-udsendelse: energi udsendes fra en exciteret nuklear tilstand i form af elektromagnetisk stråling.
Eksempler på isotoper
- Hydrogen: har tre almindelige isotoper — protium (1H, ingen neutron), deuterium (2H, én neutron) og tritium (3H, to neutroner; radioaktiv).
- Kulstof: kulstof-12 (stabil) og kulstof-14 (radioaktiv, bruges til datering af organiske materialer).
- Uran: U-235 (kan spaltes i kernekraft og våben) og U-238 (mere almindelig, langsomt henfaldende).
Anvendelser af isotoper
Isotoper har mange praktiske anvendelser i forskning, industri og medicin:
- Archaeologisk og geologisk datering (f.eks. kulstof-14-datering).
- Medicin: radioaktive isotoper bruges til diagnose og behandling (f.eks. diagnostiske sporstoffer og behandling af kræft).
- Industrielle sporstoffer: lækagedetektion, materialeforskning og sporstofforsøg.
- Energi: brændselsisotoper i kernekraft og forskning i fusionsenergi (f.eks. deuterium og tritium).
Ordet "isotop" kommer af græsk og betyder "samme sted" — isotoper af et grundstof står nemlig på samme sted i det periodiske system, fordi de har samme antal protoner, selvom deres neutrontal og masse kan være forskellige.
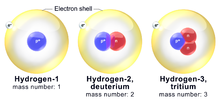
Isotoper af brint
Kemiske egenskaber
I ethvert neutralt atom er antallet af elektroner det samme som antallet af protoner. Derfor har isotoper af det samme grundstof også det samme antal elektroner og den samme elektroniske struktur. Den måde, et atom opfører sig på, bestemmes af dets elektroniske struktur, så isotoper af det samme grundstof har næsten samme kemiske adfærd, f.eks. de molekyler, de kan danne. Det er meget vanskeligt at adskille isotoper af et grundstof fra en blanding af forskellige isotoper, fordi denne adfærd er så ens.
Tungere isotoper reagerer kemisk langsommere end lettere isotoper af det samme grundstof. Denne "masseeffekt" er stor for protium (1 H) og deuterium (2 H), fordi deuterium har dobbelt så stor masse som protium. For tungere grundstoffer er det relative atomvægtforhold mellem isotoper meget mindre, så masseeffekten er normalt lille.
Stabilitet
Nogle isotoper er ikke stabile, så de ændrer sig til en anden isotop eller et andet grundstof ved radioaktivt henfald. Disse kaldes ustabile isotoper eller radioaktive isotoper. Den gennemsnitlige tid, det tager en isotop at henfalde, kaldes halveringstiden. Andre isotoper henfalder ikke, så de er ikke radioaktive. De kaldes stabile isotoper.
Alle atomer har en atomkerne, som består af protoner og neutroner, der holdes sammen af kernekraften. Fordi protoner har positiv elektrisk ladning, frastøder de hinanden. Neutroner er neutrale og stabiliserer kernen. Neutronerne holder protonerne lidt fra hinanden. Dette reducerer den elektrostatiske frastødning mellem protonerne, så kernekraften kan holde protonerne og neutronerne sammen. En eller flere neutroner er nødvendige for, at to eller flere protoner kan bindes sammen til en kerne. Efterhånden som antallet af protoner stiger, stiger også antallet af neutroner, der er nødvendige for at få en stabil kerne.
Nogle grundstoffer har kun en enkelt isotop, som er stabil. F.eks. er fluor-19 (19 F) den eneste stabile isotop af fluor. De andre isotoper af fluor henfalder hurtigt, så de findes ikke i naturen. Andre grundstoffer har mange stabile isotoper. F.eks. har xenon syv stabile isotoper. Det har også to isotoper, der henfalder meget langsomt, og som findes i naturen. Det største antal stabile isotoper for et grundstof er ti, nemlig for grundstoffet tin. Nogle grundstoffer har ingen stabile isotoper, f.eks. curium. Disse findes kun på Jorden, fordi de skabes i atomreaktorer, kerneeksplosioner eller partikelacceleratorer.
Nogle ustabile isotoper findes naturligt på Jorden, fordi de har en meget lang halveringstid. For eksempel har uran-238 en halveringstid på 4468 millioner år. Halveringstiden for radium-226 er kun 1600 år, og det findes i naturen, fordi det hele tiden dannes fra uran-238's henfald.
Brint har tre almindelige isotoper. Den mest almindelige isotop af brint kaldes protium (1 H), som har én proton og ingen neutroner. Et brintatom, der har en proton og en neutron (atommasse 2), kaldes deuterium (2 H). Brintatom med én proton og to neutroner (atommasse 3) kaldes tritium (3 H). Protium og deuterium er stabile isotoper, mens tritium er en radioaktiv isotop.
De tungeste grundstoffer i det periodiske system er alle radioaktive. Alle isotoper af radon, thorium og uran er radioaktive, da de er meget tunge. Det skyldes, at kernekræfterne i atomets kerne ikke kan holde alle protonerne og neutronerne sammen.
Relaterede sider
- Isotopisk elektrokemi
- Radionuklid
Spørgsmål og svar
Q: Hvad er isotoper?
A: Isotoper er forskellige typer af atomer af et kemisk grundstof, som har meget ens opførsel, men vejer forskellige mængder.
Q: Hvordan adskiller isotoper sig fra hinanden?
A: Atomer af det samme grundstof har det samme antal protoner, men forskellige isotoper har forskellige antal neutroner. Som følge heraf har de også forskellige massetal, som er antallet af protoner plus antallet af neutroner.
Spørgsmål: Er alle isotoper stabile?
Svar: Nej, nogle isotoper er ikke stabile, så de ændrer sig til en anden isotop eller et andet grundstof ved radioaktivt henfald. Disse kaldes radioaktive isotoper, mens andre, som ikke er radioaktive, kaldes stabile isotoper.
Spørgsmål: Hvordan kan en isotop identificeres?
A: En isotop navngives normalt ved at angive grundstoffet og dets massetal. F.eks. er kulstof-12 eller 12C et atom med 6 protoner og 6 neutroner, mens kulstof-14 eller 14C i stedet har 8 neutroner.
Spørgsmål: Hvad betyder "isotop"?
A: Ordet "isotop" betyder "på samme sted" og henviser til, at alle atomer af det samme grundstof optræder samme sted i det periodiske system.
Spørgsmål: Hvorfor vejer atomer med flere neutroner mere end atomer med færre neutroner?
Svar: Atomer med flere neutroner vejer mere, fordi de indeholder ekstra partikler (neutroner), der øger deres samlede masse i forhold til atomer med færre neutroner.
Søge