Kulstof er et meget vigtigt kemisk grundstof med det kemiske symbol C. Alt kendt liv på Jorden har brug for det. Kulstof har en atommasse på cirka 12 (grundlaget er isotopen C‑12) og et atomnummer på 6. Det er et nonmetal, hvilket betyder, at det ikke er et metal. Kulstofs evne til at danne fire kovalente bindinger gør det særligt velegnet til at bygge komplekse molekyler.
Egenskaber og allotroper
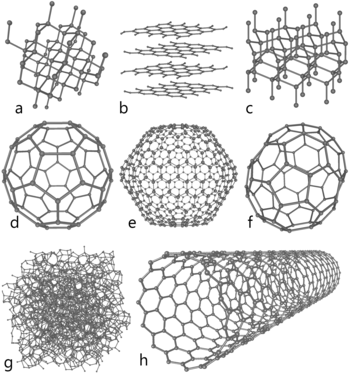
Kulstof findes i flere forskellige strukturelle former (allotroper), der har meget forskellige egenskaber:
- Grafit – blødt, skinnende sort materiale, leder elektricitet i planerne, bruges som smøremiddel og elektroder.
- Diamant – ekstremt hårdt og gennemsigtigt, bruges til smykker og industrielle skæreværktøjer.
- Grafen – et enkelt lag af carbonatomer i et hexagonalt gitter med enestående mekaniske og elektriske egenskaber.
- Fullerenes og karbonrør (nanorør) – molekylære og nanostrukturer med særlige elektroniske og mekaniske egenskaber.
- Amorft kulstof – fx sod og kul, mangler langdistanceorden, bruges som brændstof og i filtre.
Kulstof sublimerer ved meget høje temperaturer (går fra fast til gas uden at smelte under normalt tryk). Det kan indgå i stærke enkelt-, dobbelt- og tripelbindinger, og danner stabile kæder og ringe, som er grundlaget for organisk kemi.
Kulstof i liv og biokemi
Kulstof er rygraden i alle organiske molekyler: kulhydrater, lipider, proteiner og nukleinsyrer (DNA/RNA) indeholder kulstofskeletter, som bestemmer struktur og funktion. Fotosyntese omdanner atmosfærisk CO2 til organiske forbindelser, som videreføres gennem fødekæder. Åndedræt, nedbrydning og forbrænding frigiver igen kulstof som CO2, hvilket indgår i det globale kulstofkredsløb.
Kulstof i materialer og industri
Når jern legeres med kulstof, dannes der hårdt stål. Kulstoffets mængde og form (fx som sementit eller grafit) påvirker stålets hårdhed, sejrbarhed og sprødhed:
- Lavt kulstofindhold (< 0,3 %) giver sejere og mere formbart stål (bruges til bilkarrosserier, rør).
- Højere kulstofindhold (0,6–1,0 %) giver hårdere, men mere sprødt stål (værktøjsstål).
- Støbejern har ofte højt kulstofindhold og grafitindhold, hvilket giver gode støbeegenskaber.
Ud over stål er kulstof centralt i mange industrielle materialer: aktivt kul til rensning, kulfiber til letvægtsstrukturer, diamant til skære- og polerværktøj samt grafit til elektroder. Nanoteknologiske former som karbonrør og grafen anvendes i elektronik, kompositter og avancerede materialer.
Energi, kul og miljø
Kul er et vigtigt fossilt brændstof og har gennem historien været en stor energikilde i industrien. Forbrænding af kul, olie og gas oxiderer kulstof til CO2, en drivhusgas, der bidrager til global opvarmning. Derfor er håndtering af kulstofudslip, energieffektivitet og omstilling til lavemissionsenergikilder centrale emner i klimaindsatsen. Kulstoflagring (carbon capture and storage) og naturbaserede løsninger (fx skovrejsning) forsøger at mindske atmosfærens CO2-indhold.
Isotoper og datering
Kulstof har flere isotoper. De vigtigste er stabile C‑12 og C‑13 samt den radioaktive C‑14. Atommassen på cirka 12 refererer til C‑12. C‑14 bruges til radiocarbon-datering af organisk materiale og har en halveringstid på omkring 5.730 år, hvilket gør den nyttig til datering af prøver op til ~50.000 år gamle.
Opsummering
Kulstof er et alsidigt og livsvigtigt grundstof. Dets særlige kemiske egenskaber gør det fundamentalt for organisk kemi, levende organismer og en lang række materialer — fra blødt grafit til ekstremt hård diamant og stærke kompositter. Samtidig skaber udvekslingen af kulstof i atmosfære, biosfære og geosfære både muligheder og udfordringer i forhold til energi, ressourcer og klima.