Denne artikel handler kun om alkoholernes kemi.
Den alkohol, der anvendes i drikkevarer, er ethanol. Du kan finde flere oplysninger på siden Alkoholisk drik og alkoholisme.
Inden for kemi er alkohol et generelt begreb, der henviser til mange organiske forbindelser, der anvendes i industrien og videnskaben som reagenser, opløsningsmidler og brændstoffer. Alkoholer er kulhydrater, der består af en alkylgruppe med en eller flere hydroxylgrupper (-OH) bundet til kulstofatomerne. Alkohol er farveløs og også gennemsigtig.
Korrekt præcisering: I kemisk forstand er alkoholer ikke det samme som kulhydrater. Kulhydrater er en specifik gruppe biomolekyler (fx sukkerarter), mens alkoholer er en bred klasse af organiske forbindelser karakteriseret ved en eller flere hydroxylgrupper (-OH) bundet til carbon. Mange simple alkoholer er farveløse væsker ved stuetemperatur, men egenskaberne varierer med molekylstrukturen.
Definition og systematisk navngivning
Alkoholer er organiske forbindelser med mindst én hydroxylgruppe (-OH) bundet til et mættet carbonatom. I IUPAC-navngivning angives alkoholer med suffikset -ol (fx methanol, ethanol, propan-1-ol). Hvis der er flere hydroxylgrupper, anvendes -diol, -triol osv. Der findes også almindelige/traditionelle navne (fx isopropylalkohol = 2-propanol).
Klassifikation
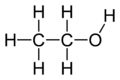
- Primær alkohol: Hydroxylgruppen sidder på et carbon bundet til én anden carbon (eller kun én substituent). Fx ethanol (CH3CH2OH).
- Sekundær alkohol: Hydroxylgruppen sidder på et carbon bundet til to andre carbonatomer. Fx 2-propanol (isopropanol).
- Tertiær alkohol: Hydroxylgruppen sidder på et carbon bundet til tre andre carbonatomer. Tertiære alkoholer oxideres typisk ikke let til carbonylforbindelser.
- Polyhydroxylalkoholer (polyoler): Indeholder flere -OH grupper, fx ethylenglycol (ethandiol), glycerol (1,2,3-propantriol).
- Phenoler: Har -OH bundet til et aromatisk ringkarbon; disse er kemisk set forskellig fra alifatiske alkoholer og har andre egenskaber og surhedsgrad.
Fysiske egenskaber
- Farve og tilstandsform: Mange simple alkoholer (methanol, ethanol, propanol) er farveløse væsker ved stuetemperatur; lavmolekylære alkoholer kan også være flygtige.
- Hydrogenbinding: Hydroxylgruppen giver mulighed for hydrogenbinding, hvilket øger kogepunkter og viskositet sammenlignet med tilsvarende kulbrinter.
- Opløselighed i vand: Små alkoholer er godt vandopløselige pga. hydrogenbinding. Opløseligheden falder med stigende længde af den hydrofobe alkylkæde.
- Surhedsgrad: Alkoholer er svage syrer med typiske pKa-værdier omkring 16–18 for alifatiske alkoholer; de kan afprotoneres kun af stærke baser (fx NaH, organometalliske reagenser).
Vigtige reaktionstyper
- Oxidation: Primære alkoholer kan oxideres til aldehyder og videre til carboxylsyrer; sekundære alkoholer til ketoner; tertiære alkoholer modstår ofte oxidation uden brud af carbonkæden.
- Esterificering: Reaktion med carboxylsyrer under syrekatalyse (Fischer-esterificering) danner estere og vand.
- Dehydrering: Syrekatalyseret fjernelse af vand fra alkoholer danner ofte alken (elimineringsreaktion).
- Substitution: Hydroxylgruppen kan erstattes af andre grupper via aktivering (fx konvertering til tosylat) eller under sure forhold (SN1/SN2 afhængig af substrat).
- Reduktion: Carbonylforbindelser (aldehyder/ketoner) kan reduceres til alkoholer (fx med NaBH4 eller LiAlH4).
Fremstilling
- Hydratisering af alken: Alken + H2O (syrekatalyse eller katalytisk hydroformylering) → alkohol.
- Reduktion af carbonylforbindelser: Aldehyder/ketoner → alkoholer (med hydride-donorer som NaBH4, LiAlH4).
- Grignard-reaktion: Carbonylforbindelser + RMgX → efter hydrolyse alkoholer (bruges til at danne sekundære/tertiære alkoholer).
- Fermentation: I bioteknologi fremstilles ethanol ved gæring af sukkerstoffer (relevant for drikkevarer og biobrændstoffer).
Anvendelser
- Opløsningsmidler: Mange organiske synteser og formuleringer bruger alkoholer pga. polaritet og opløsningsevne.
- Brændstof og additiver: Ethanol anvendes som bioethanol (transportbrændstof) og som additiv i benzin.
- Antiseptika og desinfektionsmidler: Ethanol og isopropanol bruges i medicinske desinfektionsmidler og håndsprit.
- Kemisk råvare: Fremstilling af estere, opløsningsmidler, emulgatorer, plastforstadier og farmaceutiske mellemprodukter.
- Frostvæsker: Ethylenglycol og propylenglycol anvendes i kølesystemer og som antifreeze.
Sikkerhed og toksicitet
- Brandfare: Mange alkoholer er brandfarlige væsker; opbevaring og håndtering kræver passende sikkerhedsforanstaltninger.
- Toksicitet: Methanol er særligt giftig — indtagelse kan føre til blindhed og død pga. metabolitter (formaldehyd, myresyre). Ethanol er centrale nervøs system-depressiv og kan give forgiftning; langvarig misbrug fører til helbredsskader.
- Arbejdssikkerhed: God ventilation, korrekt mærkning, brug af handsker og øjenbeskyttelse anbefales ved håndtering af koncentrerede alkoholer.
Eksempler på almindelige alkoholer
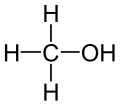
- Methanol (CH3OH) – enkelt, meget giftig og anvendes som opløsningsmiddel og råmateriale.
- Ethanol (C2H5OH) – drikkevarealkohol, opløsningsmiddel, desinfektion og brændstof.
- Isopropanol (2-propanol) – almindeligt desinfektionsmiddel og opløsningsmiddel.
- Ethylenglycol (ethandiol) – antifrostvæske.
- Glycerol (1,2,3-propantriol) – fugtighedsbevarende middel i kosmetik og farmaci.
Afsluttende bemærkninger
Alkoholer udgør en stor og alsidig gruppe forbindelser i organisk kemi med mange praktiske anvendelser og karakteristiske kemiske reaktioner. Deres egenskaber bestemmes i høj grad af antal og placering af hydroxylgrupper samt længden og forgrening af alkylkæderne. Ved arbejde med alkoholer er det vigtigt at være opmærksom på sikkerhed, især ved håndtering af giftige eller brandfarlige eksemplarer.