Kovalente bindinger er kemiske bindinger mellem to ikke-metalatomer. Et typisk eksempel er vand, hvor hydrogen (H) og oxygen (O) bindes sammen til (H2O). I mange tilfælde søger atomer at opfylde en fuld ydre skal — normalt otte elektroner (ottetalsreglen), bortset fra de letteste atomer som hydrogen og helium, som er tilfredse med to elektroner. Valenselektroner er de elektroner, der befinder sig i atomets ydre skal og som oftest er involveret i kemi og bindinger. Elektronskallenes struktur og energiniveauer bestemmes af kvantemekanikken.
Hvordan dannes kovalente bindinger?
Antallet af elektroner i et atom svarer til antallet af protoner i kernen, og elektronerne bevæger sig i fordelingsområder omkring kernen, ofte omtalt som orbitaler. Det inderste niveau kan rumme op til to elektroner, mens de næste niveauer typisk kan rumme op til otte i henhold til simple regler for opbygning. Kovalente bindinger dannes, når to atomer deler et eller flere par af valenselektroner, så hvert atom opnår en mere stabil elektronkonfiguration.
Når to atomer nærmer sig hinanden, kan deres atomorbitale overlappe og danne nye molekylorbitaler. Et overlappende orbital kan være af lavere energi (et bindende orbital), hvilket gør det energetisk fordelagtigt for en elektron at blive delt mellem de to kerner. Når en elektron går over i dette lavere energiniveau, frigives energi (f.eks. i form af en foton), og resultatet er et stabilt bundet system — en kovalent binding. For at adskille de to atomer igen skal der tilføres energi svarende til den energi, der blev frigivet ved dannelsen (bindingens bindingsenergi).
Polære versus upolære kovalente bindinger
Kovalente bindinger spænder fra helt upolære (når de to atomer trækker lige meget i deres fælles elektronpar, fx i H2 eller Cl2) til polære (når et af atomerne trækker elektronparret stærkere til sig). Forskellen skyldes elektronegativitet — et mål for et atoms evne til at tiltrække elektroner i en binding. Hvis forskellen i elektronegativitet er stor, bliver elektronparret forskudt mod det mest elektronegative atom, hvilket skaber en partiel negativ ladning (δ-) dér og en partiel positiv ladning (δ+) ved det andet atom.
Vand som konkret eksempel
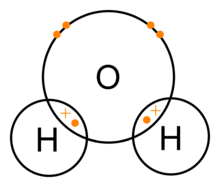
Et vandmolekyle består af et oxygenatom og to hydrogenatomer, der holdes sammen af kovalente bindinger. Oxygen deler et elektronpar med hvert hydrogenatom, men fordi oxygen er betydeligt mere elektronegativt end hydrogen, trækkes elektronparrene en smule tættere på oxygen. Det gør oxygen svagt negativt (δ-) og hvert hydrogen svagt positivt (δ+). Dermed er vand et polært molekyle: ladningen er ikke jævnt fordelt.
Den polære natur af vand giver anledning til stærke interaktioner mellem molekylerne: et hydrogenatom bundet til oxygen i ét molekyle kan tiltrækkes af et ensomt elektronpar (lone pair) på oxygen i et andet molekyle — dette kaldes hydrogenbinding. Hydrogenbindinger forklarer mange af vands usædvanlige egenskaber, fx høj kogepunkt i forhold til andre små molekyler, overfladespænding og at is er mindre tæt end flydende vand.
Vigtige kendetegn ved kovalente bindinger
- Dannelsesmekanisme: Deling af elektroner mellem atomer via overlappende orbitaler.
- Bindingstype: Kan være enkelt-, dobbelt- eller tripelbinding afhængig af hvor mange elektronpar der deles.
- Polær vs. upolær: Afhænger af forskellen i elektronegativitet mellem de bundne atomer.
- Egenskaber: Molekyler med kovalente bindinger kan være gasformige, flydende eller faste ved stuetemperatur; de leder generelt ikke elektricitet i fast tilstand (medmindre ioniseret eller ekstremt polar og i opløsning).
- Bindingens energi: Kovalente bindinger har karakteristiske bindingsenergier, og stærkere bindinger kræver mere energi at bryde.
Kort sagt giver kovalente bindinger en fleksibel og meget udbredt måde, hvorpå ikke-metaler danner stabile molekyler ved at dele elektroner. Forståelsen af, hvordan orbitaler overlapper, og hvordan elektronegativitet påvirker elektronfordelingen, er central for at forudsige molekylers form og egenskaber.