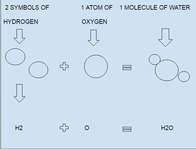
Kemisk formel er en kortfattet måde kemikere beskriver et stofs sammensætning på. En formel angiver, hvilke kemiske grundstoffer der indgår, og hvor mange atomer af hver type der er i en enkelt enhed (fx et molekyle eller en formelenhed). Nogle formler angiver også, hvordan atomerne er forbundet, eller hvordan de er anbragt i rummet, men andre viser kun det samlede antal af hvert atom.
Elementsymboler og indeks
Hvert grundstof repræsenteres af et eller to bogstaver (elementets symbol). Et undertal eller indeks angiver antallet af atomer af det pågældende element i formelen. For eksempel har hydrogenperoxid formlen H2O2. Metan består af ét kulstofatom (C) og fire hydrogenatomer, derfor CH4. Sukkermolekylet glukose har seks kulstofatomer, tolv hydrogenatomer og seks oxygenatomer: C6H12O6.
Typer af kemiske formler
- Molær (molekylær) formel: Viser det nøjagtige antal atomer i et molekyle (fx C6H12O6).
- Empirisk formel: Viser det relative antal atomer i simpleste heltal (fx CH2O er den empiriske formel for glukose C6H12O6).
- Strukturel formel: Viser, hvordan atomerne er bundet sammen (f.eks. linjeformler eller tegninger med bindinger).
- Kondenseret strukturel formel: En kompakt måde at skrive strukturinformation på, fx CH3CH2OH for ethanol.
- Skeletformel: Bruges ofte for organiske molekyler; kulstofskelet vises som streger, hydrogen bundet til kulstof udelades typisk.
- Ionisk formel: Viser sammensætningen af ionforbindelser, ofte med ladninger angivet (fx NaCl, CaCO3 eller NH4Cl).
Koeficienter, parenteser og ladninger
Ved kemiske reaktioner bruges koefficienter foran formlerne til at angive antal enheder (stoikiometri). For eksempel i 2 H2 + O2 → 2 H2O er tallet 2 en koefficient. Parenteser bruges, når en gruppe af atomer gentages, fx (NH4)2SO4 (ammoniumsulfat) betyder, at ammoniumgruppen NH4 optræder to gange. Ioners ladninger skrives med + eller −, evt. med tal foran ladningen, fx Na+, SO42−.
Brug i kemiske ligninger og reaktioner
Kemiske formler indgår i kemiske ligninger til at beskrive kemiske reaktioner. Formlerne fortæller, hvilke stoffer der reagerer, og hvilke produkter der dannes. For at ligningen er korrekt skal atomernes antal af hvert grundstof være afstemt (konservering af masse). Ofte angives tilstande med (s), (l), (g) eller (aq) for henholdsvis fast, væske, gas og opløsning.
Hvad en formel ikke viser
En simpel molekylformel viser ikke altid molekylets struktur eller 3D-geometri. Isomerer (stoffer med samme molekylformel men forskellig struktur) har derfor samme molekylformel men forskellige egenskaber. For detaljeret struktur anvendes strukturelle formler, stereokemisk notation (fx wedge/dash) eller modeller som Fischer- og Newmanprojektioner.
Konventioner og gode vaner
- Elementsymboler skrives med stort forbogstav og evt. lille andet bogstav (f.eks. C, Cl, Fe).
- Undertal (subscripts) gælder kun for det forudgående element eller gruppering.
- Ved oxoanioner og komplekse ioner skal man være opmærksom på ladninger og den korrekte samlede formel for neutralitet.
- Læs formler både som "hvad" (hvilke atomer) og som "hvor mange" (antal atomer/enheder) — det hjælper ved beregninger og støkiometri.
Historie
Systemet med symbolsprog og formler blev formaliseret i det 19. århundrede af den svenske kemiker Jöns Jacob Berzelius fra, som indførte brugen af bogstaver til repræsentation af grundstoffer og tal for atomernes antal.
Praktiske tips: Når du støder på en kemisk formel, prøv at identificere elementerne, noter eventuelle parenteser og koefficienter, og overvej om formlen angiver struktur eller blot sammensætning. Brug formler aktivt i beregninger af mol, masse og koncentration — de er nøglen til forståelse af kemiens kvantitative sider.