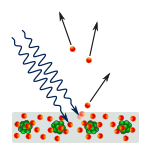
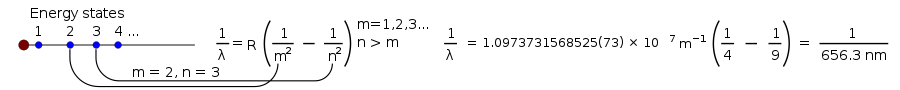Kvantemekanikkens formler og idéer blev udviklet for at forklare det lys, der kommer fra glødende brint. Kvanteteorien om atomet skulle også forklare, hvorfor elektronen forbliver i sin bane, hvilket andre idéer ikke kunne forklare. Det fulgte af de ældre ideer, at elektronen skulle falde ind i atomets centrum, fordi den i begyndelsen blev holdt i kredsløb af sin egen energi, men den ville hurtigt miste sin energi, når den kredser i sit kredsløb. (Dette skyldes, at man vidste, at elektroner og andre ladede partikler udsendte lys og mistede energi, når de ændrede hastighed eller drejede).
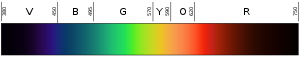
Brintlamper fungerer som neonlamper, men neonlamper har deres egen unikke gruppe af farver (og frekvenser) af lys. Forskere fandt ud af, at de kunne identificere alle grundstoffer ved hjælp af de lysfarver, de frembringer. De kunne bare ikke finde ud af, hvordan frekvenserne blev bestemt.
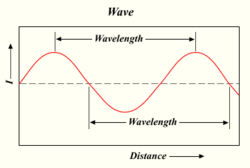
Derefter fandt en schweizisk matematiker ved navn Johann Balmer ud af en ligning, der angav, hvad λ (lambda for bølgelængde) ville være:
λ = B ( n 2 n 2 2 - 4 ) n = 3 , 4 , 5 , 6 {\displaystyle \lambda =B\left({\frac {n^{2}}}{n^{2}-4}}}\right)\qquad \qquad n=3,4,5,6} 
hvor B er et tal, som Balmer har bestemt til 364,56 nm.
Denne ligning fungerede kun for det synlige lys fra en brintlampe. Men senere blev ligningen gjort mere generel:
1 λ = R ( 1 m 2 - 1 n 2 ) , {\displaystyle {\frac {\frac {1}{\lambda }}=R\left({\frac {\frac {1}{m^{2}}}}-{\frac {1}{n^{2}}}}}}\right),} 
hvor R er Rydberg-konstanten, som er lig med 0,0110 nm−1 , og n skal være større end m.
Ved at indsætte forskellige tal for m og n er det let at forudsige frekvenser for mange typer lys (ultraviolet, synligt og infrarødt lys). For at se, hvordan det fungerer, skal du gå ind på Hyperphysics og gå ned efter midten af siden. (Brug H = 1 for hydrogen.)
I 1908 udviklede Walter Ritz Ritz-kombinationsprincippet, der viser, hvordan visse mellemrum mellem frekvenser gentager sig selv. Dette viste sig at være vigtigt for Werner Heisenberg flere år senere.
I 1905 brugte Albert Einstein Plancks idé til at vise, at en lysstråle består af en strøm af partikler kaldet fotoner. Energien af hver foton afhænger af dens frekvens. Einsteins idé er begyndelsen til kvantemekanikkens idé om, at alle subatomare partikler som elektroner, protoner, neutroner og andre er både bølger og partikler på samme tid. (Se billedet af atom med elektronen som bølger ved atom.) Dette førte til en teori om subatomare partikler og elektromagnetiske bølger kaldet bølge-partikel-dualitet. Her var partikler og bølger hverken det ene eller det andet, men havde visse egenskaber af begge dele.
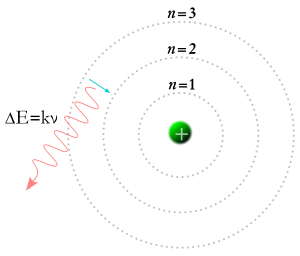
I 1913 fik Niels Bohr den idé, at elektroner kun kunne indtage bestemte baner omkring atomkernen. Ifølge Bohrs teori kunne tallene m og n i ligningen ovenfor repræsentere baner. Bohrs teori sagde, at elektroner kunne begynde i en bane m og ende i en bane n, eller at en elektron kunne begynde i en bane n og ende i en bane m, så hvis en foton rammer en elektron, vil dens energi blive absorberet, og elektronen vil bevæge sig til en højere bane på grund af den ekstra energi. Ifølge Bohrs teori vil en elektron, hvis den falder fra en højere bane til en lavere bane, være nødt til at afgive energi i form af en foton. Fotonens energi vil svare til energiforskellen mellem de to baner, og fotonens energi gør, at den har en bestemt frekvens og farve. Bohrs teori gav en god forklaring på mange aspekter af subatomare fænomener, men kunne ikke svare på, hvorfor hver af de lysfarver, der produceres af glødende brint (og af glødende neon eller ethvert andet grundstof), har sin egen lysstyrke, og at lysstyrkeforskellene altid er de samme for hvert grundstof.
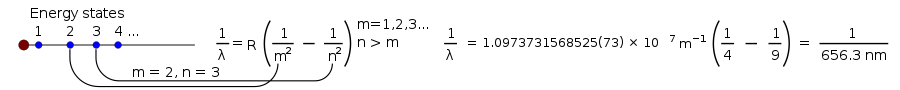
Da Niels Bohr kom med sin teori, vidste man det meste om det lys, der produceres af en brintlampe, men forskerne kunne stadig ikke forklare lysstyrken af de enkelte linjer, der produceres af glødende brint.
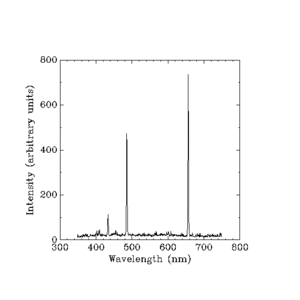
Werner Heisenberg påtog sig opgaven med at forklare lysstyrken eller "intensiteten" af hver linje. Han kunne ikke bruge nogen simpel regel som den, Balmer havde fundet frem til. Han var nødt til at bruge den klassiske fysiks meget vanskelige matematik, som udregner alting i form af ting som en elektrons masse (vægt), ladning (statisk elektrisk styrke) og andre små størrelser. Den klassiske fysik havde allerede svar på lysstyrken af de farvebånd, som en brintlampe frembringer, men den klassiske teori sagde, at der skulle være en kontinuerlig regnbue og ikke fire separate farvebånd. Heisenbergs forklaring er:
Der er en lov, der siger, hvilke lysfrekvenser lysende brint vil producere. Den skal forudsige, at frekvenserne er spredte, når de involverede elektroner bevæger sig mellem baner tæt på atomets kerne (centrum), men den skal også forudsige, at frekvenserne vil komme tættere og tættere på hinanden, når vi ser på, hvad elektronen gør, når den bevæger sig mellem baner længere og længere væk. Den skal også forudsige, at intensitetsforskellene mellem frekvenserne bliver tættere og tættere på hinanden, efterhånden som vi bevæger os udad. Hvor den klassiske fysik allerede giver de rigtige svar ved hjælp af ét sæt ligninger, skal den nye fysik give de samme svar, men ved hjælp af andre ligninger.
Den klassiske fysik bruger Joseph Fouriers matematiske metoder til at lave et matematisk billede af den fysiske verden, Den bruger samlinger af glatte kurver, der går sammen til én glat kurve, som i dette tilfælde giver intensiteter for lys af alle frekvenser fra noget lys. Men det er ikke rigtigt, fordi denne glatte kurve kun vises ved højere frekvenser. Ved lavere frekvenser er der altid isolerede punkter, og der er intet, der forbinder punkterne. Så for at lave et kort over den virkelige verden måtte Heisenberg foretage en stor ændring. Han var nødt til at gøre noget for kun at udvælge de tal, der ville stemme overens med det, der blev set i naturen. Nogle gange siger folk, at han "gættede" på disse ligninger, men han gættede ikke i blinde. Han fandt det, han havde brug for. De tal, som han beregnede, ville sætte prikker på en graf, men der ville ikke blive tegnet nogen linje mellem prikkerne. Og hvis man lavede en "graf" med prikker for hver enkelt beregning, ville man have spildt en masse papir og ikke have fået noget ud af det. Heisenberg fandt en måde at forudsige intensiteterne for forskellige frekvenser på en effektiv måde og at organisere disse oplysninger på en nyttig måde.
Ved blot at bruge den empiriske regel, som Balmer startede og Rydberg forbedrede, kan vi se, hvordan vi kan få et sæt tal, der ville hjælpe Heisenberg med at få det billede, han ønskede:
Reglen siger, at når elektronen bevæger sig fra en bane til en anden, vinder eller taber den enten energi, alt efter om den kommer længere væk fra centrum eller tættere på det. Så vi kan sætte disse baner eller energiniveauer ind som overskrifter langs toppen og siden af et gitter. Af historiske årsager kaldes den laveste bane for n, og den næste bane udad kaldes n - a, derefter kommer n - b osv. Det er forvirrende, at de brugte negative tal, når elektronerne faktisk fik mere energi, men sådan er det bare.
Da Rydberg-reglen giver os frekvenser, kan vi bruge denne regel til at sætte tal ind, afhængigt af hvor elektronen går hen. Hvis elektronen starter ved n og ender ved n, er den ikke rigtig gået nogen steder, så den har ikke vundet energi, og den har ikke mistet energi. Så frekvensen er 0. Hvis elektronen starter ved n-a og ender ved n, er den faldet fra en højere bane til en lavere bane. Hvis den gør det, så mister den energi, og den energi, den mister, viser sig som en foton. Fotonen har en vis mængde energi, e, og den er relateret til en bestemt frekvens f ved ligningen e = h f. Vi ved altså, at en bestemt ændring af kredsløb vil give en bestemt frekvens af lys, f. Hvis elektronen starter ved n og ender ved n - a, betyder det, at den er gået fra et lavere kredsløb til et højere kredsløb. Det sker kun, når en foton med en bestemt frekvens og energi kommer ind udefra, absorberes af elektronen og giver den energi, og det er det, der får elektronen til at gå ud til en højere bane. Så for at det hele skal give mening, skriver vi denne frekvens som et negativt tal. Der var en foton med en bestemt frekvens, og nu er den blevet taget væk.
Så vi kan lave et gitter som dette, hvor f(a←b) betyder den frekvens, der er involveret, når en elektron går fra energitilstand (bane) b til energitilstand a (igen, sekvenserne ser bagvendte ud, men det er sådan, de oprindeligt blev skrevet):
Raster af f
| Elektronertilstande | n | n-a | n-b | n-c | .... | |
| n | f(n←n) | f(n←n-a) | f(n←n-b) | f(n←n-c) | ..... | |
| n-a | f(n-a←n) | f(n-a←n-a) | f(n-a←n-b) | f(n-a←n-c) | ..... | |
| n-b | f(n-b←n) | f(n-b←n-a) | f(n-b←n-b) | f(n-b←n-c) | ..... | |
| overgang.... | ..... | ..... | ..... | ..... | | |
Heisenberg har ikke lavet gitteret på denne måde. Han lavede bare den matematik, der ville give ham de intensiteter, han søgte. Men for at gøre det var han nødt til at gange to amplituder (hvor højt en bølge måler) for at beregne intensiteten. (I klassisk fysik er intensiteten lig med amplituden i kvadrat.) Han lavede en mærkelig ligning for at løse dette problem, skrev resten af sin opgave, afleverede den til sin chef og tog på ferie. Dr. Born kiggede på sin sjove ligning, og den virkede lidt skør. Han må have tænkt: "Hvorfor gav Heisenberg mig denne mærkelige ting? Hvorfor er han nødt til at gøre det på denne måde?" Så gik det op for ham, at han så på en plan for noget, som han allerede vidste meget godt. Han var vant til at kalde det gitter eller den tabel, som vi kunne skrive ved f.eks. at lave al matematikken for frekvenser, for en matrix. Og Heisenbergs mærkelige ligning var en regel for at gange to af dem sammen. Max Born var en meget, meget god matematiker. Han vidste, at eftersom de to matricer (gitter), der blev ganget, repræsenterede forskellige ting (som f.eks. position (x,y,z) og impuls (mv)), så fik man ét svar, når man gangede den første matrix med den anden, og når man gangede den anden matrix med den første, fik man et andet svar. Selv om han ikke kendte til matrixmatematik, så Heisenberg allerede dette problem med "forskellige svar", og det havde generet ham. Men Dr. Born var så god en matematiker, at han så, at forskellen mellem den første matrixmultiplikation og den anden matrixmultiplikation altid ville involvere Plancks konstant, h, ganget med kvadratroden af negativ et, i. Så inden for få dage efter Heisenbergs opdagelse havde de allerede den grundlæggende matematik for det, som Heisenberg gerne kaldte "ubestemthedsprincippet". Med "ubestemthed" mente Heisenberg, at noget som en elektron bare ikke kan fastlåses, før den bliver fastlåst. Det er lidt ligesom en vandmand, der altid er i bevægelse og ikke kan være "på ét sted", medmindre man slår den ihjel. Senere fik folk for vane at kalde det "Heisenbergs usikkerhedsprincip", hvilket fik mange mennesker til at begå den fejl at tro, at elektroner og den slags ting virkelig er "et sted", men at vi bare er usikre på det i vores eget sind. Den idé er forkert. Det er ikke det, Heisenberg talte om. At have problemer med at måle noget er et problem, men det er ikke det problem, Heisenberg talte om.
Heisenbergs idé er meget svær at forstå, men vi kan gøre den tydeligere med et eksempel. Først vil vi begynde at kalde disse gitter for "matricer", fordi vi snart skal tale om matrixmultiplikation.
Lad os antage, at vi starter med to slags målinger, position (q) og impuls (p). I 1925 skrev Heisenberg en ligning som denne:
Y ( n , n - b ) = ∑ a p ( n , n - a ) q ( n - a , n - b ) {\displaystyle Y(n,n-b)=\sum _{a}^{}\}\,p(n,n-a)q(n-a,n-b)} (Ligning for de konjugerede variabler impuls og position)
(Ligning for de konjugerede variabler impuls og position)
Han vidste det ikke, men denne ligning giver en plan for at skrive to matricer (gitter) og for at gange dem. Reglerne for multiplikation af en matrix med en anden er lidt rodet, men her er de to matricer i henhold til tegningen og derefter deres produkt:
Matrix af p
| Elektronertilstande | n-a | n-b | n-c | .... | |
| n | p(n←n-a) | p(n←n-b) | p(n←n-c) | ..... | |
| n-a | p(n-a←n-a) | p(n-a←n-b) | p(n-a←n-c) | ..... | |
| n-b | p(n-b←n-a) | p(n-b←n-b) | p(n-b←n-c) | ..... | |
| overgang.... | ..... | ..... | ..... | ..... | |
Matrix af q
| Elektronertilstande | n-b | n-c | n-d | .... | |
| n-a | q(n-a←n-b) | q(n-a←n-c) | q(n-a←n-d) | ..... | |
| n-b | q(n-b←n-b) | q(n-b←n-c) | q(n-b←n-d) | ..... | |
| n-c | q(n-c←n-b) | q(n-c←n-c) | q(n-c←n-d) | ..... | |
| overgang.... | ..... | ..... | ..... | ..... | |
Matrixen for produktet af de to ovenstående matricer som angivet i den relevante ligning i Heisenbergs artikel fra 1925 er:
| Elektronertilstande | n-b | n-c | n-d | ..... |
| n | A | ..... | ..... | ..... |
| n-a | ..... | B | ..... | ..... |
| n-b | ..... | ..... | C | ..... |
Hvor:
A=p(n←n-a)*q(n-a←n-b)+p(n←n-b)*q(n-b←n-b)+p(n←n-c)*q(n-c←n-b)+.....
B=p(n-a←n-a)*q(n-a←n-c)+p(n-a←n-b)*q(n-b←n-c)+p(n-a←n-c)*q(n-c←n-c)+.....
C=p(n-b←n-a)*q(n-a←n-d)+p(n-b←n-b)*q(n-b←n-d)+p(n-b←n-c)*q(n-d←n-d)+.....
og så videre.
Hvis matricerne blev vendt om, ville følgende værdier blive resultatet:
A=q(n←n-a)*p(n-a←n-b)+q(n←n-b)*p(n-b←n-b)+q(n←n-c)*p(n-c←n-b)+.....
B=q(n-a←n-a)*p(n-a←n-c)+q(n-a←n-b)*p(n-b←n-c)+q(n-a←n-c)*p(n-c←n-c)+.....
C=q(n-b←n-a)*p(n-a←n-d)+q(n-b←n-b)*p(n-b←n-d)+q(n-b←n-c)*p(n-d←n-d)+.....
og så videre.
Bemærk, hvordan ændringen af multiplikationsrækkefølgen trin for trin ændrer de tal, der faktisk multipliceres.