En elektron er en meget lille del af stof. Dens symbol er e−, og den blev først påvist af J. J. Thomson i 1897 ved eksperimenter med katodestråler. Elektronen betragtes som en subatomar partikel og regnes i dag for en elementarpartikel, fordi den ikke kan opdeles i mindre bestanddele i de kendte eksperimenter.
Grundlæggende egenskaber
- Elektrisk ladning: Elektronen har en negativ elektrisk ladning med absolut værdi 1,602176634×10−19 coulomb (denne værdi er grundlaget for SI-enheden coulomb).
- Masse: Elektroner har meget lille masse: cirka 9,10938356×10−31 kg. På grund af den lave masse kræver det relativt lidt energi at give dem høj hastighed.
- Spin og kvantetype: Elektronen er en fermion med spinnet 1/2. Den indgår i Standardmodellen som en type lepton og har en antistofpartner, positronen (e+).
- Relativistiske hastigheder: Elektroner kan opnå hastigheder tæt på lysets hastighed i stærke elektriske felter eller i partikelacceleratorer; eksempelvis ses højehastighedselektroner som beta-partikler ved nogle typer radioaktivt henfald.
- Felt og magnetiske egenskaber: En elektron skaber et elektrisk felt og har et magnetisk moment. Dets bevægelse og spin medfører de magnetiske effekter, der udnyttes i mange teknologier.
Opdagelse og målinger
J. J. Thomsons arbejde med katodestråler i 1897 viste, at strålerne bestod af negativt ladede partikler (elektroner). Senere eksperimenter, bl.a. Millikans olie-dråbe-eksperiment (omkring 1909), kvantificerede elektrons ladning. Målinger af masse, ladning og magnetiske egenskaber er siden blevet finjusteret med præcise eksperimenter.
Elektronens rolle i atomet og kemi
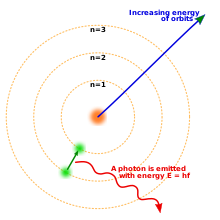
Hvert atom består af elektroner, der bevæger sig omkring atomets kerne. Elektroner kan også være helt adskilt fra et atom — frie elektroner findes i ledere, i stråling og i plasmaniveauer. I moderne kvantmekanik beskrives elektronernes tilstande af bølgefunktioner (elektronorbitaler) frem for klassiske baner.
Elektronskaller og -orbitaler (elektronskaller) bestemmer atomers kemiske egenskaber og placeringen i det periodiske system (grundstoffer) ved et givet atomnummer. Pauli-princippet og elektronernes arrangement i orbitaler forklarer kemisk binding (kovalent, ionisk, metallisk) og stoffers reaktivitet.
Interaktioner og partikelfysik
Elektroner deltager i flere fundamentale vekselvirkninger: gravitationelle, elektromagnetiske og svage vekselvirkninger. Af disse er den elektromagnetiske kraft normalt dominerende i kemiske og dagligdags situationer. Fordi elektroner har samme elektriske ladning frastøder (repellerer) de hinanden, mens de tiltrækkes af protoner med modsat ladning. Disse kræfter forklares af det elektriske felt rundt om en elektron.
I nukleare processer som beta-minus henfald udsendes ofte en elektron (sammen med en antineutrino) fra en neutron, hvilket er en manifestation af de svage vekselvirkninger. Elektroners bølge-partikel-dualitet viser sig i fænomener som elektrondiffraction og de kvantemekaniske energiniveauer i atomer.
Elektricitet, ledning og anvendelser
Den elektricitet, som driver fjernsyn, motorer, mobiltelefoner og mange andre apparater, er i metalledere i praksis mange elektroner, der bevæger sig gennem ledere. Bemærk at den konventionelle strømretning historisk er defineret som bevægelsen af positiv ladning og derfor er modsat af den faktiske gennemsnitsretning for elektroner i en metalleder.
Elektroner udnyttes i utallige teknologier: elektronmikroskoper (hvor elektronstråler giver meget høj opløsning), katodestrålerør (tidligere i fjernsyn og oscilloskoper), røntgen- og partikelacceleratorer samt i moderne elektronik og halvlederkomponenter. Superledende strøm, halvlederfysik og transistoroperation er alle knyttet til elektroners bevægelse og kvantetilstande.
Målemetoder og vigtige konstante størrelser
Fysiske konstante værdier for elektronen er målt med stor nøjagtighed: elektrisk ladning |e| = 1,602176634×10−19 C (defineret værdi i SI), og hvilemassen m_e ≈ 9,10938356×10−31 kg. Andre relevante størrelser er elektronens klassiske radius og Compton-bølgelængde, som bruges i teoretiske beskrivelser af felt- og kvanteeffekter.
Sammenfattende er elektronen en grundlæggende negativt ladet elementarpartikel med stor betydning i atomfysik, kemi, teknologi og moderne partikel- og feltteori. Dens lille masse, kvantemekaniske natur og elektriske egenskaber gør den central i næsten alle fysiske processer, der involverer stof og elektricitet.