Planck-konstanten (Plancks konstant) angiver, hvor meget energien af en foton stiger, når frekvensen af dens elektromagnetiske bølge stiger med 1 (i SI-enheder). Den er opkaldt efter fysikeren Max Planck. Planck-konstanten er en grundlæggende fysisk konstant. Den skrives som h.
Definition og centrale ligninger
Den mest kendte relation, hvor h indgår, er fotonens energi som funktion af frekvens:
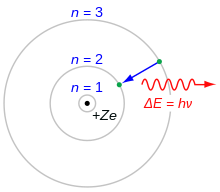
E = hν
Her er E energien og ν frekvensen. Planck-konstanten forbinder derfor kvantiserede energitrin med bølgeegenskaber. En nært beslægtet størrelse er den reducerede Planck-konstant ħ (udtales "h-bar"), defineret som ħ = h / (2π), som optræder i mange formler inden for kvantemekanik.
Dimensioner og enheder
Planck-konstanten har dimensioner af fysisk handling: energi multipliceret med tid eller impuls multipliceret med afstand. I SI-enheder udtrykkes Planck-konstanten i joule-sekunder (J⋅s), hvilket også kan skrives som (kg⋅m2⋅s−1). I SI-enheder er Planck-konstanten præcis 6,62607015×10 −34J-s (pr. definition).
Fysisk betydning og anvendelser
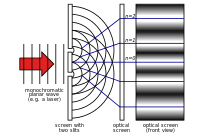
- Kvantisering af energi: At energi forbundet med elektromagnetisk stråling optræder i kvanta (fotoner) med energi E = hν var afgørende for udviklingen af kvanteteorien. Dette forklarer f.eks. fænomener som det fotoelektriske fænomen.
- De Broglie-relationen: For materiebølger forbinder Planck-konstanten bølgelængde og impuls via p = h/λ, hvor p er impuls og λ bølgelængden.
- Usikkerhedsrelationen: Den reducerede Planck-konstant ħ indgår i Heisenbergs usikkerhedsrelationer, fx Δx Δp ≥ ħ/2 og ΔE Δt ≥ ħ/2, som sætter fundamentale grænser for, hvor præcist visse par af størrelser kan kendes samtidig.
- Spektroskopi og atomfysik: Planck-konstanten bestemmer energiniveauernes adskillelse i atomer og molekyler, og den er derfor central i tolkningen af spektrallinjer og overgangsenergier.
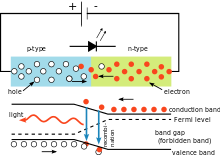
- Moderne teknologi: Den indgår indirekte i teknologier som kvantesensorer, atomure og i beskrivelser af halvleder- og fotoniske enheder.
Måling og metrologi
Indtil 2019 var kilogrammet defineret ud fra en fysisk prototype. Efter en omdefinering af SI-systemet er Planck-konstanten nu en eksakt defineret værdi, og kilogrammet er derigennem relateret til tallet h. Praktisk måles h i dag med særlige instrumenter som en Kibble-balance (tidligere kaldet watt-balance), der forbinder mekaniske størrelser med elektromagnetiske størrelser for at bestemme h meget præcist.
Planck-enheder
Fra h (ofte i kombination med gravitationskonstanten G og lysets hastighed c) kan man danne fundamentale enheder kaldet Planck-længden, Planck-tiden osv. Disse enheder angiver størrelsesordener, hvor kvantemekanik og gravitation forventes at spille lige stor rolle, og de bruges ofte som reference i teoretisk fysik.
Historisk note
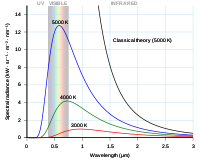
Max Planck introducerede konstanten i 1900 som et led i studiet af sort-legeme-stråling. Hans idé om kvantiserede energiniveauer lagde grundlaget for den senere udvikling af kvantemekanikken.
Opsummering: Planck-konstanten h er en grundlæggende konstant, som knytter bølgeegenskaber til kvantiseret energi, indgår i de centrale relationer i kvantemekanikken, og som også i metrologisk sammenhæng definerer moderne SI-enheder.








![Illustration fra Newtons originale brev til Royal Society (1. januar 1671 [juliansk kalender]). S repræsenterer sollys. Lyset mellem planerne BC og DE er i farve. Disse farver rekombineres til sollys på plan GH](https://www.alegsaonline.com/image/NewtonDualPrismExperiment.jpg)







![{\displaystyle h={\frac {\mu _{0}\pi }{12c^{3}}}{[{q_{0}}{[0.9163a_{0}]}^{2}]^{2}}{f_{1r}}^{5}\cdot {s}=6.63\times 10^{-34}J\cdot s}](https://www.alegsaonline.com/image/4c47db8d0ec87cc985fc3b80db4214489e87a164.svg)










