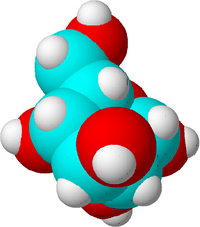
Et molekyle er den mindste enhed af et kemisk stof, der kan eksistere som dette stof med de samme kemiske egenskaber. Hvis et molekyle blev delt i mindre stykker, ville de nye stykker tilhøre et andet stof eller være reaktive fragmenter.
Hvordan er molekyler opbygget?
Molekyler består af atomer, der sidder sammen i en bestemt form ved hjælp af kemiske bindinger. Atomernes evne til at danne et bestemt antal forbindelser beskrives ofte med valens (eller oxidationstal). For eksempel:
- Ilttomer danner som regel to bindinger.
- Kulstof danner typisk fire bindinger og kan derfor bygge komplekse kæder og ringe.
- Nitrogen danner normalt tre bindinger.
Denne begrænsning i antallet af bindinger og i geometriske muligheder forklarer, hvorfor ikke alle kombinationer af atomer kan give stabile molekyler.
Typer af kemiske bindinger
Molekyler holdes sammen af forskellige typer bindinger og intermolekylære kræfter:
- Kovalente bindinger — delt elektronpar mellem atomer; kan være enkelt-, dobbelt- eller tripelbindinger. De bestemmer ofte molekylets skelet og geometri.
- Ioniske bindinger — tiltrækning mellem positive og negative ioner; almindelig i salte (ofte mindre “molekylære” i snæver forstand, men danner ioniske enheder).
- Metalbindinger — delokaliserede elektroner i metaller; giver materialer som ledningsevne og duktilitet.
- Koordinative (dative) bindinger — et atom stiller begge elektroner til et delt par.
- Intermolekylære kræfter — hydrogenbindinger, dipol-dipol-interaktioner og van der Waals-kræfter; disse bestemmer egenskaber som kogepunkt, smeltepunkt og opløselighed.
Form og geometri
Elektronpar og bindinger omkring et centralt atom bestemmer molekylets form. VSEPR-teorien (valence shell electron pair repulsion) forudsiger former som lineær, trigonal planar, tetraedrisk, bøjelig (vinkel), trigonal bipyramidal mv. Molekylgeometri påvirker egenskaber som polaritet, reaktivitet og biologisk aktivitet.
Nogle molekyler har delokaliserede elektroner og resonans, hvor den reelle elektronfordeling er et gennemsnit af flere strukturer — det ses fx i benzenringen.
Molekyler i forskellige stoftilstande
I den kinetiske teori omtales molekyle ofte om enhver gaspartikel, uanset om den er sammensat af et atom eller flere; derfor betragtes også ædelgasatomer som monoatomare “molekyler”.
I praksis optræder molekyler forskelligt afhængigt af tilstanden:
- I gasser som luft bevæger molekylerne sig frit og kolliderer elastisk; interaktionerne mellem molekyler er ofte svage sammenlignet med bindinger inde i molekylet.
- I væsker som vand er molekyler mere tæt pakkede og påvirker hinanden via intermolekylære kræfter, men de kan stadig bevæge sig og glide forbi hinanden.
- I faste stoffer som sukker er molekylerne i faste positioner i et netværk eller krystal, og kan primært vibrere omkring deres ligevægtspositioner.
- I plasma, den fjerde stoftilstand, er atomerne ofte ioniseret (elektroner revet løs) og kan ikke længere danne stabile neutrale molekyler på samme måde.
Molekylformel, strukturformel og masse
En molekylformel angiver antallet af hvert atom i et molekyle. For eksempel er molekylformlen for glukose C6H12O6, hvilket betyder seks kulstof-, tolv brint- og seks oxygenatomer i ét molekyle glukose. Ud over molekylformlen findes:
- Empirisk formel — simpel forholdsangivelse mellem grundstoffer (eks. CH2O for glukoses empiriske formel).
- Strukturformel — viser, hvordan atomer er forbundet og molekylets form (kan inkludere stereokemi).
Molekylmasse (molar masse) beregnes som summen af atommasserne og angives ofte i g/mol. Til beregninger af stofmængde anvendes mol, hvor 1 mol = 6,022×10^23 partikler (Avogadros tal).
Særlige typer molekyler og begreber
- Monoatomare “molekyler” — noble gasser som He og Ne er enkeltatomære partikler, men i gaskinetisk sammenhæng tælles de som molekyler/partikler.
- Diatomare molekyler — nogle grundstoffer forekommer naturligt som to-atomers molekyler, f.eks. H2, O2, N2 og halogener.
- Isomerer — forbindelser med samme molekylformel, men forskellig struktur (fx glukose vs. fruktose eller cis/trans-isomerer).
- Polære vs. upolære molekyler — afhænger af forskelle i elektronegativitet og molekylgeometri; polaritet påvirker opløselighed og intermolekylære kræfter.
Hvorfor er forståelsen af molekyler vigtig?
Kendskab til molekylers opbygning og egenskaber ligger til grund for kemi, biokemi, materialeforskning, lægemiddeludvikling og miljøvidenskab. Molekylære interaktioner styrer reaktioner, stoftransport, katalyse og meget mere — fra simple reaktioner i laboratoriet til komplekse biologiske processer i levende organismer.
Hvis du vil, kan jeg uddybe et afsnit (f.eks. bindingsenergi, VSEPR-modellen, beregning af molarmasse eller eksempler på isomerer) eller lave simple tegninger/ASCII-illustrationer af molekylstrukturer.