Atomorbitaler er de områder omkring atomets kerne, hvor elektronerne sandsynligvis befinder sig på et givet tidspunkt. I kvantemekanik beskrives en orbital ved en matematisk funktion, ofte kaldet en bølgefunktion ψ. Kvadratet af bølgefunktionen, |ψ|², giver sandsynlighedstæthed for at finde en elektron i et bestemt punkt i rummet — altså ikke en bestemt bane, men en sandsynlighedsfordeling i rummet omkring et atom.
Hvorfor hedder det "orbital"?
Ordet "orbital" stammer historisk fra en klassisk idé om elektroner som partikler, der bevæger sig i baner rundt om kernen, på samme måde som solsystemet, hvor kernen blev opfattet som solen, og elektronerne kredser som planeterne. Kvantemekanikken viste dog, at elektroner i stedet beskrives bedst som bølgefunktioner: begrebet "orbital" bevarede navnet, men nu som en sandsynlighedsfordeling fremfor en klassisk bane.
Hvordan beskrives orbitaler kvantemekanisk?
I atomteorien og kvantemekanikken karakteriseres en orbital af et sæt kvantetal. De vigtigste er:
- Principalkvantetallet (n) — bestemmer skalens størrelse (skal eller "shell") og energiniveauet groft set.
- Azimutkvantetallet (l) — bestemmer orbitalens form (s, p, d, f osv.).
- Magnetisk kvantetal (m) — angiver orienteringen af orbitalen i rummet.
- Spinnet (s) — elektronens egen indre vinkelmoment; to elektroner i samme orbital skal have forskelligt spin (Pauli-udelukkelsesprincippet).
Hver orbital kan rumme op til to elektroner, med modsatrettet spin. Fordelingen af elektroner i orbitalerne giver atomets elektronkonfigurationer. For en given principalkvantetalskal n findes der i alt n² orbitaler i den skal, og dermed maksimum 2n² elektroner i selve skallen.
Former, noder og spektral oprindelse
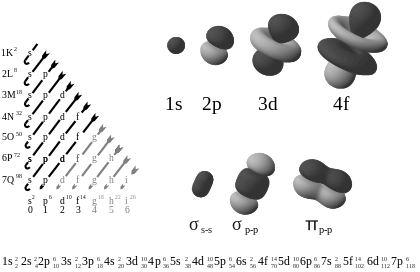
Orbitaler har karakteristiske former: s‑orbitaler er sfæriske, p‑orbitaler har to lobber (dumbbell), d‑ og f‑orbitaler har mere komplekse former med flere lobber og noder. En node er et område, hvor sandsynligheden for at finde en elektron er nul — der findes både radiale og vinkelmæssige noder.
Navnene s, p, d og f kommer fra tidlige spektroskopiske beskrivelser: man klassificerede spektrallinjer som skarpe, primære, diffuse og fundamentale; disse betegnelser er senere blevet knyttet til de respektive orbitaltyper. Faktisk blev nogle af disse begreber afledt af beskrivelser, som tidlige spektroskopikere gav af visse spektroskopiske linjer af alkalimetaller.
Hvordan findes orbitalerne i praksis?
For hydrogensystemet (én elektron) løses Schrödinger-ligningen eksakt, og man får analytiske udtryk for orbitalerne. For multielektronatomer gør elektron-elektron-interaktioner ligningen kompleks, og man anvender tilnærmelsesmetoder som Hartree–Fock, konfigurationsinteraktion eller tæthedsfunktionalteori (DFT) for at beregne orbitaler og energier.
Betydning for kemi og spektroskopi
Atomorbitaler er centrale for at forstå kemisk binding: atomer kombinerer deres atomorbitaler til molekylære orbitaler, og hybridisering (fx sp, sp2, sp3) forklarer geometrien i molekyler. Elektronovergange mellem orbitaler fører til absorption eller emission af fotoner, hvilket ligger til grund for atomer og molekylers spektrallinjer — derfor er orbitalbegrebet også afgørende i spektroskopi.
Visualisering og intuition
Orbitaler visualiseres ofte som overflader eller farvekodede tætheder, hvor en overflade kan repræsentere et område med fx 90 % sandsynlighed for at finde elektronen. Selvom billeder af orbitaler giver god intuition om form og orientering, er det vigtigt at huske, at orbitaler er matematiske funktioner — ikke faste "skaller" eller baner — og deres præcise udseende afhænger af kvantetallene og atomets elektroniske miljø.
Opsummering: En atomorbital er en kvantemekanisk bølgefunktion, der beskriver, hvor en elektron sandsynligvis findes omkring atomets kerne, og orbitalerne bestemmer elektronstrukturen i atomer (elektronkonfigurationer.) De styrer atomers kemiske egenskaber, spektrallinjer og hvordan molekyler dannes.