Gaskromatografi-massespektrometri (GC-MS) kombinerer egenskaberne ved gas-væske-kromatografi (GC) og massespektrometri (MS). Dette gør det muligt at identificere forskellige stoffer i en prøve. GC-MS har mange anvendelsesmuligheder, herunder narkotikadetektion, brandundersøgelser, miljøanalyser og sprængstofundersøgelser. Det kan også bruges til at identificere ukendte prøver. GC-MS kan også anvendes i lufthavnssikkerhedssystemet til at påvise stoffer i bagage eller på mennesker. Desuden kan GC-MS identificere sporstoffer i ødelagte materialer, selv efter at prøven er faldet så meget fra hinanden, at andre test ikke kan fungere.
GC-MS er den bedste måde for retsmedicinske eksperter at identificere stoffer på, fordi det er en specifik test. En specifik test identificerer positivt den faktiske tilstedeværelse af et bestemt stof i en given prøve. En uspecifik test siger kun, at der er kategorier af stoffer i prøven. Selv om en uspecifik test statistisk set kan antyde stoffets identitet, kan dette føre til falsk positiv identifikation.
Principper for GC-MS
GC-MS består af to hoveddele:
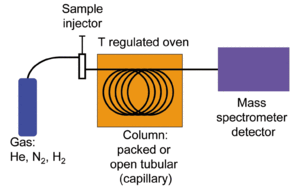
- Gaskromatografi (GC) adskiller en prøve i dens individuelle komponenter ved at føre en bæregas gennem en kolonne med en flydende eller fast stationær fase. Komponenter adskilles efter flygtighed og interaktion med kolonnens overflade, hvilket giver hver komponent en karakteristisk retentionstid.
- Massespektrometri (MS) ioniserer de adskilte molekyler og måler forholdet mellem masse og ladning (m/z) for de dannede ioner. Resultatet er et massespektrum, der fungerer som et fingeraftryk for hvert stof.
Typisk arbejdsgang
- Prøveindsamling og -mærkning (vigtig i retsmedicin for chain of custody).
- Prøveforberedelse (ekstraktion, oprensning, eventuel derivatisering).
- Indsprøjtning i GC (direkte, headspace eller via SPME).
- Separation i GC-kolonne — detektoren (MS) modtager komponenterne enkeltvis.
- Ionisering i MS, detektion af ioner og opbygning af massespektrum.
- Dataanalyse: sammenligning af retentionstid og massespektralprofil med referencebiblioteker (fx NIST) og kvantificering ved kalibreringskurver eller interne standarder.
Prøveforberedelse
Prøveforberedelse afhænger af matrixen (luft, vand, blod, urin, jord, fødevarer). Almindelige metoder:
- Opløsning og ekstraktion (væske-væske, fast-fase ekstraktion).
- Headspace eller SPME (Solid Phase Microextraction) til flygtige og semi-flygtige forbindelser.
- Derivatisering (fx silylering) for at gøre polære eller termisk ustabile forbindelser egnede til GC.
Ionisering og detektion
- Electron Ionization (EI) er almindelig i GC-MS: hård ionisering, som giver reproducible fragmenteringsmønstre gode til identifikation.
- Chemical Ionization (CI) er blødere og bevarer ofte molekylionen, hvilket hjælper med at bestemme den molekylære vægt.
- Maskintyper: kvadrupol, iontøjle (ion trap), time-of-flight (TOF) — hver med fordele ved opløsning, følsomhed og massespektral hastighed.
- Driftsmåder: SCAN (fuldt spektrum, god til identifikation) vs. SIM (Selected Ion Monitoring — forbedret følsomhed for kendte ioner, god til kvantificering).
Identifikation og kvantificering
- Identifikation bygger på kombinationen af retentionstid og matches af massespektralprofiler mod biblioteker (fx NIST).
- Kvantificering sker ofte med kalibreringskurver og interne standarder for at korrigere for tab i prøveforberedelse og instrumentvariation.
- Grænser for detektion (LOD) og kvantificering (LOQ) afhænger af instrument, matrix og mådemetode (SCAN vs. SIM).
Anvendelser
GC-MS bruges bredt, blandt andet:
- Retsmedicin og toksikologi: narkotika, giftstoffer, dødsårsagsundersøgelser.
- Miljøanalyse: pesticider, VOC'er, forurenende stoffer i jord, vand og luft.
- Brand- og sprængstofundersøgelser: identifikation af acceleranter og sprængstofrester.
- Fødevarer og aroma: bestemmelse af smagsstoffer, forureninger og sporstoffer.
- Farmaceutisk udvikling og kvalitetssikring: analyse af råmaterialer, forurenende stoffer og rester fra syntese.
- Sikkerhedskontrol: screening for sprængstoffer og narkotika i lufthavne og andre checkpoints.
- Metabolomics og kliniske studier: profilering af små molekyler i biologiske prøver.
Fordele og begrænsninger
- Fordele:
- Høj specificitet og muligheden for positiv identifikation.
- God følsomhed ved korrekt opsætning (især i SIM-mode).
- Bredt bibliotek til sammenligning af spektra.
- Begrænsninger:
- Kun egnet til flygtige eller let volatiliserbare stoffer — ikke egnede for tunge, termisk ustabile eller meget polære forbindelser uden derivatisering.
- Matrixeffekter og co-elution kan hæmme identifikation/kvantificering.
- Kræver regelmæssig vedligeholdelse (kolonne, kilder, septa) for at undgå forurening og kolonnebleed.
Kvalitetssikring og gode praksisser
- Brug af interne standarder og kalibreringskurver for nøjagtig kvantificering.
- Validering af metoder for følsomhed, linearitet, præcision og nøjagtighed.
- Rutinemæssig rengøring og vedligeholdelse af ionkilde og kolonne for at reducere baggrundssignal og forurening.
- God prøvehåndtering og dokumentation (især i retsmedicinske anvendelser) for at sikre sporbarhed og bevare integriteten af bevismateriale.
Konklusion
GC-MS er et alsidigt og stærkt analytisk værktøj, der forener effektiv separation med detaljeret massespektrometrisk information. Dets evne til at levere både identifikation og kvantificering gør det uundværligt i mange felter — fra retsmedicin til miljøforskning og fødevaresikkerhed. For at opnå pålidelige resultater er korrekt prøveforberedelse, passende instrumentopsætning og løbende kvalitetssikring afgørende.