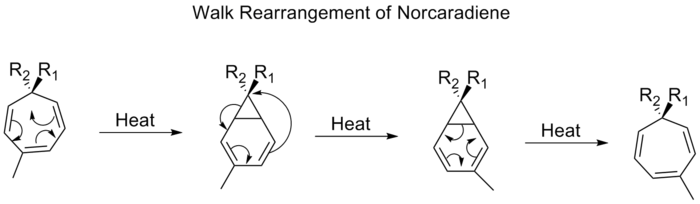
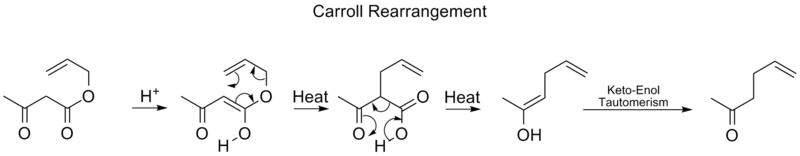
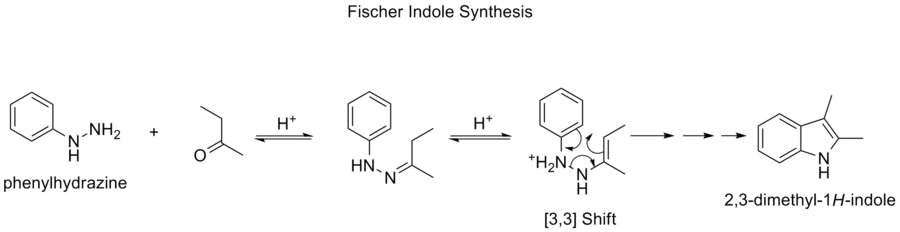
En sigmatropisk reaktion i organisk kemi er en pericyklisk reaktion. En sigmatropisk reaktion anvender ikke en katalysator og involverer et enkelt molekyle (en ikke-katalyseret intramolekylær proces). Den ændrer en σ-binding til en anden σ-binding. Navnet sigmatropisk er resultatet af en sammensætning af den længe etablerede betegnelse "sigma" for enkelte kulstof-kulstof-bindinger og det græske ord tropos, der betyder drejning. Der er tale om en omarrangeringsreaktion, hvilket betyder, at bindingerne i et molekyle forskydes mellem atomer, uden at der udgår atomer fra eller tilføjes nye atomer til molekylet. I en sigmatropisk reaktion flytter en substituent sig fra en del af et π-bundet system til en anden del i en intramolekylær reaktion med samtidig omlægning af π-systemet. Ægte sigmatropiske reaktioner kræver normalt ikke en katalysator. Nogle sigmatropiske reaktioner katalyseres af en Lewis-syre. Sigmatropiske reaktioner har ofte overgangsmetalkatalysatorer, der danner mellemprodukter i analoge reaktioner. De mest kendte af de sigmatrope omlægninger er [3,3] Cope-omlægningen, Claisen-omlægningen, Carroll-omlægningen og Fischer-indolsyntesen.
Notation og mekanistisk oversigt
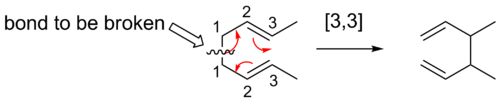
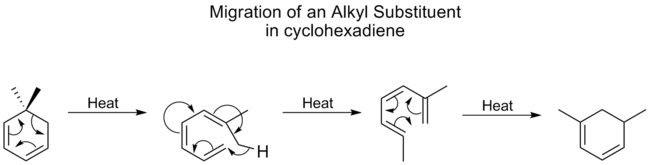
Sigmatropiske omlægninger betegnes ofte som [i,j]-reaktioner, hvor tallene i og j angiver antallet af atomer i hvert af de to π-systemer, målt fra den oprindelige σ-binding. For eksempel er en [3,3]-omlægning en process hvor σ-bondens endepunkter ender tre positioner fra hinanden i hver af de to deltagende π-systemer. Disse reaktioner er typisk pericykliske og foregår via et enkelt, concerted overgangsforløb uden frie radikaler eller ioner (medmindre en særlig variant eller katalyse indfører sådanne intermediater).
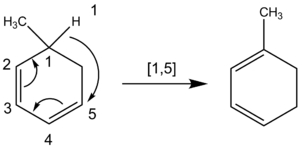
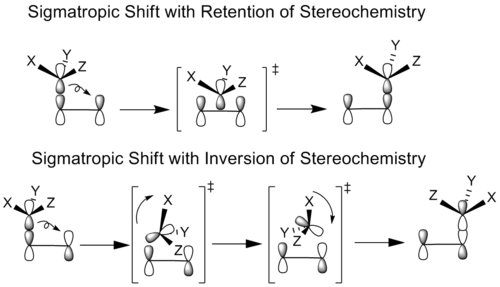
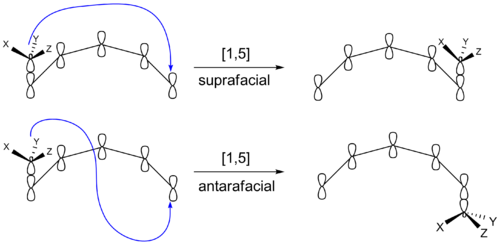
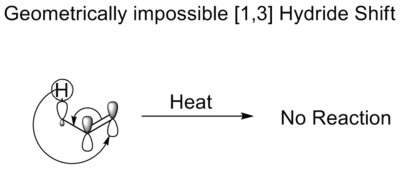
Elektronisk og stereokemisk styres sigmatropiske reaktioner af Woodward–Hoffmann-reglerne: termiske [i,j]-sigmatropiske reaktioner foregår typisk suprafacialt (samme side af π-systemet) for de almindelige lave-order tilfælde ([1,5], [3,3] osv.), mens photokemisk aktivering kan ændre den tilladte symmetri og dermed give andre stereokemiske udfald. Geometriske begrænsninger (fx ringstørrelse) kan gøre en antarafacial migrationsvej nødvendig, men sådanne veje er ofte vanskelige at gennemføre i praksis.
Cope-omlægningen (klassisk og varianter)
Cope-omlægningen er en prototypisk [3,3]-sigmatropisk omlejring af 1,5-dien-systemer. Den involverer omlejring af bindinger i et 1,5-dien til isomeriske 1,5-dien-produkter. Nogle vigtige punkter:
- Cope-omlægningen kan være degenereret, dvs. produktet er identisk med udgangsmolekylet, så reaktionen er i ligevægt.
- Substituenter påvirker termodynamikken: f.eks. gør 3,3-dialkylsubstitution (Claisen-strain relief og hyperkonjugation) ofte omlægningen termodynamisk favoriseret.
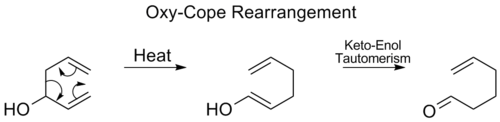
- Oxy-Cope og anionisk oxy-Cope: hvis der er en hydroxylgruppe på passende position, kan oxy-Cope-followed-by-tautomerisering give en karbonylforbindelse (en enon eller aldehyd). Den anioniske variant, hvor hydroxylgruppen først deprotoneres, sænker aktiveringsenergien markant og gør omlægningen meget mere letdreven ved milde betingelser.
- Overgangsstatetypisk er chair-lignende (lavere energi) eller boat-lignende afhængigt af substituenternes krav, hvilket bestemmer stereokemi i produktet.
Claisen-omlægningen og dens varianter
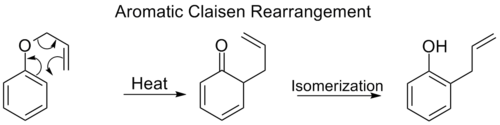
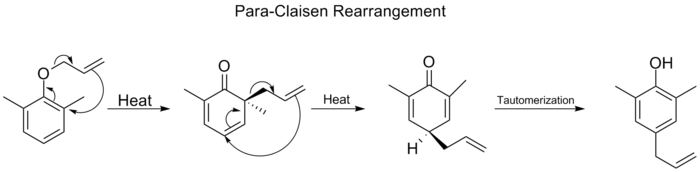
Claisen-omlægningen er også en [3,3]-sigmatropisk reaktion, klassisk for allyl-ethers (f.eks. allyl vinyl-ethers, allyl aryl-ethers). Ved en typisk Claisen-omlægning dannes en ny C–C-binding, og produkter inkluderer allylerede karbonylforbindelser eller o-allylphenoler fra allylphenyl-ethers. Nogle varianter og vigtige punkter:
- Der findes flere tilpasninger af Claisen: Ireland–Claisen (gennem ester-enolat intermediater), Johnson–Claisen (alkoksycarbonyl varianter), Eschenmoser–Claisen (iminium-baserede varianter) osv., som udvider anvendeligheden under mildere betingelser eller med kontrol over stereokemi.
- Claisen-omlægningen er nyttig i syntese for at flytte allylgrupper og bygge op konjugerede systemer og funktionaliserede carbonylforbindelser.
- Ligesom for Cope spiller overgangsstatets geometri (chair vs. boat) og substituenternes placering en afgørende rolle for stereokemien i produktet.
Stereokemi og Woodward–Hoffmann-reglerne
Woodward–Hoffmann-symmetrireglerne for pericykliske reaktioner forklarer, hvilke sigmatropiske omlægninger der er tilladte under termiske forhold og hvilke der kræver fotonisk aktivering. For de almindelige [3,3]-omlægninger betyder det:
- Termisk [3,3] → suprafacial-suprafacial overførsel af elektronpar er symmetry-allowed, hvilket sikrer en koncerted proces med bevarelse af stereokemi (kopler cis/trans-forhold i substrat til produkt på en forudsigelig måde).
- Fotokemisk aktivering kan tillade alternativer, fx antarafacial komponenter, men ofte med ændret stereokemisk udfald.
Katalyse, metalkomplekser og påvirkning af reaktionsbetingelser
Selvom mange sigmatropiske reaktioner er termisk drevne uden katalysator, kan både Lewis-syre-katalyse og overgangsmetalkomplekser ændre barriererne eller føre til alternative mekanismer:
- Lewis-syrer kan koordinere til funktionen (fx oxygen) og stabilisere overgangstilstanden, sænke aktiveringsenergien og gøre reaktionen mulig ved lavere temperatur.
- Overgangsmetaller kan interagere med π-systemer og danne π-allyl-intermediater, som effektivt ændrer reaktionsforløbet fra en concerted pericyklisk proces til en stepwise mekanisme — det kan være ønsket for at opnå andre selektiviteter.
- Anioniske varianter (fx anionisk oxy-Cope) initieres ved base-deprotonering og giver ofte dramatisk lavere aktiveringsenergi og hurtigere omlejring.
Anvendelser og praktiske eksempler
Sigmatropiske omlejninger anvendes bredt i organisk syntese:
- Cope og oxy-Cope-omlægninger anvendes til konstruktion af cykliske skeletoner og til at omarrangere konjugerede systemer. Den anioniske oxy-Cope bruges ofte til at frembringe en stabiliseret enolanion, der efterfølgende tautomeriserer til en karbonylforbindelse.
- Claisen-omlægningen er et standardværktøj til at installere allylgrupper ortho til aromatiske oxygen-funktioner (f.eks. allylering af fenoler) eller til opbygning af konjugerede carbonylsystemer; Ireland–Claisen er populær til stereokontrolleret dannelse af γ,δ-umættede carbonylforbindelser.
- Hvor pericykliske reaktioner generelt er stereospecifikke, bruges de ofte i totalsyntese af naturlige produkter for at sikre stereokemisk renhed.
Termodynamik, kinetik og praktiske hensyn
Om en sigmatropisk omlejring går til produkt afhænger af både termodynamik og kinetik. Mange Cope-omlægninger er reversible og kræver termodynamiske faktorer (substituent-effekter, forløsning af ringspænding, efterfølgende tautomerisering) for at fortrænge ligevægten mod produktet. Reaktionsbetingelserne — temperatur, opløsningsmiddel, tilstedeværelse af base eller Lewis-syre — afgør ofte, hvilken variant (termisk, fotokemisk, anionisk eller metalassisteret) man vælger i praktisk syntese.
Kort résumé
Sigmatropiske reaktioner er en central klasse af pericykliske omlejringer i organisk kemi, karakteriseret ved intramolekylær migration af en σ-binding i forbindelse med omlægning af et π-system. De mest anvendte eksempler er [3,3]-omlægninger som Cope og Claisen, som giver kraftfulde og stereospecifikke værktøjer i organisk syntese. Forståelse af pericyklisk mekanisme, Woodward–Hoffmann-symmetri og effekten af substituenter og katalysatorer er afgørende for at kunne udnytte disse reaktioner effektivt.

![[1,3] Alkyl Shifts](https://www.alegsaonline.com/image/550px-1,3alkylfixed.png)
![[1,5] Hydride shift in a cyclic system](https://www.alegsaonline.com/image/300px-1,5hydridecyclicfixed.png)
![Antarafacial [1,5] Hydride Shift](https://www.alegsaonline.com/image/600px-1,5hantarafacialfixed.png)


![[5,5] shift of phenyl pentadienyl ether](https://www.alegsaonline.com/image/800px-5,5shiftfixeds.png)