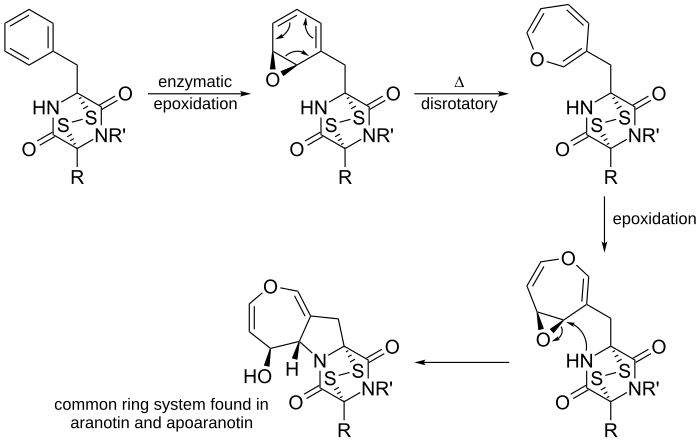
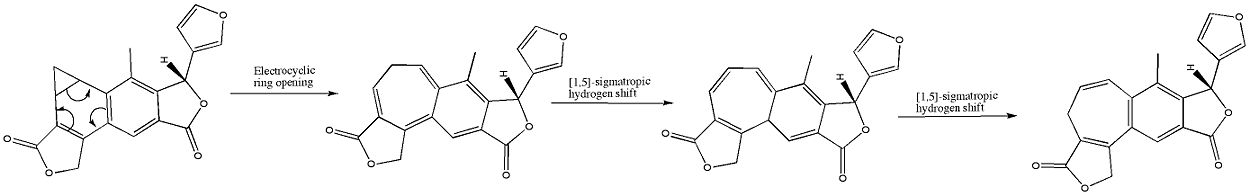
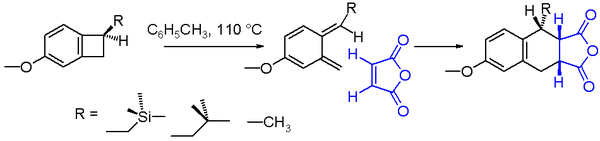
I organisk kemi er en elektrocyklisk reaktion en type pericyklisk omlægningsreaktion. Reaktionen er elektrocyklisk, hvis resultatet er, at en pi-binding bliver til en sigma-binding eller en sigma-binding bliver til en pi-binding. Elektrocykliske reaktioner kendetegnes ved samtidig dannelse eller brydning af en række bindinger i en cyklisk, sammenhængende overgangstilstand, uden at der dannes frie radikaler eller ioner som hovedtrin. Disse reaktioner er stereospecifikke og følger regler for bevarelse af molekylorbitalernes symmetri.
- elektrocykliske reaktioner drives af lys (fotoinduceret) eller varme (termisk)
- reaktionsmåden bestemmes af antallet af pi-elektroner i den del, der har flest pi-bindinger
- en elektrocyklisk reaktion kan lukke en ring (elektrocyklisering) eller åbne en ring
- stereospecifiteten bestemmes af en konrotatorisk eller disrotatorisk overgangstilstandsdannelse som forudsagt af Woodward-Hoffmann-reglerne.
Mekanisme og orbital-synkronisering
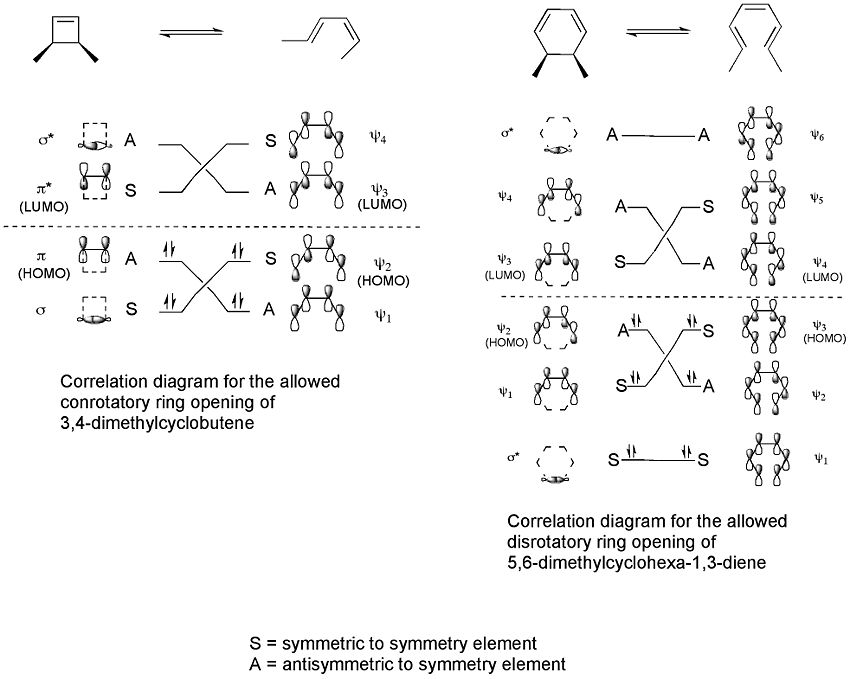
Den enkle måde at forudsige, hvilken rotationsmode (konrotatorisk eller disrotatorisk) en elektrocyklisk reaktion følger, er via Woodward–Hoffmann-reglerne, som bygger på bevarelse af molekylorbitalernes symmetri under reaktionen. Kort sagt:
- Termisk: systemer med 4n pi-elektroner (n = 1, 2, ...) går typisk via konrotatorisk overgangstilstand; systemer med 4n+2 pi-elektroner går via disrotatorisk.
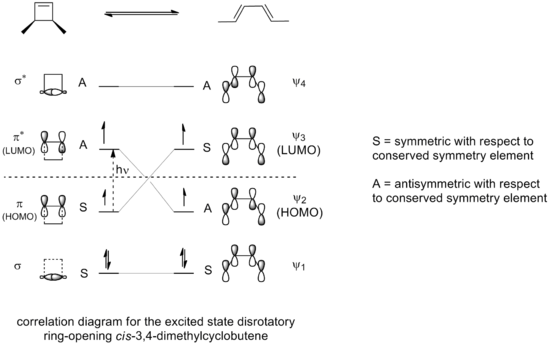
- Fotokemisk: reglen omvendes — 4n systemer følger disrotatorisk og 4n+2 systemer følger konrotatorisk.
Denne opførsel kan forklares ved grænse-orbitalmetoden (frontier molecular orbital, FMO): reaktionens stereokemi bestemmes af symmetrien af den højest besatte molekylære orbital (HOMO) i det relevante elektroniske tilstand (grundtilstand for termiske reaktioner, eksiteret tilstand for fotokemiske). Overgangstilstanden dannes på en måde, så de nye eller brudte p-orbitaler kan matche fasen i HOMO og dermed give en stabil, bindingsdannende interaktion.
Woodward–Hoffmann-reglerne og korrelation
Woodward-Hoffmann-reglerne er en formel måde at udlede de ovennævnte tendenser på ved at bruge korrelationsdiagrammer eller ved at anvende begrebet Hückel- og Möbius-type overgangstilstandaromaticitet. Reglerne opsummerer, at orbitaliære symmetrier bevares gennem en kontinuert, pericyklisk omlejring — hvis en bevarende korrelation kræver en ændring i fase, vil den proces være symmetrisk forbudt eller have høj aktiveringsenergi og vil derfor ikke observeres under de givne forhold.
Torquoselektivitet
Torquoselektiviteten i en elektrocyklisk reaktion henviser til den retning, som substituenterne roterer. F.eks. kan substituenterne i en reaktion, der er konrotatorisk, stadig rotere i to retninger. Det giver en blanding af to produkter, der er spejlbilledet af hinanden (enantiomeriske produkter). En reaktion, der er torquoselektiv, begrænser en af disse rotationsretninger (delvist eller fuldstændigt) for at fremstille et produkt i enantiomeroverskud (hvor den ene stereoisomer fremstilles i langt højere grad end den anden).
Torquoselektivitet påvirkes af substituenternes elektroniske egenskaber, steriske krav, tilstedeværelse af koordinerende metaller eller syrer og sekundære orbitalinteraktioner. I praksis bruges chirale auxiliærer, asymmetriske katalysatorer eller strategisk placering af elektrondonor-/acceptor-grupper til at styre torquoen og opnå høj enantioselektivitet.
Eksempler og eksperimentelt bevis
Kemikere er interesserede i elektrocykliske reaktioner, fordi molekylernes geometri bekræfter en række forudsigelser, som teoretiske kemikere har lavet. De bekræfter bevarelsen af den molekylære orbitalsymmetri, og eksperimenter med stereospecifikke substrater giver ofte entydige resultater, der matcher Woodward–Hoffmann-forudsigelserne.
Nazarov-cykliseringsreaktionen er en elektrocyklisk reaktion, der lukker en ring. Den omdanner divinylketoner til cyclopentenoner. (Den blev opdaget af Ivan Nikolaevich Nazarov (1906-1957).) Typisk aktiveres Nazarov-cykliseringen under sure forhold eller ved Lewis-syrer, som fremmer dannelsen af en elektron-underskudende mellemtilstand og dermed faciliterer den konrotatoriske 4π-elektrocyklisering, som leder til cyclopentenonproduktet.
Et klassisk og illustrativt eksempel er den termiske ringåbningsreaktion af 3,4-dimethylcyclobuten. Cis-isomeren giver kun cis,trans-2,4-hexadien. Men trans-isomeren giver trans,trans-dien:
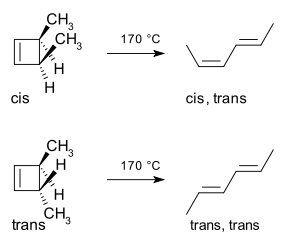
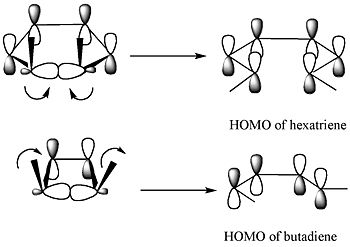
Grænse-orbitalmetoden forklarer, hvordan denne reaktion fungerer. Sigma-bindingen i reaktanten åbnes på en sådan måde, at de resulterende p-orbitaler har samme symmetri som den højest besatte molekylære orbital (HOMO) i produktet (et butadien). Dette kan kun ske ved en konrotatorisk ringåbning, der resulterer i modsat fortegn for de to lober i de knækkede ender af ringen. (En disrotatorisk ringåbning ville danne en antibinding.) Følgende diagram viser dette:
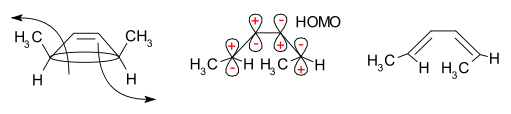
Resultatets stereospecificitet afhænger af, om reaktionen foregår gennem en konrotatorisk eller disrotatorisk proces. I mange tilfælde kan man forudsige produktets relative konfiguration direkte fra reaktionsmoden uden at kende alle detaljer om overgangstilstanden, fordi orbitalfasen dikterer rotationen.
Anvendelse i syntese
Elektrocykliske reaktioner bruges hyppigt i syntetisk organisk kemi til opbygning af cykliske strukturer med veldefineret stereokemi, især når hurtig ringdannelse eller ringomlejring ønskes. Kombinationer af elektrocykliske trin med andre pericykliske reaktioner (f.eks. Diels–Alder) er almindelige i totalsyntese af komplekse naturlige produkter. Kontrol af torquoselektivitet og anvendelse af fotokemiske forhold udvider desuden værktøjskassen for selektiv syntese.
Opsummering
- Elektrocykliske reaktioner er pericykliske omlægninger, der omdanner pi- til sigma-bindinger eller omvendt.
- Termisk vs. fotokemisk aktivering ændrer den tilladte rotationsmode (konrotatorisk vs. disrotatorisk) afhængigt af antallet af pi-elektroner (4n vs. 4n+2) som forudsagt af Woodward-Hoffmann-reglerne.
- Torquoselektivitet og substituenteffekter kan give høj stereokontrol og er vigtige i syntetisk anvendelse.
- Eksempler som dimethylcyclobutene og Nazarov-cykliseringen illustrerer principperne i praksis.