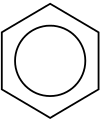
Et aromatisk kulbrinte eller aren er en kulbrinteforbindelse med en ringformet kulbrinte. Den har skiftevis dobbelt- og enkeltbindinger mellem kulstofatomer, der danner ringe. Mange af forbindelserne har en sødlig duft, deraf betegnelsen "aromatisk". Ringen af seks kulstofatomer i aromatiske forbindelser kaldes en benzenring, efter den enkleste mulige kulbrinte ring, benzen. Aromatiske carbonhydrider kan være monocykliske (MAH) eller polycykliske (PAH).
Nogle ikke-benzenbaserede forbindelser, kaldet heteroarener, som følger Hückels regel, er også aromatiske forbindelser. I disse forbindelser er mindst ét kulstofatom erstattet af et af oxygen, nitrogen eller svovl.
Struktur og aromatiske kriterier
Aromatiske forbindelser kendetegnes ved:
- Cyklicitet: atomerne danner en lukket ring.
- Planaritet: ringens atomer ligger i ét plan, så π-orbitaler kan overlappe.
- Konjugation: et uhindret system af overlappende π-orbitaler (skiftevis enkelt- og dobbeltbindinger eller delokaliserede elektroner).
- Hückels regel: ringens π-elektronsystem indeholder (4n + 2) π-elektroner (n = 0, 1, 2 …), hvilket giver særlig stabilitet.
Et klassisk eksempel er benzen (C6H6). I stedet for faste enkelt- og dobbeltbindinger beskrives benzen ofte ved resonans eller som et delokaliseret π-system med lige lange C–C-bindinger og en markant aromatisk stabilisering.
Elektronfordeling og reaktivitet
Aromatiske systemer indeholder delokaliserede π-elektroner, som gør dem kemisk mere stabile end tilsvarende ikke-aromatiske alifatiske forbindelser. Derfor foretrækker aromater ofte substitution frem for addition; i stedet for at bryde aromatiskitet ved additioner, gennemgår de typisk elektrofil aromatisk substitution (EAS) såsom:
- nitrering (introduktion af –NO2)
- sulfonering (introduktion af –SO3H)
- halogenering (Cl, Br)
- Friedel–Crafts alkylation og acylering
Disse reaktioner bevarer ringens aromatiske stabilitet ved at erstatte et hydrogenatom i ringen med en substituent.
Typer og eksempler
- Monocykliske aromater (MAH): f.eks. benzen, toluen (methylbenzen) og xylen – en enkelt benzenring med forskellige substituenter.
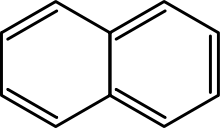
- Polycykliske aromatiske hydrocarboner (PAH): f.eks. naphthalen (to sammenkoblede benzenringe), anthracen og phenantren. PAH dannes ofte ved ufuldstændig forbrænding af organiske materialer.
- Heteroarener: aromatiske ringe hvor mindst ét atom er ikke-kulstof, f.eks. pyridin (N), pyrrol (N), furan (O) og thiophen (S). Disse følger også Hückels regel, men deres kemiske egenskaber kan variere kraftigt pga. heteroatomets elektroniske indflydelse.
Fysiske og spektroskopiske kendetegn
- Aromatiske hydrogenatomer giver karakteristiske signaler i 1H-NMR typisk i området ca. 6,5–8,5 ppm (afhænger af substituenter).
- IR-spektre viser aromatiske C–H-strækninger tæt på 3000 cm−1 og C=C-absorptionsbånd omkring 1600 cm−1.
- PAH viser ofte karakteristiske UV/Vis-absorptioner pga. udstrakte konjugerede π-systemer.
Anvendelser
- Aromatiske forbindelser bruges som råmaterialer i organisk syntese til fremstilling af farmaceutika, farvestoffer, polymerer og kemiske mellemprodukter.
- Toluen og xylen anvendes som industrielle opløsningsmidler.
- PAH er vigtige i studiet af forbrændingsprocesser, materialeforskning og astro-kemi (PAH er fundet i interstellare medier).
Sundhed og miljø
Mange PAH er miljøpersistente og kan være giftige, mutagene eller kræftfremkaldende (f.eks. benzo[a]pyren). PAH dannes ved ufuldstændig forbrænding (f.eks. i biludstødning, tobaksrøg og grillmad) og akkumuleres i jord og sedimenter. Derfor er overvågning og reduktion af PAH-emissioner vigtig for folkesundhed og miljøbeskyttelse.
Analyse og identifikation
Typiske analytiske metoder til at identificere og kvantificere aromatiske forbindelser:
- GC-MS (gaschromatografi-massespektrometri) til flygtige og halvflygtige aromater.
- HPLC (væskekromatografi) til tungere eller polære derivater.
- NMR og IR til strukturbestemmelse.
Samlet set er aromatiske kulbrinter en central gruppe i organisk kemi med særlige elektroniske egenskaber, bred anvendelse i industrien og samtidig betydelige miljø- og sundhedsmæssige implikationer.