Phenol: Struktur, egenskaber, fremstilling og anvendelser
Lær om phenol: struktur, egenskaber, fremstilling og anvendelser i industri, rengøringsmidler og herbicider. Få en klar, faglig gennemgang af kemiske egenskaber og produktion.
Phenol er en organisk forbindelse med formlen C6H5OH. Det er et hvide til farveløst fast stof ved stuetemperatur med en karakteristisk skarp, svagt sødlig lugt. Molekylet består af en hydroxylgruppe (OH) bundet direkte til en benzenring. Som en type alkohol adskiller phenol sig fra alifatiske alkoholer ved, at den aromatiske ring påvirker OH-gruppens kemiske egenskaber: den elektroner-tiltrækkende og -delokaliserende effekt giver phenoxidet (den deprotonerede form) særlig stabilitet, hvorfor phenol er relativt sur sammenlignet med almindelige alkoholer. Industrielt fremstilles phenol hovedsageligt fra råstoffer fra olie via de såkaldte cumene-processer og andre metoder. Det er et vigtigt molekyle, fordi det indgår som byggesten i mange kemiske produkter; det anvendes også som råvare til rengøringsmidler, herbicider og i produktion af farvestoffer, plast og medicin.
Struktur og grundlæggende egenskaber
- Formel: C6H5OH.
- Fysisk form: Krystallinsk fast stof ved lavere temperaturer; smeltepunkt ca. 40,5 °C og kogepunkt ca. 181,7 °C.
- Syrebaseegenskaber: pKa ≈ 9,9–10,0, hvilket gør phenol betydeligt mere surt end alifatiske alkoholer på grund af resonansstabilisering af phenoxid-anionen.
- Opløselighed og bindinger: Phenol kan danne hydrogenbindinger og er moderat opløseligt i vand; det opløses godt i mange organiske opløsningsmidler.
- Reaktivitet: Hydroxylgruppen aktiverer ringens positioner o- og p- (ortho- og para-) for elektrofiler, så aromatic substitutionsreaktioner ofte sker i disse positioner.
Vigtige kemiske reaktioner
- Deprotonering: Phenol reagerer med stærke baser (fx NaOH) og danner vandopløselige fenoxider/phenolater.
- Elektrofil aromatisk substitution: Nitrering, halogenering og sulfonering foregår primært i ortho- og para-positionerne i forhold til OH-gruppen.
- Kondensations- og substitutionsreaktioner: Phenoler kan indgå i dannelse af ethers og estere samt videre omdannelse til komplekse byggesten som bisphenol A.
- Oxidation: Phenoler kan oxideres til quinoner og andre oxygenholdige aromatiske forbindelser.
Fremstilling
Historisk blev phenol udvundet fra trækulstjære (coal tar). I dag fremstilles phenol industrimæssigt primært ved:
- Cumene-processen: Benzen alkylieres med propylengas til cumen, som oxideres til cumylhydroperoxid og derefter spaltes til phenol og acetone. Denne metode er den mest udbredte industrielt.
- Andre metoder omfatter direkte hydroxylation af benzen og processer baseret på klorering og efterfølgende hydrolyse i nogle specialtilfælde.
Anvendelser
Phenol er en central råvare i kemisk industri og bruges til mange formål, for eksempel:
- Produktion af fenol-formaldehyd-harpiks (fx Bakelit) til beklædninger, limer og kompositmaterialer.
- Syntese af bisphenol A, som er udgangsstoffet til polycarbonater og visse epoxyharpikser.
- Fremstilling af salicylsyre (via Kolbe–Schmitt-reaktionen), en forløber for acetylsalicylsyre (aspirin) og andre lægemidler.
- Brug som antiseptisk stof og desinfektionsmiddel historisk (karbolsyre) og i visse industrielle desinfektionsmidler.
- Råvare til fremstilling af farvestoffer, additiver, overfladeaktive stoffer, og visse plantebeskyttelsesmidler (herbicider).
Sikkerhed og miljø
- Toksicitet: Phenol er ætsende og kan forårsage alvorlige kemiske brandsår ved kontakt med hud og slimhinder. Optagelse gennem huden kan give systemisk toksicitet med påvirkning af centralnervesystemet, leveren og nyrerne.
- Håndtering: Brug altid passende værnemidler (handsker, øjenbeskyttelse, åndedrætsværn ved dampe) og arbejd i godt ventilerede rum. I industrien anvendes lukkede systemer for at minimere eksponering.
- Miljø: Phenol er giftig for vandlevende organismer. Spild skal forebygges og håndteres efter gældende regler for farligt affald og forureningsbekæmpelse.
- Førstehjælp: Fjern forurenet tøj, skyl hud og øjne grundigt med vand og søg lægehjælp straks ved alvorlig eksponering.
Historiske noter
Phenol blev tidligere kaldt karbolsyre og fik tidligt betydning inden for antiseptisk behandling efter Joseph Lister demonstrerede dens evne til at reducere sårinfektioner i slutningen af 1800-tallet. I moderne tid er brugen som antiseptisk stof dog reduceret til fordel for mindre toksiske alternativer.
Samlet set er phenol et almen anvendt og kemisk vigtigt stof med både nyttige industrielle anvendelser og væsentlige sikkerheds- og miljøhensyn. Ved arbejde med phenol er korrekt håndtering og overholdelse af sikkerhedsprocedurer afgørende.
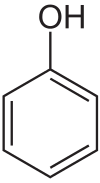
Phenols struktur
Egenskaber
Surhedsgrad
Phenol har en pKa på ca. 10. For normale alkoholer er dette tal normalt omkring 15. Phenol er dog mindre surt end forbindelser som carboxylsyrer. Årsagen til denne høje surhedsgrad er molekylets resonansstabilisering, når det bliver til en anion.
Reaktioner
Phenol kan udføre elektrofile aromatiske substitutionsreaktioner meget godt. Det skyldes, at det ensomme par på oxygenatomet kan afgive elektroner gennem benzenringen til en elektrofil. Fordi loneparret har så høj energi, reagerer phenol imidlertid nogle gange for mange gange.
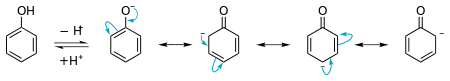
Et diagram, der viser stabiliseringen af det ensomme par på oxygen i phenol. Dette forklarer syreniveauet.
Historie
Phenol blev først opdaget i 1834. Det blev fundet som et produkt fra forbrænding af kul. En af de første anvendelser var til at dræbe bakterier i kirurgi. Det bruges stadig i dag i visse smertestillende midler. Under Anden Verdenskrig blev phenol også brugt af nazisterne. De brugte det i koncentrationslejre til hurtigt at dræbe små grupper af mennesker.
Søge