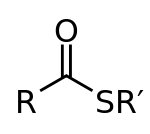
En thioester er et molekyle hvor en carboxylgruppe er bundet til et svovlatom i stedet for et oxygen, typisk skrevet som R-C(=O)-S-R'. Den simple beskrivelse C-S-CO-C fra folkeudgaven svarer til dette: thioestere ligner estere, men har et oxygenatom udskiftet med et svovlatom. De dannes på tilsvarende måde som estere fra carboxylsyrer, men i syntesen anvendes en thiol i stedet for en alkohol.
Struktur og kemiske egenskaber
Forskellen i atomtype (sulfur i stedet for oxygen) giver thioestere særlige kemiske egenskaber:
- Mindre resonansstabilisering: Sulfur overlapper svagere med carbonylets π-system end oxygen. Det betyder, at karbonyl-carbonen er mere elektrofil (modtagelig for nukleofile angreb) end i tilsvarende estere og amider.
- Højere reaktivitet: Thioestere er generelt mere reaktive over for nukleofil acylsubstitution (acyloverførsel) end estere, hvilket gør dem til gode "aktiverede" acylbærere.
- Energi ved hydrolyse: Hydrolyse af thioestere frigiver ofte mere fri energi end hydrolyse af oksyestere — derfor omtales de somme tider som "højt energibånd" i biologiske systemer.
- Alpha-hydrogener og enolat-dannelse: Thioestere har ofte lettere afgivelige α-hydrogener (større aciditet) og danner enolater/enolater-lignende intermediat nemmere, hvilket er nyttigt i C–C-bindingsdannende reaktioner og biosyntetiske kondensationssteg.
Syntese og reaktioner i laboratoriet
Kemisk kan thioestere fremstilles ved flere metoder, fx ved aktivering af en carboxylsyre (som acid chloride eller via en koblingsreagens som DCC/EDC) efterfulgt af reaktion med en thiol, eller ved omdannelse af syrederivater direkte til thioestere. I organisk syntese bruges thioestere ofte som effektive elektrofiler i acyloverførsler, og de kan indgå i kondensationsreaktioner (fx Claisen-typen) og i aldolreaktioner under de rette betingelser.
Biokemisk rolle — "aktiverede" acylgrupper
Thioestere er centrale i biokemi. De optræder i mange metaboliske processer som aktiverede former af fedtsyrer og andre acylgrupper. De mest kendte biothioestere er derivater af coenzym A (CoA): acyl‑CoA-forbindelser (fx acetyl‑CoA, palmitoyl‑CoA) og acylgrupper bundet til acyl carrier protein (ACP) i fedtsyresyntesen.
- Fedtsyresyntese og -nedbrydning: I syntesen bliver acylgrupper båret som thioestere på ACP eller CoA; i beta-oxidationen er fedtsyrer aktiveret som acyl‑CoA før degradering. Disse thioesterbindinger muliggør effektive enolatformeringer og kondensationstrin.
- ATP-produktion og energioverførsel: Thioestere optræder også som vigtige mellemprodukter i centrale energihintinger. Eksempelvis frigiver omdannelsen af succinyl‑CoA til succinat (via succinyl‑CoA synthetase) den energi, der bruges til at lave GTP eller ATP ved substrat‑niveau‑fosforylering i citratcyklus. Desuden er dannelsen af acetyl‑CoA et centralt trin, der fører til dannelse af reducerede cofaktorer (NADH, FADH2), som siden bruges til at danne ATP i oxidative fosforylering.
- Aktiv acyloverførsel: Thioestere fungerer som gode acyldonorer i enzymkatalyserede transthiolerings- og acyltransferreaktioner — de er derved essentielle i mange biosyntetiske og kataboliske veje.
Eksempler og anvendelser
Eksempler på vigtige thioestere i levende organismer:
- Acetyl‑CoA: Central metabolit ved kulhydrat-, fedt- og proteinmetabolisme og starterreaktant i citratcyklus.
- Malonyl‑ACP og acetyl‑ACP: Nøgleintermediater i fedtsyresyntesen, hvor thioesterbindingen til ACP muliggør gentagne forlængelsestrin.
- Succinyl‑CoA: Deltager i citratcyklus og i syntese af porfyriner og visse aminosyrer; omdannelsen til succinat kobler sig til ATP/GTP-dannelse.
I organisk kemi og peptidsyntese bruges thioestere også praktisk: de kan fungere som gode acylbærere i tværkoblingsreaktioner, i native chemical ligation ved peptidsyntese og i syntetiske strategier, hvor høj acylativitet er ønskelig.
Opsummering
Thioestere er R‑C(=O)‑S‑R' forbindelser, der på grund af sulfurens egenskaber er mindre resonansstabiliserede og dermed mere reaktive end tilsvarende estere og amider. Denne øgede reaktivitet gør dem uundværlige som biologiske "aktiverede" acylformer i biokemi — især i forbindelse med reaktioner der danner fedtsyrer og i processer, der indirekte eller direkte bidrager til kroppens energi (ATP). Kemisk bruges de også som kraftige elektrofiler og reaktive intermediater i organisk syntese, fx ved aldolreaktioner og andre C–C‑dannende trin.