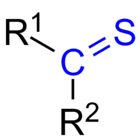
En thioketon (eller thion) er ethvert molekyle med gruppen R2 C=S. Det svarer til en almindelig keton, hvor oxygenatomet er udskiftet med et svovlatom. Svovlatomet er bundet til kulstof med en dobbeltbinding og bærer desuden to ensomme par. Kulstofatomet i C=S er typisk sp2-hybridiseret og ligger i et næsten planært miljø, mens C=S-båndet normalt er længere og har en anden elektronisk karakter end C=O.
Struktur og elektronisk karakter
Hvor en carbonylgruppe (C=O) bygger på et godt overlap mellem 2p-orbitaler, involverer C=S 3p-orbitaler fra svovl. Det giver dårligere pπ–pπ-overlap, hvilket påvirker både båndstyrke og elektronfordeling. Som følge heraf har thioketoner ofte:
- et længere og generelt svagere dobbeltbinding end tilsvarende ketoner,
- en lavere energimæssig π*-orbital, hvilket gør kulstofsitet mere elektrofil (delvist positivt) og dermed mere modtageligt for nukleofile angreb,
- markante n→π* elektronovergange fra svovls ensomme par, som ofte medfører stærkere farvning (farvede forbindelser) end tilsvarende ketoner.
Fremstilling
Den mest almindelige vej til at lave en thioketon er ved at omdanne en carbonylforbindelse (keton eller aldehyd) ved hjælp af thioneringsreagenser, fx Lawesson’s reagent eller P4S10. Disse reagenser udskifter oxygenet med svovl og giver R2C=S som produkt. Enkelte thioketoner fremstilles også direkte ved kondensations- eller substitutionsreaktioner afhængigt af den ønskede substitutionsmønster.
Reaktivitet
Generelt er thioketoner mere reaktive end deres oxygen-analoger. De opfører sig som gode elektrofiler, fordi kulstofsitet i C=S er let modtageligt for nukleofile angreb. Typiske reaktioner omfatter:
- Nukleofil addition til kulstofet i C=S, som kan give tilsvarende additionsprodukter eller efterfølgende omlejring.
- Cycloadditionsreaktioner — mange thioketoner danner ringe ved [4+2]- eller [3+2]-type cycloadditioner. Disse reaktioner ligner ofte Diels–Alder-reaktionen eller 1,3-dipol-cycloadditioner, hvor C=S fungerer som dienofil eller elektrofil komponent.
- Photokemiske og radikalbaserede processer kan give specielle additionsprodukter (fx thiiraner ved passende betingelser), men reaktionsforløbet afhænger stærkt af substratets struktur.
Stabilitet og undtagelser
Mange enkle thioketoner er ustabile eller polymeriserer let; det skyldes stærk reaktivitet ved C=S. Stabilitet kan øges ved:
- sterisk hindring (store, voluminøse substituenter),
- konjugation med aromatiske systemer, som delokaliserer ladning og sænker reaktiviteten,
- individuelle eksempler på relativt stabile thioketoner findes — et velkendt eksempel er thiobenzophenone (diphenylthioketone), som er farvet og isolerbar under almindelige forhold.
Modsat er en thial (R–CH=S), altså når en af R-grupperne er hydrogen, endnu mere reaktiv end thioketoner og polymeriserer eller reagerer ofte umiddelbart.
Spektroskopiske træk og praktiske bemærkninger
Thioketoner viser karakteristiske spektroskopiske træk: C=S-området i IR ligger forskelligt fra carbonylområdet, og elektroniske absorptioner (UV–vis) kan give synlige farver på grund af n→π*-overgange. I praksis har mange thioketoner skarpe lugte, og nogle (fx thioacetone) er berygtet for ubehagelige og stærke odører. Håndtering bør derfor ske i aftræk og med passende værnemidler.
Anvendelser
På trods af udfordringer med stabilitet bruges thioketoner som byggesten i syntetisk kemi til at indføre svovlfunktionalitet, som intermediater i opbygning af svovlholdige heterocykliske systemer, og i studier af reaktionsmekanismer hvor den særlige elektronik af C=S udnyttes.
Opsummerende: Thioketoner (R2C=S) er svovl-analoger til ketoner med en karakteristisk elektronisk struktur, høj reaktivitet og rig kemi, men deres praktiske brug kræver ofte særlige forhold på grund af ustabilitet og lugtgener.