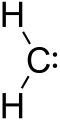Et carbene er et molekyle med et kulstofatom, der har to bindinger, og to andre elektroner, der ikke danner nogen bindinger. Da kulstoffet kun har 6 elektroner omkring sig, er det ret reaktivt. Den generelle formel kan skrives som R-(C:)-R'.
Elektronstruktur og elektronkonfiguration
Carbenens centrale kulstof har i princippet kun seks valenselektroner. De to ikke-bindende elektroner kan enten være parvis i én orbital (et singlet) eller fordelt i to forskellige orbitaler med parallelle spind (et triplet). I singlettilstanden optræder de to elektroner som et ensomt par og befinder sig typisk i samme orbital. I et tripletcarbene er elektronerne i forskellige orbitaler og har begge det samme spin, hvilket gør systemet biradikalt i karakter.
Singlet vs. triplet
Overgangen mellem singlet og triplet afhænger af substituenterne på carbene og deres evne til at stabilisere den tomme orbital eller det frie elektronpar. Substituenter, der kan delokalisere eller donere elektroner (fx heteroatomers frie elektronpar i N-heterocykliske carbenes), stabiliserer ofte singlet-tilstanden. Alkylgrupper og mindre elektron-donerende grupper favoriserer ofte triplet-tilstanden gennem hyperkonstribution og mindsket elektronparstabilisering. Eksperimentelt kan man sondre mellem dem med spektroskopiske metoder (f.eks. EPR for tripletter) eller ved reaktionsmønstre, da singlet- og tripletcarbener ofte reagerer forskelligt.
Typer af carbener
- Frie carbener: meget kortlivede mellemprodukter som methylen (:CH2) og dichlorocarbene (:CCl2).
- Persistente og stabile carbener: nogle carbenarter kan isoleres og opbevares, særligt N-heterocykliske carbenes (NHC), som er singlet og bruges meget som ligander i katalyse.
- Metal-carbenes (alkylidener): carben-lignende enheder bundet til metaller. Disse er centrale i mange katalytiske processer, f.eks. i olefinmetatese; et velkendt industriel relevant system er Grubbs' katalysator, som indeholder en ruthenium–alkylidene-komponent.
- Fischer- vs. Schrock-carbenes: to begreber for metal-carbenes: Fischer-carbenes er ofte bundet til lav-oksidationstilstandsmetaller og er elektronsøgende (elektrofile), mens Schrock-carbenes optræder ved højere metalliske oxidationstilstande og er mere nukleofile.
Fremstilling af carbener
Carbener dannes typisk som reaktive mellemprodukter ved forskellige procedurer, fx:
- Termisk eller fotokemisk spaltning af forstadier (f.eks. ved spaltning af diazoforbindelser - udsendelse af N2 giver carben).
- α-Eliminationer, hvor et halogen og et hydrogen fjernes fra et methylencenter (fx fremstilling af dichlorocarbene fra chloroform + base).
- Metalmedierede processer, hvor et metalkompleks dekomponerer en diazoforbindelse og leverer et metal–carbene.
Reaktivitet og typiske reaktioner
Carbener er meget reaktive og kan optræde både som elektrofil og nukleofil afhængigt af deres art (og af, om de er frie eller metal-bundne). Typiske reaktioner omfatter:
- Additionsreaktioner på dobbeltbindinger, hvilket ofte fører til cyclopropananer (cyklopropanering).
- Indsættelse i sigma-bindinger, fx C–H indsættelse, som kan skabe nye C–C- eller C–X-bindinger.
- Ylide- og betaine-dannelse ved reaktion med nukleofiler som fosfiner eller sulfider.
- Cheletropiske reaktioner, hvor et carbene addereer til konjugerede systemer eller diener — carbener optræder også i cheletropiske reaktioner.
Nogle carben-agtige reagenser (carbenoider), fx i Simmons–Smith-reaktionen, bruges til selektiv cyclopropanisering uden at have et "frit" carbene som isolerbart mellemprodukt.
Stabilisering, anvendelser og eksempler
De fleste carbener er meget ustabile og kortelevende. Nogle carben-typer kan dog eksistere i lang tid under de rette betingelser: særligt sterisk beskyttede eller elektronisk stabiliserede carbenes (fx N-heterocykliske carbenes) kan isoleres og bruges som ligander i katalyse og organisk syntese. Et berømt område, hvor carbene-lignende enheder er vigtige, er metatese af olefiner, hvor Grubbs' katalysator (udviklet af Robert Grubbs) indeholder en ruthenium–alkylidene, der er afgørende for katalysens aktivitet.
Praktisk betydning
Carbenes og metal-carbenes spiller en central rolle i moderne organisk syntese og katalyse: de bruges til at bygge cykliske strukturer, indsætte funktionelle grupper og udføre transformationer, som er svære at gennemføre med andre reagenser. Forståelsen af singlet vs. triplet, substituent-effekter og metalstøtte er nødvendig for at styre deres reaktivitet sikkert og selektivt.