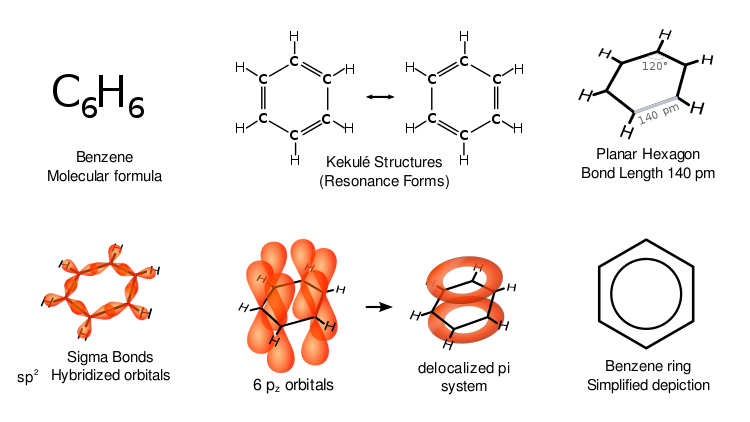Benzen, også kendt som benzol, er en organisk kemisk forbindelse med formlen 6CH6. Det er en farveløs og brandfarlig væske med en sødlig lugt. Benzenmolekyler er en ring af seks kulstofatomer, der hver er bundet til et hydrogenatom. Det er en aromatisk forbindelse – ikke blot en ring med vekslende dobbeltbindinger, men en struktur med delokaliserede π-elektroner, som giver ekstra stabilitet (aromatisk stabilisering).
Struktur og kemiske egenskaber
Benzen har en plan, hexagonal ringstruktur med seks lige lange kulstof–kulstof-bindinger. Den følger Hückels regel for aromatiske systemer (6 π-elektroner). Som følge af elektronernes delokalisering viser benzen særlige reaktionsmønstre: det gennemgår helst substitutionsreaktioner fremfor additionsreaktioner, fordi additionsreaktioner ville ødelægge aromatisk stabilitet.
- Fysiske egenskaber: Flygtig væske, lavt kogepunkt og smeltepunkt, uopløselig i vand men opløselig i organiske opløsningsmidler.
- Kemi: Relativt inert over for simple elektrofile additioner; indgår i reaktioner som nitrering, sulfonering og halogenering under kontrollerede betingelser.
Anvendelser
Benzen er en vigtig råvare i den kemiske industri. Det bruges både direkte som opløsningsmiddel i særlige industrielle processer og – vigtigst – som udgangsstof (råmateriale) til fremstilling af en lang række kemikalier og produkter:
- Fremstilling af styren (til polystyren), phenol og anilin samt cyclohexan.
- Produktion af plastik, syntetisk gummi, farvestoffer og mange andre mellemprodukter.
- Bruges som industrielt opløsningsmiddel i udvalgte processer (dog er anvendelsen som almindeligt opløsningsmiddel i mange lande begrænset på grund af sundhedsrisici).
- Benzen indgår naturligt i råolie og findes derfor i benzin, hvor det bidrager til oktantal og andre egenskaber, men indholdet er reguleret.
- Mange lægemidler og organiske molekyler er kemisk fremstillet fra benzen eller indeholder benzenringe som byggesten.
Sundhedsrisici og eksponering
Benzen er kræftfremkaldende (klassificeret som kræftfremkaldende for mennesker af bl.a. IARC). Kortvarig og langvarig eksponering kan give forskellige helbredseffekter:
- Akutte virkninger: Hovedpine, svimmelhed, kvalme, sløvhed eller bevidsthedspåvirkning ved høje koncentrationer (narcoselignende effekter ved indånding).
- Kroniske virkninger: Langvarig eksponering påvirker blod- og knoglemarvsfunktionen med risiko for anæmi, aplastisk anæmi og øget risiko for leukæmi (især akut myeloid leukæmi).
- Eksponeringsveje: Indånding er den mest almindelige; hudkontakt og i sjældne tilfælde indtagelse kan også forekomme.
På grund af disse risici er benzen omfattet af stramme arbejdsmiljøregler og brugen i forbrugerprodukter er begrænset i mange lande. Kontrolgrænser ligger typisk i ppm‑området eller lavere; arbejdsmiljømyndigheder og sundhedsorganisationer anbefaler så lave eksponeringsniveauer som praktisk muligt.
Sikkerhed, håndtering og førstehjælp
- Forebyggelse: Arbejd med benzen i lukkede systemer, brug god ventilation (fx procesventilation), og undgå åbne beholdere. Undgå antændelseskilder — benzen er meget brandfarligt.
- Personligt værneudstyr: Egnede handsker (fx nitril), kemikalieresistente dragter, og hvor påkrævet åndedrætsværn eller PAPR-enheder afhængigt af koncentrationen og varigheden af eksponering.
- Opbevaring: I lukkede, jordforbundne beholdere i en kølig, ventileret og brandmæssigt sikker zone, adskilt fra oxidanter.
- Førstehjælp: Ved indånding: Flyt den eksponerede person til frisk luft og søg læge ved symptomer. Ved hudkontakt: Fjern forurenet tøj og skyl med vand og sæbe. Ved øjenkontakt: Skyl grundigt med vand i mindst 15 minutter. Ved indtagelse: Undgå at fremkalde opkast; få straks lægehjælp. Kontakt altid læge ved alvorlig eksponering.
Miljø og regulering
Benzen forekommer naturligt i petroleum og frigives ved forbrænding af fossile brændstoffer, i biludstødning og fra industrielle kilder. I miljøet kan benzen fordampe fra overflader og spredes i luften; det kan også forurene jord og grundvand ved spild. Nedbrydning i naturen foregår bl.a. ved biologisk nedbrydning, men afhænger af betingelserne.
På grund af helbredsrisiciene reguleres benzen i mange lande i forhold til indhold i brændstoffer, emissioner fra industri og arbejdspladsgrænser. For aktuelle grænseværdier og anbefalinger bør man konsultere nationale myndigheder (arbejdsmiljøinstitutter eller miljøstyrelser).
Analyse og biomonitorering
Til påvisning og måling af benzen i luft og væsker anvendes metoder som gaschromatografi (ofte med massespektrometri, GC‑MS) og enkelte hurtige instrumenter (f.eks. fotoionisationsdetektorer). Biologisk overvågning kan bestå af måling af benzenuitskillelse i blod eller urin, eller af determinanter som trans,trans-mukonsyre og S-fenylmerkapturinsyre i urinen.
Alternativer og reduceret brug
På grund af sundhedsfarerne forsøger industrien og regulatorer at erstatte benzen hvor muligt med mindre toksiske alternativer eller at minimere brugen ved at benytte lukkede processer, reformulere produkter og begrænse emissioner. I mange forbrugerprodukter er benzenindhold kraftigt reduceret eller forbudt.
Samlet set er benzen en kemisk vigtig, men sundhedsmæssigt farlig forbindelse. Kendskab til dens egenskaber, sikker håndtering, overvågning og gældende regler er væsentligt for at minimere risikoen for mennesker og miljø.

_1964,_MiNr_440.jpg)