Grignard-reaktion: Definition, mekanisme og anvendelser
Grignard-reaktion: lær definition, mekanisme og anvendelser — praktiske tips, reaktionsmekanik, begrænsninger og sikkerhed for effektiv dannelse af C–C og C–heteroatom-bindinger.
Grignard-reaktionen (udtales /ɡriɲar/) er en organometallisk kemisk reaktion, hvor alkyl- eller aryl-magnesiumhalogenider (Grignard-reagenser) angriber elektrofilt kulstofatomer, der er til stede i polære bindinger (f.eks. i en carbonylgruppe som i eksemplet nedenfor). Grignard-reagenser virker som nukleofile. Grignard-reaktionen danner en kulstof-kulstof-binding. Den ændrer hybridiseringen omkring reaktionscentret. Grignard-reaktionen er et vigtigt redskab til dannelse af kulstof-kulstof-bindinger. Den kan også danne kulstof-fosfor-, kulstof-tin-, kulstof-silicium-, kulstof-bor- og andre kulstof-heteroatombindinger.
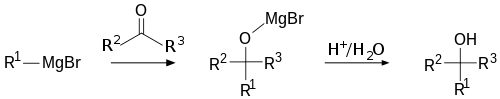
Mekanisme
Grignard-reagenser har formelt formlen R–MgX (R = alkyl eller aryl, X = halogen). De opfører sig som kilder til et stærkt nukleofilt kulstof (ofte omtalt som en "carbanion-lignende" art). Ved angreb på en carbonylgruppe sker en nukleofil additionsreaktion: det nukleofile kulstof binder til carbonylcarbonet og danner et alkoxid-kompleks bundet til magnesiumionen. Efter en sur (protisk) arbejdsopsætning (f.eks. tilsætning af vand eller fortyndet syre) protoneres alkoxidet og giver det tilsvarende alkohol.
Generelt trinvis skematisk for carbonyladditioner:
- R–MgX + R'–C(=O)–R'' → R'–C(OMgX)(R)(R'') (alkoxid–Mg kompleks)
- Arbejd-up (H3O+ eller H2O) → R'–C(OH)(R)(R'') (alkohol) + Mg(OH)X
Forberedelse og reaktionsbetingelser
Grignard-reagenser fremstilles typisk ved reaktion mellem magnesiummetal og et alkyl- eller arylhalogenid i et æteropløsningsmiddel (f.eks. diethylæter eller THF). Æteren koordinerer til magnesium og stabiliserer reagenset, som ofte eksisterer som aggregater eller klynger frem for simple ioniske par. Den høje pKa for de tilsvarende kulbrinter (pKa ≈ 45–50) betyder, at reaktionen med carbonylkomponenter i praksis er irreversible, og at RMgX opfører sig som en meget stærk base.
Fremstilling kræver absolut tørre forhold, da nærvær af protiske forbindelser (vand, alkoholer, aminer) ødelægger reagenset. For at fjerne fugt bruges ofte flammetørring, inert gas (N2 eller Ar), Schlenk-teknik eller handskemiljøer. Aktivisering af magnesiumoverfladen kan ske ved mekanisk omrøring, ultralyd, tilsætning af en lille mængde jod eller 1,2-dibromoethan for at starte reaktionen. Originalteksten nævner ultralyd som en aktiveringsmetode — det kan hjælpe med at fjerne overfladelag af oxid og øge reaktionshastigheden.
Typiske reaktioner og anvendelser
Grignard-reaktionen er et centralt redskab i organisk syntese til konstruktion af C–C-bindinger. Nogle almindelige reaktionstyper:
- Formaldehyd → primære alkoholer (ved arbejdsopsætning)
- Aldehyder → sekundære alkoholer
- Ketoner → tertiære alkoholer
- Estere og acylhalider → efter to ækvivalenter ofte tertiære alkoholer (via additon til carbonyl og videre reaktion)
- Carboxylation (CO2) → efter arbejde op giver carboxylsyre (brug af CO2 er en måde at danne karboxylsyrer fra R-MgX)
- Epoxider → ringåbning giver sekundære eller primære alkoholer afhængigt af regiokemi
- Nitriler → after hydrolyse giver ketoner
- Reaktioner med elektrofile heteroatom-komponenter giver f.eks. C–Si, C–B, C–P, C–Sn bindinger (afhængig af det electrophile substrat)
Begrænsninger og særlige hensyn
Ulemper ved Grignard-reagenser inkluderer:
- Følsomhed over for protiske opløsningsmidler og funktionelle grupper med sure protoner (f.eks. –OH, –NH), som hurtigt deaktiverer reagenset ved protonoverførsel.
- Luftfugtighed påvirker udbyttet ved syntese af Grignard-reagenser; derfor er tørre procedurer nødvendige.
- Grignard-reagenser reagerer generelt ikke effektivt med alkylhalogenider via en simpel bimolekylær SN2-mekanisme; i stedet kan reaktionen gå via single-electron transfer (SET) og radikalveje, hvilket ofte fører til bivirkninger som koblingsprodukter (f.eks. Wurtz-lignende koblinger) eller ringreaktioner.
- Sikkerhed: reaktioner kan være stærkt exoterme ved dannelse eller ved quench; kontakt med vand eller luft kan frigive brændbare gasser og varme. Arbejde med Grignard-reagenser kræver egnede forholdsregler — inert atmosfære, passende køling ved eksoterme trin og sikkerhedsprocedurer ved quench.
Praktiske tips for succesfulde Grignard-reaktioner
For at opnå gode resultater:
- Brug tørrede opløsningsmidler (distilleret eller købt anhydrous) og tørre beholdere.
- Aktiver magnesium som nødvendigt (ultralyd, frisk metal, tilsæt en initierer såsom jod eller en spor af en reaktiv halogenforbindelse).
- Kontroller halidets reaktivitet: iodider og bromider reagerer lettere end chlorider.
- Planlæg arbejdsopsætning (acid work-up) til sidst for at omdanne alkoxider til alkoholprodukter.
- Undgå substrater med protiske eller stærkt elektrontrækende funktionelle grupper medmindre disse er beskyttet eller beregnet til at blive omdannet først.
Det er også godt at være opmærksom på alternative metodikker til dannelse af C–C-bindinger, fx organozink- eller organocuprat-reaktioner, når funktionel gruppe-tolerance kræver mildere reagenser.
Det er en nukleofil organometallisk additionsreaktion. Den høje pKa -værdi af alkylkomponenten (pKa = ~45) gør reaktionen irreversibel. Grignard-reaktioner er ikke ioniske. Grignard-reagenset findes som en organometallisk klynge (i ether).
Ulempen ved Grignard-reagenser er, at de let reagerer med protiske opløsningsmidler (f.eks. vand) eller med funktionelle grupper med sure protoner som f.eks. alkoholer og aminer. Luftfugtighed kan ændre udbyttet ved fremstilling af et Grignard-reagens af magnesiumspåner og et alkylhalogenid. En af de mange metoder, der anvendes til at udelukke vand fra reaktionsatmosfæren, er at flammetørre reaktionsbeholderen for at fordampe al fugt, hvorefter den forsegles for at forhindre, at fugten vender tilbage. Kemikere bruger derefter ultralyd til at aktivere magnesiumets overflade, så det forbruger alt tilstedeværende vand. Dette kan gøre det muligt at danne Grignard-reagenser med mindre følsomhed over for tilstedeværelsen af vand.
En anden ulempe ved Grignard-reagenser er, at de ikke let danner kulstof-kulstof-bindinger ved at reagere med alkylhalogenider ved en SN 2-mekanisme.
François Auguste Victor Grignard opdagede Grignard-reaktioner og -reagenser. De er opkaldt efter denne franske kemiker (fra universitetet i Nancy, Frankrig), som fik Nobelprisen i kemi i 1912 for dette arbejde. Opdagelsen ændrede organisk syntese fundamentalt ved at give kemikere en pålidelig måde at bygge kulstofskeletter på, og Grignard-reaktioner er stadig en grundpille i moderne organisk kemi.

En opløsning af en carbonylforbindelse tilsættes til et Grignard-reagens. (Se galleri nedenfor)
Reaktionsmekanisme
Additionen af Grignard-reagenset til en carbonylgruppe foregår typisk gennem en seks-ledet ringovergangstilstand.
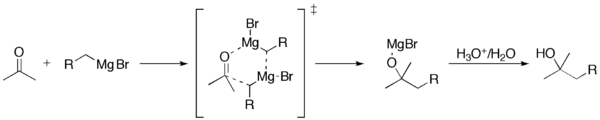
Med sterisk hæmmede Grignard-reagenser kan reaktionen imidlertid foregå ved enkeltelektronoverførsel.
Grignard-reaktioner fungerer ikke, hvis der er vand til stede; vand får reagenset til hurtigt at blive nedbrudt. De fleste Grignard-reaktioner finder derfor sted i opløsningsmidler som vandfri diethylether eller tetrahydrofuran (THF), fordi ilten i disse opløsningsmidler stabiliserer magnesiumreagenset. Reagensen kan også reagere med ilt i atmosfæren. Herved indsættes et oxygenatom mellem kulstofbasen og magnesiumhalogenidgruppen. Normalt kan denne bivirkningsreaktion begrænses af, at de flygtige opløsningsmiddeldampe fortrænger luft over reaktionsblandingen. Kemikere kan dog udføre reaktionerne i nitrogen- eller argonatmosfære. I små reaktioner har opløsningsmiddeldampene ikke plads nok til at beskytte magnesiumet mod ilt.
Fremstilling af en Grignard-reagens
Grignard-reagenser dannes ved virkning af et alkyl- eller arylhalogenid på magnesiummetal. Reaktionen udføres ved at tilsætte det organiske halogenid til en suspension af magnesium i en ether, som tilfører de ligander, der er nødvendige for at stabilisere den magnesiumorganiske forbindelse. Typiske opløsningsmidler er diethylether og tetrahydrofuran. Ilt og protiske opløsningsmidler som f.eks. vand eller alkoholer er ikke forenelige med Grignard-reagenser. Reaktionen foregår ved enkeltelektronoverførsel.
R-X + Mg → R-X•− + Mg•+
R-X•− → R• + X−
X− + Mg•+ → XMg•
R• + XMg• → RMgX
Grignard-reaktioner starter ofte langsomt. Først er der en induktionsperiode, hvor reaktivt magnesium bliver eksponeret for de organiske reagenser. Efter denne induktionsperiode kan reaktionerne være stærkt eksoterme. Alkyl- og arylbromider og -jodider er almindelige substrater. Chlorider anvendes også, men fluorider er generelt ikke reaktive, undtagen med specielt aktiveret magnesium, som f.eks. Rieke-magnesium.
Mange Grignard-reagenser, f.eks. methylmagnesiumchlorid, phenylmagnesiumbromid og allylmagnesiumbromid, fås i handelen i tetrahydrofuran- eller diethyletheropløsninger.
Ved hjælp af Schlenk-ligevægten danner Grignard-reagenser varierende mængder diorganomagnesiumforbindelser (R = organisk gruppe, X = halogenid):
2 RMgX R![]() 2 Mg + MgX2
2 Mg + MgX2
Indvielse
Der er udviklet mange metoder til at initiere Grignard-reaktioner, som er langsomme at starte. Disse metoder svækker det lag af MgO, der dækker magnesiumet. De eksponerer magnesiumet for det organiske halogenid for at starte den reaktion, der danner Grignard-reagenset.
Mekaniske metoder omfatter knusning af Mg-stykkerne in situ, hurtig omrøring eller anvendelse af ultralyd (sonicering) af suspensionen. Jod, methyljodid og 1,2-dibromometan er almindeligt anvendte aktiveringsmidler. Kemikere anvender 1,2-dibrometan, fordi dets virkning kan overvåges ved observation af ethylenbobler. Desuden er biprodukterne uskadelige:
Mg + BrC H24 Br → C H24 + MgBr2
Mg-forbruget af disse aktiveringsmidler er normalt ubetydeligt.
Tilsætning af en lille mængde kviksølvklorid vil amalgamere metallets overflade, så det kan reagere.
Industriel produktion
Grignard-reagenser fremstilles i industrien til brug på stedet eller til salg. Som i bench-scale er det største problem initiering. En del af en tidligere batch af Grignard-reagenset anvendes ofte som initiator. Grignard-reaktioner er exoterme; denne exotermi skal tages i betragtning, når en reaktion skaleres fra laboratorie- til produktionsanlæg.
Reaktioner af Grignard-reagenser
Reaktioner med carbonylforbindelser
Grignard-reagenser reagerer med en række forskellige carbonylderivater.
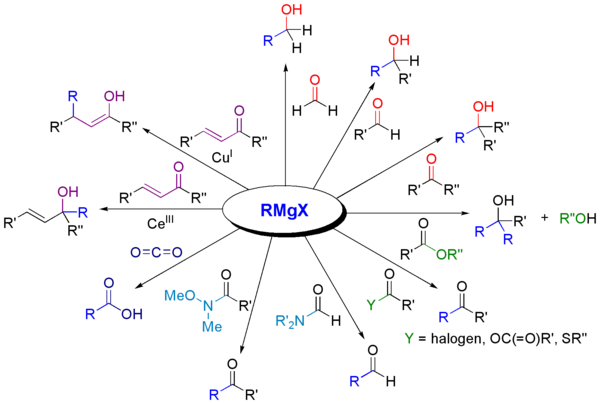
Den mest almindelige anvendelse er alkylering af aldehyder og ketoner, som i dette eksempel:
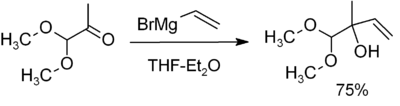
Bemærk, at acetalfunktionen (en maskeret carbonyl) ikke reagerer.
Sådanne reaktioner involverer normalt en vandbaseret (vandig) sur oparbejdning, selv om dette sjældent fremgår af reaktionsskemaerne. I tilfælde, hvor Grignard-reagenset tilsættes til en prochiral aldehyd eller keton, kan Felkin-Anh-modellen eller Cram's regel normalt forudsige, hvilken stereoisomer der vil blive dannet.
Reaktioner med andre elektrofile stoffer
Desuden vil Grignard-reagenser reagere med elektrofiler.
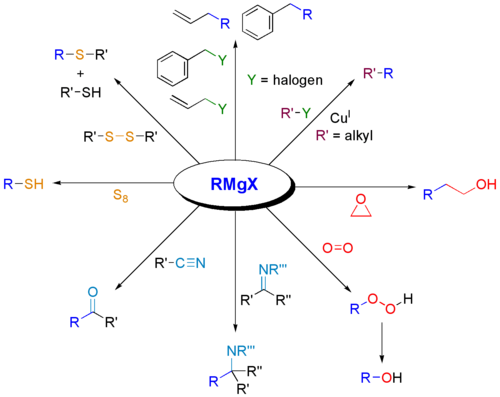
Et andet eksempel er fremstilling af salicylaldehyd (ikke vist ovenfor). Først reagerer bromethan med Mg i ether. For det andet omdannes phenol i THF til Ar-OMgBr. For det tredje tilsættes benzen i nærværelse af paraformaldehydpulver og triethylamin. For det fjerde destilleres blandingen for at fjerne opløsningsmidlerne. Derefter tilsættes 10% HCl. Salicylaldehyd vil være det vigtigste produkt, så længe det hele er meget tørt og under inerte forhold. Reaktionen fungerer også med jodoethan i stedet for bromoethan.
Dannelse af bindinger til B, Si, P, Sn
Grignard-reagenset er meget nyttigt til dannelse af kulstof-heteroatombindinger.
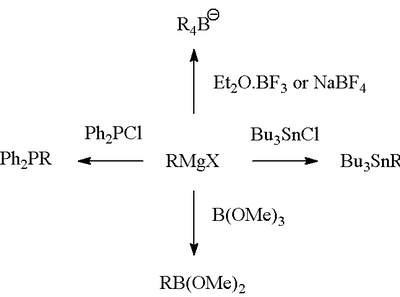
Kulstof-kulstof-koblingsreaktioner
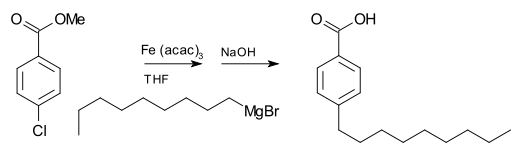
Et Grignard-reagens kan også indgå i koblingsreaktioner. F.eks. reagerer nonylmagnesiumbromid med methyl p-chlorbenzoat til p-nonylbenzoesyre i tilstedeværelse af Tris(acetylacetonato)jern(III), ofte symboliseret som Fe(acac)3 , efter behandling med NaOH for at hydrolytere esteren, som vist som følger. Uden Fe(acac)3 ville Grignard-reagenset angribe estergruppen frem for arylhalogenidet.
Til kobling af arylhalogenider med arylgrignarder er nikkelchlorid i tetrahydrofuran (THF) også en god katalysator. En effektiv katalysator til koblinger af alkylhalogenider er desuden dilithiumtetrachlorocuprat (Li2 CuCl4 ), der fremstilles ved at blande lithiumchlorid (LiCl) og kobber(II)chlorid (CuCl2 ) i THF. Kumada-Corriu-koblingen giver adgang til [substituerede] styrener.
Oxidation
Oxidation af et Grignard-reagens med ilt sker gennem et radikalt mellemprodukt til magnesiumhydrogenperoxid. Hydrolyse af dette kompleks giver hydroperoxider, og reduktion med yderligere en ækvivalent Grignard-reagens giver en alkohol.
En reaktion af Grignards med ilt i tilstedeværelse af en alken giver en ethylenudvidet alkohol. Disse er nyttige til at syntetisere større forbindelser. Denne modifikation kræver aryl- eller vinylgrignardreagenser. Tilsætning af Grignard-reagenser og alken alene resulterer ikke i en reaktion, hvilket viser, at tilstedeværelsen af ilt er afgørende. Den eneste ulempe er kravet om mindst to ækvivalenter af Grignard-reagenset i reaktionen. Dette kan løses ved at anvende et dobbelt Grignard-system med et billigt reducerende Grignard-reagens som f.eks. n-butylmagnesiumbromid.
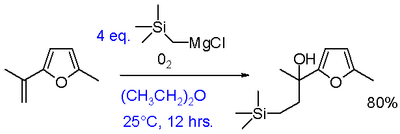
Nukleofil alifatisk substitution
Grignard-reagenser er nukleofile i nukleofile alifatiske substitutioner, f.eks. med alkylhalogenider i et vigtigt trin i den industrielle produktion af Naproxen:
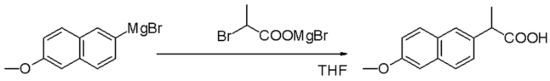
Eliminering
I Boord-olefinsyntesen resulterer additionen af magnesium til visse β-haloethere i en eliminationsreaktion til alkenet. Denne reaktion kan begrænse anvendeligheden af Grignard-reaktioner.
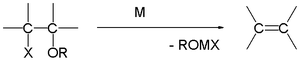
Grignard-nedbrydning
Grignard-nedbrydning var engang et værktøj til strukturidentifikation (opklaring), hvor et Grignard RMgBr dannet af et heteroarylbromid HetBr reagerer med vand til Het-H (brom erstattet af et hydrogenatom) og MgBrOH. Denne hydrolysemetode gør det muligt at bestemme antallet af halogenatomer i en organisk forbindelse. I moderne tid anvendes Grignard-nedbrydning til kemisk analyse af visse triacylglyceroler.
Industriel anvendelse
Et eksempel på Grignard-reaktionen er et vigtigt trin i den industrielle fremstilling af tamoxifen. (Tamoxifen anvendes i øjeblikket til behandling af østrogenreceptorpositiv brystkræft hos kvinder):
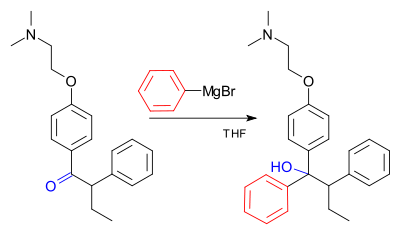
Galleri
· 
Magnesiumspåner anbragt på en kolbe.
· 
Dækkes med THF og tilsættes et lille stykke jod.
· 
En opløsning af alkylbromid blev tilsat under opvarmning.
· 
Efter endt tilsætning opvarmes blandingen i et stykke tid.
· 
Dannelsen af Grignard-reagenset var afsluttet. Der var stadig en lille mængde magnesium tilbage i kolben.
· 
Det således fremstillede Grignard-reagens blev afkølet til 0 °C inden tilsætning af carbonylforbindelsen. Opløsningen blev grumset, da Grignard-reagenset udfældede.
· 
En opløsning af carbonylforbindelse blev tilsat til Grignard-reagenset.
· 
Opløsningen blev opvarmet til stuetemperatur. Reaktionen var fuldstændig.
Relaterede sider
- Wittig-reaktion
- Barbier-reaktion
- Bodroux-Chichibabin aldehyd-syntese
- Fujimoto-Belleau-reaktionen
- Organolithiumreagenser
- Sakurai reaktion
Spørgsmål og svar
Spørgsmål: Hvad er Grignard-reaktionen?
A: Grignard-reaktionen er en organometallisk kemisk reaktion, hvor alkyl- eller aryl-magnesiumhalogenider (Grignard-reagenser) angriber elektrofilt kulstofatomer, der er til stede i polære bindinger.
Sp: Hvilken type binding dannes der ved Grignard-reaktionen?
Svar: Grignard-reaktionen danner en kulstof-kulstof-binding.
Sp: Hvilke andre typer bindinger kan dannes ved hjælp af Grignard-reaktionen?
Svar: Grignard-reaktionen kan også danne kulstof-fosfor-, kulstof-tin-, kulstof-silicium-, kulstof-bor- og andre kulstof-heteroatom-bindinger.
Spørgsmål: Hvordan påvirker alkylkomponentens høje pKa-værdi Grignard-reaktionen?
Svar: Den høje pKa-værdi af alkylkomponenten (pKa = ~45) gør reaktionen irreversibel.
Sp: Hvilken type additionsreaktioner deltager Grignard-reagenser i?
Svar: Grignard-reagenser deltager i nukleofile organometalliske additionsreaktioner.
Spørgsmål: Hvilke ulemper er der forbundet med brugen af Grignard-reagenser? Svar: Nogle af ulemperne ved anvendelse af Grignard-reagenser er deres reaktivitet med protiske opløsningsmidler som f.eks. vand og funktionelle grupper med sure protoner, f.eks. alkoholer og aminer, deres følsomhed over for luftfugtighed og deres vanskeligheder med at danne kulstof-kulstofbindinger ved at reagere med alkylhalogenider ved en SN2-mekanisme.
Sp: Hvem opdagede Grigand-reaktionen og -reagenserne?
Svar: Opdagelsen af Griand-reaktionen og -reagenset tilskrives den franske kemiker Franחois Auguste Victor Griand, som fik Nobelprisen i kemi i 1912 for dette arbejde.
Søge
