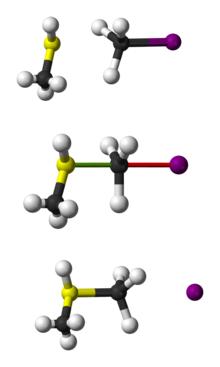
SN 2-reaktionen (også kendt som bimolekylær nukleofil substitution) er en substitutionsreaktion i organisk kemi. Det er en type nukleofil substitution, hvor et ensomt par fra en nukleofil angriber et elektronmanglende elektrofilt center og binder sig til det. Herved udstødes en anden gruppe, der kaldes en "leaving group". Den indgående gruppe erstatter altså den udgående gruppe i ét trin. Da to reagerende arter er involveret i det langsomme, hastighedsbestemmende trin af reaktionen, fører dette til navnet bimolekylær nukleofil substitution eller SN 2. Blandt uorganiske kemikere er SN 2-reaktionen ofte kendt som udvekslingsmekanismen.
Mekanisme og overgangstilstand
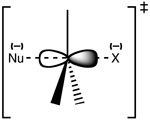
SN 2-reaktionen forløber concerted (i ét trin) uden stabile intermediater. Nukleofilen angriber bagfra i forhold til leaving group, hvilket fører til en overgangstilstand, hvor det elektrofilt centrum er delvist bundet til både den indgående nukleofil og den udgående gruppe. Overgangstilstanden kan beskrives som pentacoordineret eller "dobbeltbundet" på et øjeblik—der er delvise bindinger til både nukleofil og leaving group. Når reaktionen fuldføres, forlader leaving group, og produktet dannes.
Hastighed (kinetik)
SN 2-reaktioner følger andenordens kinetik med hastighedsloven:
rate = k [nukleofil] [substrat]
Det betyder, at hastigheden er proportional med koncentrationerne af både nukleofil og det elektrofilt centrum (typisk et alkohol derivat som en alkylhalid).
Faktorer der påvirker reaktionshastigheden
- Substratets struktur: Methyl- og primære centrum reagerer hurtigst. Sekundære centrum reagerer langsommere pga. sterisk hindring. Tertiære centrum reagerer næsten ikke via SN 2 på grund af kraftig sterisk afskærmning.
- Nukleofilens styrke: Stærkere nukleofiler (typisk negative ioner, mindre sterisk hæmmede) fremmer SN 2. Nucleofilens basisitet og polariserbarhed spiller ind.
- Leaving group: En god leaving group er en svag base og stabil som anion (f.eks. I– > Br– > Cl–; OH– er dårlig uden aktivering).
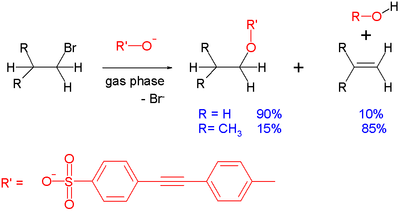
- Solvent: Polar aprotiske opløsningsmidler (f.eks. acetone, DMF, DMSO) øger hastigheden for anioniske nukleofiler, fordi de ikke hydrogenbinder stærkt til nukleofilen. Protic solventer (f.eks. vand, alkohol) kan nedsætte nukleofilens reaktivitet ved solvatisering.
- Steriske effekter: Store substituenter omkring reaktionscentret blokerer for backside attack og nedsætter hastigheden.
- Resonans og elektrontrækning: Allyl- og benzyl-centre er ofte mere reaktive end simple alifatiske centre pga. stabilisering af overgangstilstanden; elektrontrækkende grupper kan gøre centrum mere elektrofil.
Stereokemi
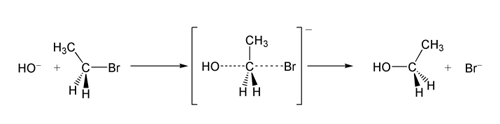
En karakteristisk egenskab ved SN 2 er stereospecifik inversion af konfiguration ved et chiralt center (Walden-inversion). Fordi nukleofilen angriber fra den modsatte side af leaving group, får man en inversion af den tredimensionelle opbygning, hvilket gør reaktionen nyttig til selektiv stereokemisk syntese.
Sammenligning med SN1
- SN2 er concerted og bimolekylær (rate afhænger af begge reaktanter).
- SN1 forløber via et karbokationisk mellemtrin (unisubstitueret trin), og hastigheden erordnet efter [substrat] alene; ofte foretrækkes tertiære centre i SN1.
- Stereokemisk: SN2 giver inversion, SN1 ofte racemisering (pga. plan karbokation der kan angribes fra begge sider).
Praktiske eksempler
- Williamson-ethersyntese: en alkoxid reagerer med et primært alkylhalid via SN2 for at danne en ether.
- Cyanid substitution: R–Br + CN– → R–CN (ofte hurtig SN2 for primære og sekundære halider).
- Hydroxid substitution: R–X + OH– → R–OH (kræver ofte gode leaving groups eller aktivering).
Yderligere betragtninger
SN 2-reaktioner er centrale i organisk syntese pga. deres forudsigelige kinetik og stereokemiske konsekvenser. I praksis vælger man reaktanter og opløsningsmiddel for at maksimere hastighed og ønsket stereokemi—f.eks. bruge polar aprotiske opløsningsmidler for at fremme reaktiviteten af anioniske nukleofiler, og vælge primære substrater for at undgå konkurrerende mekanismer. Dertil kan ionstyrke, temperatur og tilstedeværelse af komplekserende kationer (f.eks. kronen-ethers eller 18-crown-6) også ændre reaktionsforløbet.