Enzymer er proteinmolekyler i celler, der fungerer som biologiske katalysatorer. Enzymer fremskynder kemiske reaktioner i kroppen, men bliver ikke opbrugt i processen og kan derfor bruges igen og igen.
Næsten alle biokemiske reaktioner i levende væsener kræver enzymer. Med et enzym går de kemiske reaktioner meget hurtigere, end de ville gøre uden enzymet.p39 Andre biokatalysatorer er katalytiske RNA-molekyler, kaldet ribozymer.
De stoffer, der står i begyndelsen af en reaktion, kaldes substrater. De stoffer, der er i slutningen af en reaktion, er produkterne. Enzymer arbejder på substraterne og omdanner dem til produkter. Studiet af enzymer kaldes enzymologi.
Det første enzym blev fundet i 1833 af Anselme Payen.
Hvordan enzymer virker
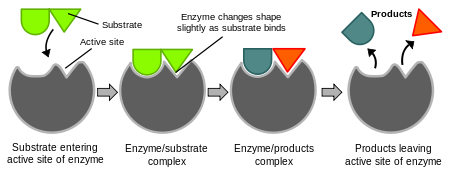
Enzymer har en specifik tredimensionel struktur med et aktivt sted, hvor substratet bindes. Bindingen mellem enzym og substrat kan beskrives med modeller som "lock-and-key" eller den mere realistiske "induced fit", hvor enzymet ændrer form en smule ved substratbinding for at optimere reaktionen. Det aktive sted sænker aktiveringsenergien for reaktionen, så omdannelsen til produkter sker hurtigere.
Kofaktorer og koenzymer
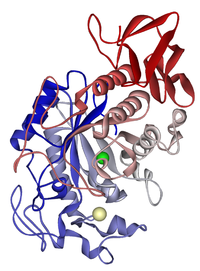
Nogle enzymer kræver ikke-protein komponenter for at fungere korrekt. Kofaktorer kan være metalioner (fx Mg2+, Zn2+, Fe2+) eller organiske molekyler kaldet koenzymer (fx NAD+, FAD, coenzym A). Disse hjælper med elektron- eller gruppetransfer og er nødvendige for enzymets katalytiske aktivitet.
Enzymkinetik og regulering
Enzymkinetik beskriver, hvordan reaktionshastigheden afhænger af substratkoncentration og enzymets egenskaber. Michaelis–Menten-ligningen er en grundlæggende model med parametrene Vmax (maksimal hastighed) og Km (substratkoncentration ved halvdelen af Vmax), der siger noget om enzymets effektivitet og affinitet for substratet.
Regulering af enzymaktivitet sker på flere niveauer:
- Allosterisk regulering, hvor små regulatoriske molekyler binder et andet sted end det aktive sted og ændrer enzymets aktivitet.
- Reversibel eller irreversibel hæmning gennem inhibitorer (fx konkurrerende, non-konkurrerende eller uncompetitive hæmmere).
- Kontrol gennem genekspression og syntese/degradation af enzymet.
- Post-translationelle ændringer, fx fosforylering, som hurtigt kan tænde eller slukke et enzym.
Miljøfaktorer
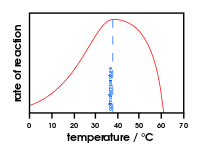
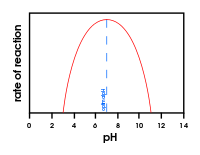
Enzymers aktivitet er følsom over for temperatur og pH. Hvert enzym har et optimalt temperatur- og pH-område, hvor aktiviteten er størst. Høj temperatur kan denaturere proteinstrukturen og derved inaktivere enzymet, mens skarpe pH-ændringer kan påvirke ladning og tredimensionel form i det aktive sted.
Typer af enzymer
Enzymer klassificeres ofte efter den type kemisk reaktion, de katalyserer: oxidoreduktaser, transferaser, hydrolaser, lyaser, isomeraser og ligaser. Eksempler på velkendte enzymer er amylase (nedbryder stivelse), proteaser (spalter proteiner), lipaser (nedbryder fedt) og DNA-polymeraser (kopierer DNA).
Betydning og anvendelser
Enzymer er afgørende for livet: de styrer stofskifte, energiproduktion, signalering og reparation i celler. Mangler eller defekte enzymer kan føre til arvelige sygdomme (fx nogle stofskiftesygdomme). I industrien udnyttes enzymer i vaskemidler, fødevareproduktion (f.eks. fermentering og ostefremstilling), bioteknologi (enzymatiske analyser, PCR og DNA-sekventering) og i lægemiddelproduktion.
Historie og forskning
Efter Anselme Payens opdagelse er studiet af enzymer vokset til et centralt felt i biokemi og molekylærbiologi. Moderne forskning undersøger enzymers struktur med røntgenkrystallografi og cryo-EM, designer kunstige enzymer og udvikler enzymhæmmere som lægemidler mod infektioner, cancer og metaboliske sygdomme.