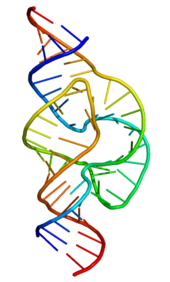
Et ribozym (ribonukleinsyreenzym) er et RNA-molekyle, der kan fremme og katalysere kemiske reaktioner på lignende måde som proteinenzymernes virkemåde. Ribozymer viser, at RNA ikke kun bærer genetisk information, men også kan danne tredimensionelle aktive steder, som udfører katalyse.
Funktioner og biologiske roller
Ribozymer deltager i flere fundamentale cellulære processer:
- I ribosomet ligger den katalytiske funktion i peptidyltransferasecentret i RNA, som sammenkæder aminosyrer under proteinsyntesen.
- De er centrale ved RNA-splejsning (fx gruppeselvspaltende introner og spliceosom-relaterede processer), hvor RNA-molekyler kan beskære og sammenføje sig selv eller andre RNA-molekyler.
- Nogle ribozymer, som viral replikerende elementer, deltager i replikation af vira eller viruslignende RNA.
- Andre ribozymer er involveret i biosyntese og bearbejdning af overførsels-RNA.
Mekanismen bag catalyse
Ribozymers katalyse bygger på RNA's evne til at folde sig i komplekse tredimensionelle strukturer, så nukleotidbaser og rygsøjle kan placeres tæt nok til at fremme kemiske reaktioner. De vigtigste katalytiske principper omfatter:
- General acid/base-katalyse: bestemte nukleotider i RNA kan fungere som protondonorer eller -acceptorer for at accelerere spaltning og sammenføjning af fosfodiesterbindinger.
- Metal-ion-katalyse: især Mg2+ (magnesiumioner) stabiliserer negative ladninger på RNA-rygsøjlen og deltager aktivt i overgangstilstanden under fosfodiesterspaltning eller -dannelse.
- Orientering og nærhed: foldning bringer reaktive grupper i nær kontakt, hvilket øger reaktionshastigheden.
- Tertiære interaktioner: strukturelle motiver som pseudoknuder, tetraløkker og tRNA-lignende foldninger er ofte nødvendige for aktiviteten.
Typer og velkendte eksempler
Der findes flere klasser af naturlige ribozymer:
- Hammerhead- og hairpin-ribozymer: små, selvspaltende motiver, der findes i plantevirusoider og satellit-RNA'er og ofte bruges i research og syntetisk biologi.
- RNase P: et ribonukleoprotein, hvor RNA-delen udfører den kemiske kløvning af præ-tRNA for at generere modne tRNA'er, ofte med hjælp fra proteinundersystemer.
- Grupp I og II introner: store selvspaltende introner, der kan katalysere deres egen excision og nogle gange fungere som mobiliserende elementer.
- Ribosomets peptidyltransferasecenter: et tydeligt eksempel på et funktionelt ribozym, hvor RNA i stor subenhed katalyserer peptidbindingens dannelse under translation.
Opdagelse og historisk betydning
Opdagelsen af ribozymer i begyndelsen af 1980'erne — bl.a. gennem arbejde af Thomas R. Cech og Sidney Altman — viste, at RNA både kan være genetisk materiale (DNA) og en biologisk katalysator. Deres banebrydende resultater førte til Nobelprisen i kemi i 1989 og stimulerede opbygningen af RNA-verdenshypotesen, som foreslår, at RNA-former med både informationslagring og katalytisk aktivitet kunne have været tidlige nøglekomponenter i livets oprindelse.
Ribozymers betydning for studiet af livets oprindelse
Forskere, der studerer livets oprindelse, ser ribozymer som plausible aktører i præbiotiske selvreplikerende systemer, fordi de forener to kritiske funktioner: informationslagring og katalyse. Hypotesen understøttes af laboratorieeksperimenter, hvor man har fremstillet syntetiske eller udviklede ribozymer, som kan kopiere RNA eller katalysere nøglereaktioner.
Laboratorieudvikling og polymerase-ribozymer
I laboratoriet er der udviklet ribozymer med polymerase-aktivitet, som kan katalysere forlængelse af RNA-strenge. Eksempler nævnt i litteraturen inkluderer varianter af "Round-18"-polymerase-ribozymet. Moderne varianter som "B6.61" kan, under visse betingelser, tilføje op til 20 nukleotider til en primerskabelon over 24 timer, indtil ribozymet selv går i stykker ved spaltning af dets fosfodiesterbindinger. Ribozymer som "tC19Z" har vist endnu større ydeevne og kan tilføje op til 95 nukleotider med høj nøjagtighed. Disse resultater opnås ofte via in vitro-selektion og directed evolution, hvor RNA-molekyler iterativt udvælges for ønskede egenskaber.
Medicinske og bioteknologiske anvendelser
Nogle ribozymer er blevet udviklet som terapeutiske midler og forskningsværktøjer:
- Som terapeutika ved målretning og spaltning af specifikke RNA-sekvenser (fx antivirale strategier), men klinisk anvendelse har været udfordret af stabilitet og levering til celler.
- Som biosensorer i diagnostik og syntetisk biologi, hvor ribozymer eller riboswitch-lignende strukturer registrerer små molekyler eller RNA-sekvenser og omformer denne binding til et målbart signal.
- Inden for genomforskning og molekylær biologi bruges ribozymer til at manipulere eller studere RNA-funktion, herunder som værktøj til at rense eller aktivere specifikke RNA-molekyler.
Begrænsninger og udfordringer
Selvom ribozymer har interessante egenskaber, er der begrænsninger:
- Stabilitet: RNA er generelt mere udsat for hydrolytisk nedbrydning end DNA eller proteiner, hvilket begrænser varigheden af mange ribozymers aktivitet i biologiske miljøer.
- Katalytisk effektivitet: Mange naturlige ribozymer arbejder langsommere eller med lavere effektivitet end protein-enzymer for visse reaktioner.
- Levering ved terapi: at få ribozymer ind i levende celler, beskytte dem mod nedbrydning og sikre specifik måldækning er praktiske barrierer for klinisk anvendelse.
Fremtidsperspektiver
Forskningen i ribozymer fortsætter både for at forstå grundlæggende biologiske processer og for at udvikle nye teknologier. Kombinationer af kemiske modifikationer, intelligente leveringssystemer og avanceret in vitro-evolution forbedrer stabilitet og aktivitet. I syntetisk biologi anvendes ribozymer og riboswitches som komponenter i regulerbare genkredsløb, og de laboratorie-evolverede polymeraser bringer os tættere på at demonstrere selvreplikerende RNA-systemer under simple betingelser — en vigtig test af RNA-verdenshypotesen.
Opsummering: Ribozymer er katalytiske RNA-molekyler med centrale roller i cellens RNA-håndtering og proteinsyntese, med store implikationer for vores forståelse af livets oprindelse og potentiale til anvendelse i terapi og bioteknologi. Fortsat forskning i deres struktur, mekanisme og laboratorieudvikling udvider både grundviden og praktiske muligheder.