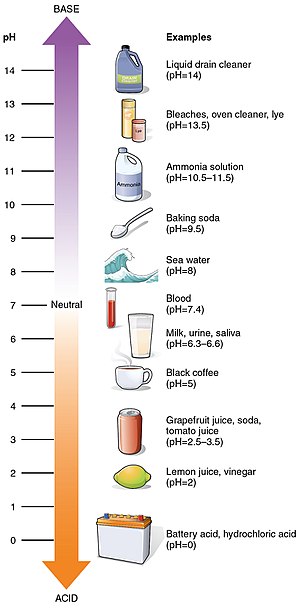
pH er en skala for surhedsgrad fra 0 til 14. Den angiver, hvor surt eller basisk et stof er. Mere sure opløsninger har en lavere pH-værdi. Mere basiske opløsninger har en højere pH-værdi. Stoffer, der ikke er sure eller basiske (dvs. neutrale opløsninger), har normalt en pH-værdi på 7. Syrer har en pH-værdi på under 7. Baser har en pH-værdi på over 7.
Hvad pH måler
pH er et mål for koncentrationen af protoner (H+) i en opløsning. S.P.L. Sørensen introducerede dette begreb i 1909. P'et står for det tyske potenz, der betyder kraft eller koncentration, og H'et for hydrogenionen (H+).
Formel og definition
Den mest almindelige formel til beregning af pH er:
pH = - log 10 [ H + ] {\displaystyle {\mbox{pH}}}=-\log _{10}\left[{\mbox{H}}}^{+}\right]}
[H+] angiver koncentrationen af H+-ioner (også skrevet [H3O+], den samme koncentration af hydroniumioner), målt i mol pr. liter (også kendt som molaritet).
Men den korrekte ligning er faktisk:
pH = - log 10 [ a H + ] {\displaystyle {\mbox{pH}}}=-\log _{10}\left[a_{\mathrm {H^{+}}} }\right]}
hvor a H + {\displaystyle a_{\mathrm {H^{{+}} }}}
pH-skalaen og ekstreme værdier
De fleste stoffer har en pH-værdi i intervallet 0–14. Dette interval kommer fra vandets autodissociation og dets ionprodukt ved 25 °C, men ekstremt sure opløsninger kan have pH < 0, og ekstremt alkaliske opløsninger kan have pH > 14. Sådanne værdier forekommer ved meget høje koncentrationer af stærke syrer eller baser.
Syrer, baser og hydroxid
Syrer er stoffer, der øger H+-koncentrationen i en opløsning, mens baser reducerer den (ofte ved at afgive OH-, hydroxidioner). Basiske stoffer har i stedet for hydrogenioner en koncentration af hydroxidioner (OH-) i stedet for hydrogenioner. Forholdet mellem [H+] og [OH-] i vand er givet ved ionproduktet:
- Kw = [H+][OH-] ≈ 1,0×10^-14 ved 25 °C
- Derfor gælder pH + pOH = 14 ved 25 °C (hvor pOH = -log10[OH-]).
Måling af pH i praksis
Der findes flere metoder til at måle pH:
- pH-meter: elektronisk måling med en glaselektrode; giver præcise værdier og bruges i laboratorier, industri og feltarbejde.
- pH-indikatorpapir: fra indikatorstrimler til universale indikatorer; giver et hurtigt, omtrentlig mål.
- Syre-base indikatorer: farvestoffer (f.eks. phenolphthalein, methylrød) skifter farve i bestemte pH-intervaller og bruges i titreringer.
Ved præcise målinger påvirker temperatur, ionstyrke og elektrodekalibrering resultatet, så korrektion for temperatur og brug af standardbufferopløsninger anbefales.
Eksempler på typiske pH-værdier
- Stærk syre (fx 1 M HCl): pH ≈ 0
- Citron/eddike: pH ≈ 2–3
- Rent vand (neutral, 25 °C): pH ≈ 7
- Husholdningssæbe: pH ≈ 9–10
- Stærk base (fx 1 M NaOH): pH ≈ 14
- Havvand: typisk pH ≈ 7,5–8,4 (afhænger af opløste salte og vejrmæssige forhold)
- Menneskers blod: normalt pH ≈ 7,35–7,45 (stramt reguleret i kroppen)
Buffersystemer og biologisk betydning
Buffersystemer modvirker ændringer i pH ved at optage eller afgive H+-ioner. Eksempler:
- Karbonat-bikarbonat-systemet i blod og havvand (CO2/H2CO3 ↔ HCO3- ↔ CO32-).
- Fosfat-buffer i celler.
- Proteiner og aminosyrer, som kan fungere som buffere i biologiske systemer.
pH er kritisk i biologi, kemi, landbrug og miljø: en lille ændring i pH kan påvirke enzymaktivitet, toksicitet af metalioner, jordbundens næringsstoftilgængelighed og mange industrielle processer.
Temperaturens indflydelse
Vandets ionprodukt (Kw) og dermed sammenhængen mellem pH og pOH er temperaturafhængig. Ved højere temperaturer stiger Kw, hvilket betyder, at neutral pH (hvor [H+] = [OH-]) ikke nødvendigvis er 7 ved andre temperaturer end 25 °C. Derfor angives pH-målinger ofte sammen med prøvens temperatur eller der anvendes temperaturoverensstemmelse ved måling.
Regningseksempel
Hvis en opløsning har [H+] = 1,0×10^-3 mol/L, så er pH = -log10(1,0×10^-3) = 3. Hvis man kender [OH-] i stedet for [H+], kan man finde pH ved først at beregne pOH = -log10[OH-] og derefter bruge pH = 14 - pOH (ved 25 °C).
Samlet set er pH et enkelt, men kraftfuldt mål for surhedsgrad, som bygger på logaritmisk skala af hydrogenionaktivitet eller koncentration og har afgørende betydning i mange naturvidenskabelige og tekniske sammenhænge.
Basiske stoffer har i stedet for hydrogenioner en koncentration af hydroxidioner (OH-) i stedet for hydrogenioner.
![{\displaystyle {\mbox{pH}}=-\log _{10}\left[{\mbox{H}}^{+}\right]}](https://www.alegsaonline.com/image/093977a79b6a17e02db4699475930e48c05d6468.svg)
![{\displaystyle {\mbox{pH}}=-\log _{10}\left[a_{\mathrm {H^{+}} }\right]}](https://www.alegsaonline.com/image/7a631c4037415f3d4483a6cb07e69858b64890fc.svg)