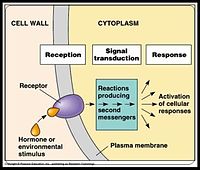
En signaltransduktion i biologien er en cellulær mekanisme. Den omdanner en stimulus til et respons i cellen. Der er to faser i denne proces:
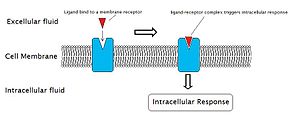
- Et signalmolekyle knytter sig til et receptorprotein på cellemembranen.
- En anden budbringer sender signalet videre ind i cellen, og der sker en ændring i cellen.
Signaltransduktion starter altså med et signal til en cellereceptor og slutter med en ændring i cellens funktion. I begge trin kan signalet forstærkes. Et signalmolekyle kan således forårsage mange reaktioner.
Receptorer: typer og lokalisering
Receptorer findes ofte i cellemembranen, hvor en del af receptoren vender ud mod omgivelserne og en del vender ind i cellens indre. Det kemiske signal binder sig til den ydre del af receptoren og ændrer dens konformation. Dette føre til et indre signal. Nogle signalmolekyler, fx testosteron, er dog lipofile og kan passere cellemembranen for direkte at binde receptorer i cytoplasmaet eller i kernen. Sådanne receptorer fungerer ofte som transkriptionsfaktorer og regulerer DNA-udtryk direkte.
De mest almindelige receptorfamilier er:
- G-protein-koblede receptorer (GPCR) — 7-transmembrane proteiner, der aktiverer G-proteiner og videreføres til second messengers som cAMP eller Ca2+.
- Receptor-tyrosinkinaser (RTK) — membranreceptorer som dimeriserer og fosforylerer sig selv for at starte kaskader (fx insulinreceptoren).
- Ionkanal-koblede receptorer — åbner eller lukker ionkanaler ved ligandbinding og ændrer membranpotentialet hurtigt (bruges fx i nervesystemet).
- Nukleare receptorer — binder lipofile hormoner i cytoplasma eller kerne og regulerer genaktivitet.
Sekundære budbringere og kaskader
Når et receptorprotein aktiveres, overføres signalet ofte videre af sekundære budbringere — små, opløselige molekyler eller ioner, der forstærker og spreder signalet i cellen. Vigtige second messengers inkluderer:
- cAMP — syntetiseres af adenylylcyclase og aktiverer protein kinase A (PKA).
- Ca2+ — frigivet fra intracellulære depoter via f.eks. IP3-receptorer; binder calmodulin og aktiverer en række enzymer.
- IP3 og DAG — genereres af phospholipase C og henholdsvis frigiver Ca2+ og aktiverer protein kinase C (PKC).
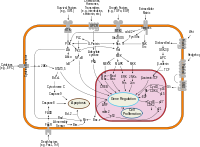
Disse budbringere sætter ofte gang i en kaskade af proteinkinaser, der fosforylerer downstream-proteiner. Et velkendt eksempel er MAPK-kaskaden, som kan føre til ændringer i cellecyklus og genekspression.
Forstærkning, hastighed og varighed
Signalforstærkning er et centralt træk: én aktiveret receptor kan aktivere mange G-proteiner eller kinaser, hvilket betyder, at en lille stimulus kan give et stort cellulært respons. Tidsmæssigt spænder signaltransduktion fra millisekunder (fx ionflux i synapser) til minutter eller timer (fosforylering af enzymer) og op til dage ved varige ændringer i genekspression.
Regulering, feedback og kryds-talk
Signalveje er ikke lineære rør; de indeholder feedforward- og feedback-mekanismer, inhibitoriske komponenter og mulighed for kryds-talk mellem veje. Post-translationelle ændringer som fosforylering, ubiquitinering og proteolyse regulerer signalstyrke og -varighed. Desuden sørger mekanismer som receptorinternalisering og desensibilisering for, at celler kan tilpasse deres følsomhed over for vedvarende stimuli.
Biologisk rolle og evolutionær betydning
I bakterier og andre encellede organismer begrænser de transduktionsprocesser, som en celle har, antallet af måder, hvorpå den kan reagere på sit miljø. I flercellede organismer anvendes mange forskellige signaltransduktionsprocesser til at koordinere de enkelte cellers adfærd. På denne måde organiseres organismens funktion som helhed. Jo mere kompleks organismen er, jo mere komplekst er det repertoire af signaltransduktionsprocesser, som organismen må besidde.
Disse systemer til kommunikation mellem celler er meget gamle og findes i alle metazoer. Evolutionært har genbrug og variation af samme grundlæggende signaltrin (receptor → second messenger → kinase → transkriptionsfaktor) skabt et mangfoldigt sæt reguleringsmuligheder.
Klinisk betydning og eksempler
Signaltransduktion er central i sundhed og sygdom. Fejl i signalveje kan føre til alvorlige sygdomme — derfor er mange lægemidler rettet mod komponenter i disse veje. Eksempler:
- Diabetes — defekt insulin-signalering (insulinreceptor/RTK) påvirker glukoseoptagelse og stofskifte.
- Hjertesygdomme — forstyrrelser i β-adrenerge GPCR-veje påvirker hjertefrekvens og kontraktilitet; β-blokkere er et eksempel på terapeutisk intervention.
- Autoimmunitet — dysreguleret cytokinsignalering kan føre til overaktivitet af immunsystemet.
- Kræft — mutationer i receptorer eller signalmolekyler (fx Ras, RTKs, kinaser) giver ofte ukontrolleret vækst; målrettede lægemidler inkluderer tyrosinkinaseinhibitorer og monoklonale antistoffer.
Eksempler på velundersøgte veje
- Insulin-signaling via PI3K-Akt-mTOR: regulerer glukoseoptag, proteinsyntese og celleoverlevelse.
- GPCR → adenylylcyclase → cAMP → PKA: vigtig i hormonrespons og neuronal kommunikation.
- RTK → Ras → Raf → MEK → ERK (MAPK-kaskade): styrer proliferation og differentiering.
Hvordan studeres signaltransduktion?
Forskere bruger en række metoder til at følge signalveje: biokemiske teknikker som western blot og immunoprecipitation, levende celle-imaging med fluorescerende rapportere (f.eks. GFP-fusioner eller FRET-baserede sensorer), massespektrometri til at identificere fosforyleringssteder og genetik/CRISPR til at undersøge funktionelle konsekvenser af mutationer.
Afsluttende bemærkninger
På celleniveau er signaltransduktion nødvendig for at kunne registrere både det ydre og det indre miljø og for at reagere passende. Mange sygdomsprocesser som f.eks. diabetes, hjertesygdomme, autoimmunitet og kræft skyldes fejl i signaltransduktionsvejene. Dette understreger den kritiske betydning af signaltransduktion for biologi og medicin.
Forståelse af signaltransduktion giver indsigt i cellulære beslutningsprocesser, muliggør udvikling af målrettede terapier og hjælper med at forklare, hvordan komplekse biologiske systemer koordineres på tværs af celler og væv.