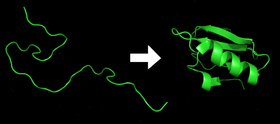
Proteinfoldning er den proces, hvorved et protein antager sin funktionelle tre-dimensionelle form eller konformation. Foldning er i høj grad en selvorganiserende proces: en lineær kæde af aminosyrer går fra en mere eller mindre tilfældig spole til en veldefineret struktur, som lige nøjagtigt gør proteinet i stand til at udføre sin biologiske funktion. De stabiliserende kræfter omfatter bl.a. hydrogenbindinger, hydrofobe interaktioner, ionbindinger, van der Waals‑kræfter og disulfidbånd.
Hvordan foregår foldningen?
- Et nyligt syntetiseret protein begynder som et ufoldet polypeptid – en lineær rækkefølge af aminosyrer dannet ved translation (mRNA → kæde). Denne ufoldede form mangler en fast tredimensionel struktur.
- Under foldningen interagerer aminosyrernes sidekæder og ryggrad med hinanden og med vandmiljøet omkring dem, hvilket fører til en specifik, stabil tredimensionel struktur. Den endelige struktur bestemmes i høj grad af aminosyresekvensen (se Anfinsens dogme), men processen påvirkes også af cellulære forhold, tilstedeværelsen af metalioner, cofaktorer og hjælpende proteiner.
Foldningen sker ikke nødvendigvis som et enkelt trin, men gennem mellemliggende tilstande (fx en "molten globule") og via et energilandskab, hvor folding kan beskrives som en tragt mod lavere fri energi. Dette forklare bl.a., hvordan et protein kan finde sin native form hurtigt trods astronomisk mange mulige konformationer (Levinthal‑paradokset).
De vigtigste drivkræfter og støttefaktorer
- Hydrofob effekt: Hydrofile (vandelskende) og hydrofobe (vandskyende) sidekæder sørger for, at hydrofobe rester typisk begraves i proteinets indre, hvilket er en vigtig drivkraft for sammenpakning.
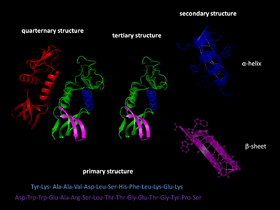
- Hydrogenbindinger: Stabiliserer sekundære strukturer som α‑helix og β‑sheet (hydrogenbindinger).
- Kovalente bindinger: Disulfidbånd mellem cysteiner kan låse dele af strukturen eksternt i nogle proteiner.
- Chaperoner og chaperoniner: Specielle hjælperproteiner (fx Hsp70‑familien, GroEL/GroES i bakterier) assisterer foldning, forhindrer sammenklumpning og kan hjælpe med korrekt foldning under stress eller når foldning er kompleks.
- Co‑translationel foldning: Mange proteiner begynder at folde allerede mens de syntetiseres på ribosomet, hvilket påvirker foldingens kinetik og rækkefølge.
Kvalitetskontrol i cellen
Cellen overvåger og håndterer ufoldede eller fejlfoldede proteiner via flere systemer:
- Endoplasmatisk retikulum (ER) kvalitetskontrol: Proteiner der foldes i ER, gennemgår fejlkontrol; mislykkede foldninger sendes ofte til ER‑associeret degradationssystem (ERAD).
- Proteasom og ubiquitinering: Fejlfoldede proteiner mærkes med ubiquitin og nedbrydes i proteasomet.
- Autofagi: Aggregater eller større strukturer kan fjernes via autofagi.
- Unfolded Protein Response (UPR): Et stressrespons som tilpasses når foldningskapaciteten i ER overskrides.
Fejlfoldning og sygdomme
Hvis proteiner ikke når eller ikke bevarer deres korrekte native form, mister de ofte funktion og kan blive giftige. Mange alvorlige sygdomme er forbundet med fejlfoldning og proteinaggregation:
- Amyloid‑sygdomme: Forkert foldede proteiner kan danne stabilt β‑foldede fibre (amyloider). Eksempler omfatter Alzheimers sygdom (β‑amyloid og tau), Parkinsons sygdom (α‑synuclein) og Huntingtons sygdom (polyglutamin‑aggregater).
- Prionsygdomme: Smitsomme, fejlfoldede prionproteiner kan inducere ændret foldning i normale proteinformer og forårsage neurodegeneration.
- Protein‑mangeltilstande pga. degradering: Nogle mutationer medfører at proteinet fejlfoldes og degraderes hurtigere, fx visse former for cystisk fibrose (CFTR‑mutationer), hvilket giver tab af funktion.
- Kardiomyopatier og systemiske amyloidoser: Fejlfoldede proteiner kan aflejres i væv og skade organfunktion.
Desuden spiller proteinstruktur en rolle i immunologi og allergier: Antistofgenkendelse afhænger af tredimensionelle epitoper, og immunsystemet reagerer forskelligt på forskellige konformationer, hvorfor foldning påvirker antigenicitet.
Naturens variation: intrinsisk uordnede proteiner
Ikke alle proteindele er faste, kompakte strukturer. Mange proteiner eller domæner er intrinsisk uordnede og kræver ikke en stiv, velordnet fold for at fungere — de kan være fleksible og interagere med flere partnere, hvilket er vigtigt i regulering og signalering.
Metoder til at studere foldning
Forskere undersøger proteinstruktur og foldning med en række metoder: röntgenkristallografi, NMR‑spektroskopi, cryo‑EM, cirkulær dichroisme (CD), fluorescens og single‑molecule teknikker (f.eks. smFRET), samt computermodellering og avancerede forudsigelsesværktøjer (fx AlphaFold). Kinetiske studier kan afsløre mellemtrin og foldningsveje.
Betydning og perspektiv
Forståelse af proteinfoldning er centralt for biologi, medicin og bioteknologi: det hjælper med at forklare sygdomsmekanismer, designe stabilere enzymer, udvikle farmaka, og forbedre produktion af terapeutiske proteiner. Fortsat forskning i foldningsmekanismer, chaperonsystemer og kvalitetssikring i cellen er vigtig for at bekæmpe foldningsrelaterede sygdomme og udnytte proteiner i anvendelser som industri og terapi.