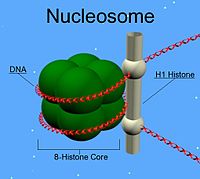
Nukleosomer er byggestenene i kromosomer. Hvert nukleosom består af et stykke DNA viklet omkring en kerne af histonprotein. Denne regelmæssige pakning af DNA i nukleosomer er grundlaget for kromatinets struktur og gør det muligt at komprimere det meget lange DNA-molekyle, så det kan være i cellekernen.
Struktur
Et klassisk nukleosom indeholder en histon-octamer bestående af to kopier hver af histonerne H2A, H2B, H3 og H4. Omkring denne octamer er cirka 147 basepar DNA viklet i omkring 1,65 omdrejninger. Mellem nukleosomerne ligger linker-DNA (typisk 10–80 basepar), og et ekstra histon, H1, binder ofte til linker-DNA og hjælper med at stabilisere højereordens pakkestrukturer.
Funktion
- Pakning: Nukleosomer tillader effektiv sammenfoldning af det lange DNA, så det passer i cellekernen.
- Beskyttelse: DNA bundet til histoner er delvist beskyttet mod skader og degradering.
- Regulering af genaktivitet: Placering og kemiske ændringer af histoner påvirker, hvor tilgængeligt DNA er for transkriptionsmaskineriet, og dermed om et gen er aktivt eller slukket. Dette er en central mekanisme i epigenetisk regulering (regulerer genernes funktion).
- Rolle ved celleprocesser: Ved celledeling, replikation og DNA-reparation skal nukleosomer ofte fjernes, flyttes eller genindsættes, så de ikke hindrer de nødvendige enzymer.
Regulering og dynamik
Nukleosomer er ikke statiske — de kan flytte sig langs DNA (sliding), blive delvist fjernet (eviction) eller få udskiftet histoner. Enzymer og komplekser, kaldet kromatinremodelleringskomplekser (fx SWI/SNF), samt histon-modificerende enzymer ændrer kromatinets tilgængelighed via post-translationelle modifikationer som acetylation, methylation, phosphorylierung og ubiquitination. Disse kemiske mærker udgør i praksis en "histonkode", der hjælper cellen med at afgøre, hvilke områder af genomet der skal være aktive.
Betydning for genregulering og sygdom
Nukleosomernes positionering nær promotorer og regulatoriske elementer påvirker transkriptionens start og styrke. Ændringer i histon-modifikationer eller i de maskiner, der håndterer nukleosomer, kan føre til forkert genregulering og er forbundet med sygdomme, herunder kræft. Derfor er en del lægemidler rettet mod histon-modificerende enzymer (fx HDAC-hæmmere) under udvikling eller i klinisk brug.
Hvordan studeres nukleosomer?
Forskere bruger teknikker som MNase-sekventering (MNase-seq) til at kortlægge nukleosomposition, ChIP-sekventering (ChIP-seq) til at identificere histonmodifikationer og avancerede strukturbestemmelsesmetoder (fx cryo-EM) til at se detaljerne i histon–DNA-interaktioner.
Samlet set er nukleosomer essentielle både for fysisk pakning af genomisk DNA og for reguleringen af adgangen til genetisk information — fra daglig genregulering i cellen til kritiske processer ved kromatin omorganisering og funktion i hele organismen.