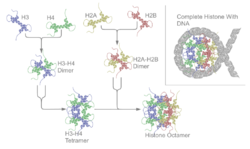
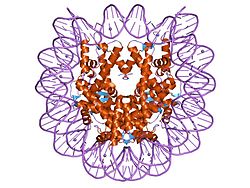
Histoner er proteiner, der findes i eukaryote cellekerner, og som pakker DNA'et ind i strukturelle enheder kaldet nukleosomer. De er de vigtigste proteinkomponenter i kromatin, den aktive komponent i kromosomerne.
Histoner fungerer som spoler, som DNA vikler sig rundt om, og spiller en rolle i genreguleringen. Uden histoner ville det afviklede DNA i kromosomerne være meget langt. F.eks. har hver menneskecelle ca. 1,8 meter DNA, men viklet om histonerne har den ca. 90 millimeter kromatin, som, når de duplikeres og kondenseres under mitosen, resulterer i ca. 120 mikrometer kromosomer.
Struktur og nukleosomer
Et nukleosom består af et histonkjerner — et otterprotein-kompleks dannet af to kopier hver af histonerne H2A, H2B, H3 og H4 — omkring hvilket cirka 147 basepar DNA er viklet. Mellem nukleosomer findes kortere stykker linker-DNA; til dette binder ofte histon H1, som hjælper med at stabilisere højere ordens samling af kromatin.
Den regelmæssige pakning af nukleosomer reducerer DNA-længden markant og danner grundlaget for videre foldning (tidligere omtalt som 30 nm-fiberen, som dog er genstand for løbende forskning) og for loop-strukturer, der organiserer kromatin i domenestrukturer i kernen.
Typer og varianter af histoner
- Kernehistoner: H2A, H2B, H3 og H4 — danner nukleosomets kerne.
- Linker-histon: H1 — binder til linker-DNA og påvirker kromatinets kompaktering.
- Histonvarianter: Der findes specialiserede varianter som H3.3, som ofte findes i aktivt transskriberet kromatin, og CENP-A, som er essentiel for centromerfunktion. Varianterne kan ændre nukleosomets stabilitet og funktion.
Histonmodifikationer og genregulering
Histoner har fleksible N-terminale "haler", som kan kemisk modificeres på mange måder. Disse post-translationelle modifikationer udgør et nøglesystem i genreguleringen og i epigenetisk kontrol.
De mest almindelige modifikationer omfatter:
- Acetylering (typisk på lysin): forbindes ofte med åben kromatin og transkriptionsaktivitet.
- Methylering (lysiner og argininer): kan være forbundet med enten aktivering eller repression afhængigt af positionen (fx H3K4me3 = aktivt, H3K27me3 = repressivt).
- Fosforylering: involveret i respons på signaler, celledeling og DNA-reparation.
- Ubiquitinering og andre mærkninger: påvirker kromatinstruktur og proteinudskiftning.
Disse mærker fungerer både ved at ændre den fysiske pakning af kromatin og ved at fungere som bindingssteder for effektorproteiner (læseproteiner), der fremmer eller hæmmer transskription. Kombinationen af forskellige modifikationer kaldes ofte for histonkoden.
Kromatin-remodellering og histoneudskiftning
Kromatin er dynamisk: ATP-afhængige remodelleringskomplekser (fx SWI/SNF, ISWI, CHD) kan flytte, fjerne eller omarrangere nucleosomer og derved ændre DNA-tilgængeligheden. Histon-chaperoner (fx CAF-1 og HIRA) hjælper med korrekt indsættelse og udskiftning af histoner under DNA-replikation, reparation og aktiv transkription.
Funktioner i replikation, DNA-reparation og udvikling
Under DNA-replikation bliver histoner delvist adskilt og fordelt mellem datterstrenge; nydannede histoner indsættes og modificeres, så kromatinets tilstand kan genskabes — en vigtig mekanisme for epigenetisk arv. Ved DNA-skader rekrutteres specifikke histonmodifikationer og remodeleringsfaktorer for at åbne eller lukke kromatin og tillade reparationsmaskineriet at virke.
I udvikling og celledifferentiering styrer histonmarkører hvilke gener, der er tilgængelige for transskription, og dermed celleidentitet.
Medicinsk betydning
Fejl i histonmodifikationer, mutationer i histongener eller dysfunktion i de enzymer, der skriver/aflæser/modificerer histoner, er impliceret i en række sygdomme, især kræft. Fx er onkogene oncohistoner (som mutationer i histon H3) og ændret aktivitet i histon-methyltransferaser eller histon-deacetylaser dokumenterede mekanismer i tumordannelse. Terapier, der målretter histon-modificerende enzymer (fx HDAC-hæmmere, EZH2-hæmmere), bruges eller udvikles som behandlingsstrategier.
Afsluttende bemærkninger
Histoner er således ikke bare passive "spoler" — de er aktive regulatorer af genomets funktion. Gennem deres struktur, varianter og modifikationer kontrollerer de adgang til den genetiske information, påvirker cellefunktion, arv af epigenetiske tilstande og spiller en central rolle i sundhed og sygdom.