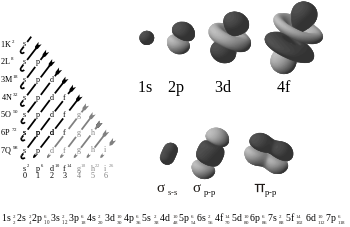
I kemi er pi-bindinger (π-bindinger) kovalente kemiske bindinger, hvor to atomorbitaler overlapper side om side i stedet for direkte langs forbindelsesaksen. I praksis dannes π-bindinger oftest ved sidestillet overlap mellem to p-orbitaler, så elektronernes fordelingsform har to lober over og under bindingsaksen (se billede). Der opstår to separate overlapningsområder — en over og en under aksen — og et af orbitalernes knudeplaner (en nodalplan) går gennem begge de involverede kerner.
Dannelse og orbitalsymmetri
Det græske bogstav π i navnet henviser til p-orbitalernes oprindelse. Orbitalsymmetrien for en π-binding ligner p-orbitalens form, når man ser ned langs bindingsaksen: der er et nodalplan indeholdende aksen, og elektronfordelingen ændrer fortegn på hver side af dette plan. Når to p-orbitaler overlapper sideværts, dannes en bindende π-orbital og en antibindende π*-orbital i molekylorbitalbeskrivelsen.
Sammenligning med sigma-bindinger
π-bindinger er normalt svagere end sigma-bindinger, fordi p-orbitalernes parallelle orientering giver mindre orbitaloverlap end hoved-i-hoved-overlapningen i σ-bindinger. Kvantemekanikken forklarer denne forskel ved, at mindre overlap betyder lavere bindingsenergi. Alligevel bidrager π-bindinger væsentligt til en multipelbindings samlede styrke og giver samtidig kortere bindinger end tilsvarende enkeltbindinger.
Pi-binding i dobbelt- og tripelbindinger
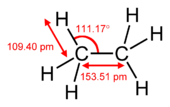
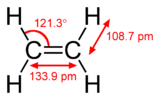
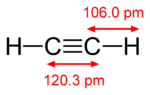
I en almindelig dobbeltbinding består forbindelsen af én σ- og én π-binding (fx i ethylen, H2C=CH2). I en tripelbinding findes én σ-binding og to π-bindinger, hvor de to π-orbitaler ligger vinkelret på hinanden (fx i ethyn, HC≡CH). Elektroner, der indgår i π-bindinger, kaldes ofte pi-elektroner. Molekylære fragmenter, der er forbundet med en π-binding, kan ikke frit rotere omkring denne binding uden at bryde π-overlappet; rotation vil ødelægge de parallelle p-orbitalers faseforhold og dermed π-bindingens stabilisering. Denne rotationshæmning er årsag til geometrisk stereoisomeri (cis/trans) omkring dobbeltbindinger.
Konjugation, delokalisering og aromatisme
Når π-bindinger optræder vekslende med enkeltbindinger i en kæde (konjugation), kan π-elektronerne blive delokaliserede over flere atomer. Delokalisering sænker systemets energi og giver særlige elektroniske egenskaber, fx nedsat reaktivitet mod visse typer reaktioner og karakteristiske absorptionsbånd i UV-vis spektre (π→π* overgange). I cykliske, planære systemer med (4n+2) π-elektroner opstår aromatisme, hvor delokaliserede π-elektroner giver ekstra stabilitet (Hückels regel) — benzol (C6H6) er et klassisk eksempel.
Reaktivitet og spektroskopi
π-elektroner er generelt mere tilgængelige for reagenser end σ-elektroner, fordi de ligger højere i energi og er mere spredte. Derfor er π-bindende systemer typisk de steder, hvor elektrofiler angriber (fx elektrofilt additionsangreb på alkeners dobbeltbinding). Spektroskopisk kan π→π* og n→π* elektronovergange observeres i UV-vis og infrarøde frekvenser kan vise karakteristiske absorptionsbånd for C=C- og C≡C-grupper.
Pi-bindinger og d-orbitaler
Udover p-orbitaler kan også d-orbitaler deltage i π-lignende bindinger, særligt i komplekser med overgangsmetaller. Her taler man om π-donation (fra ligand til metal) og π-backbonding (fra metal til ligand), begge vigtige for metal–ligand-kemi. I forbindelse med hypervalens har man historisk antaget d-orbitalinvolvering i nogle centrale atomer; moderne teoretiske studier viser dog, at graden af d-orbitalbidrag varierer og ofte er mindre end først antaget.
Konsekvenser for struktur og eksempler
- Geometri: π-bindinger kræver orthogonalt orienterede p-orbitaler — derfor er et alkens carbon-atom sp2-hybridiseret og planært.
- Stereokemi: Manglende frit rotationsrum omkring π-bindinger fører til cis/trans-isomeri ved dobbeltbindinger.
- Eksempler: Ethylen (H2C=CH2), ethyn (HC≡CH), benzol (C6H6) og konjugerede diener som butadien.
- Molekylorbitaler: Pi-bindende orbitaler danner også antibindende π*-orbitale, som er vigtige i fotokemi og reaktivitet — excitation til π* kan gøre en binding svagere eller brydes.
Sammenfattende er π-bindinger en central type kovalent binding, der bestemmer mange molekylers elektroniske egenskaber, reaktivitet og tredimensionelle form. Forståelse af π-systemer er derfor afgørende i organisk kemi, materialekemi og koordinationskemi.