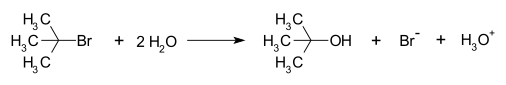
SN1-reaktionen er en substitutionsreaktion i organisk kemi. "SN" står for nukleofil substitution, og "1" repræsenterer det faktum, at det hastighedsbestemmende trin kun involverer ét molekyle (unimolekylært). Reaktionen foregår typisk via et karbokationsintermediat og kan ses ved solvolyse af alkylhalogenider eller ved substitution af protonerede alkoholer under sure betingelser.
Mekanisme — trin for trin
SN1-mekanismen beskrives ofte i to hovedtrin:
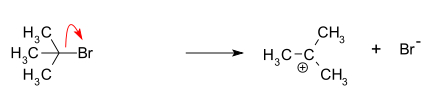
- Trin 1 (langsommere, hastighedsbestemmende): Leaving group (f.eks. Cl–, Br–) dissocierer fra substratet og danner et positivt ladet karbokation. Dette trin er unimolekylært, derfor afhænger reaktionshastigheden kun af koncentrationen af substratet (rate = k[substrat]).
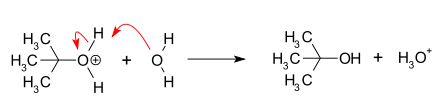
- Trin 2 (hurtigt): Nukleofilen angriber det planare karbokation og danner substitutionsproduktet. I mange tilfælde angriber opløsningsmidlet (solvolyse), hvilket leder til produkter som alkoholer eller ethers.
Kinetik og eksperimentelle kendetegn
- Hastighedsudtryk: rate = k[substrat] (første ordens kinetik).
- Reaktionshastigheden er uafhængig af nukleofilens koncentration i det hastighedsbestemmende trin.
- Polar protiske opløsningsmidler (f.eks. vand, alkohol) fremmer SN1 ved at stabilisere ioner og overgangstilstanden gennem solvatisering.
Hvad påvirker om en reaktion går via SN1?
- Substratets struktur: Stabiliserede karbokationer favoriserer SN1. Tertiære > sekundære >> primære. Primære substrater gennemgår normalt SN2-reaktion i stedet.
- Afgangsgroups evne: En god leaving group (svag base, f.eks. I–, Br–) fremmer dissociation.
- Opløsningsmiddel: Polar protisk opløsningsmiddel stabiliserer karbokationer og anioner og fremmer SN1.
- Nukleofilens styrke: Har mindre effekt på hastigheden end i SN2; selv svage nukleofiler (f.eks. opløsningsmidlet) kan reagere efter karbokationets dannelse.
- Temperatur og koncentration: Højere temperatur øger typisk reaktionshastigheden; høj substratkoncentration øger hastigheden (første ordens afhængighed).
Stereokemi
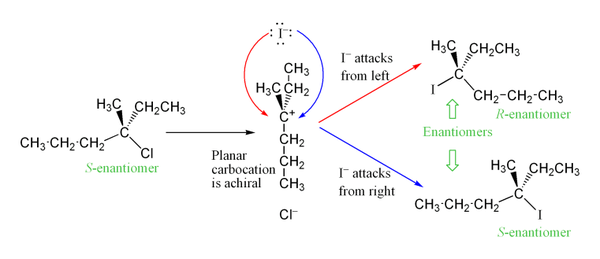
Da karbokationen er planart (sp2-hybridiseret), kan nukleofilen angribe fra begge sider, hvilket ofte giver racemisering ved spormolekyler med chirale centre. Dog kan der forekomme delvis retention af stereokemi, hvis nukleofilen angriber inden fuldstændig separation af ionpar (ion-pair effekt) eller hvis der er tæt ion-par (solvent-separated ion pair vs. intimate ion pair).
Karbokationer og rearrangementer
Karbokationer kan undergå internal omlejring for at danne mere stabile kationer (f.eks. hydrid- eller alkylskift). Disse rearrangementer ændrer ofte produktets struktur og er et vigtigt kendetegn ved SN1-mekanismer — især ved sekundære karbokationer, der kan omdannes til tertiære karbokationer.
Sammenligning med SN2
- SN1: unimolekylær hastighedsbestemmende trin, karbokationintermediat, favoriseres af tertiære substrater og polar protiske opløsningsmidler.
- SN2: bimolekylær enkelttrin (nukleofilangreb og leaving group fraspaltning samtidigt), favoriseres af primære substrater og stærke nukleofiler i polar aprotiske opløsningsmidler.
Eksempler
- Tert-butylchlorid i vand: tert-butylchlorid hydrolyserer hurtigt til tert-butanol gennem SN1 (dissociation til tert-butylkarbokation efterfulgt af vandangreb).
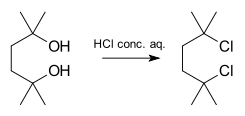
- Protonerede sekundære eller tertiære alkoholer under sure forhold kan undergå substitution til give alkylhalider eller andre substituerede produkter — dette ses ofte i dehydratisering og substitutionsreaktioner af alkohol. Se også eksempler med sekundære eller tertiære alkoholer.
- Many solvolyses of benzylic and allylic halides følger SN1, da de resulterende karbokationer er rezonansstabiliserede.
Beviser og historisk note
Kinetiske målinger (første ordens afhængighed), isolerede eller spektroskopisk observerede karbokationer og studier af stereokemiske resultater understøtter SN1-mekanismen. Blandt uorganiske kemikere er SN1-reaktionen ofte kendt som den dissociative mekanisme. Christopher Ingold et al. foreslog først reaktionsmekanismen i 1940, og siden da er mekanismen blevet grundigt undersøgt og udbygget.
Praktiske overvejelser
- Ved syntese vælges SN1 ofte, når man ønsker substitution på tertiære centre eller når nukleofilen er svag.
- For at undgå uønskede rearrangementer eller racemisering kan alternative reaktionsbetingelser eller reaktionsveje (f.eks. SN2 eller brug af beskyttelsesgrupper) overvejes.
Sammenfattende er SN1 en central mekanisme i organisk kemi, karakteriseret ved dannelsen af karbokationer, første ordens kinetik og en række praktiske implikationer for reaktionsudfald og produktfordeling.