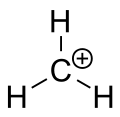
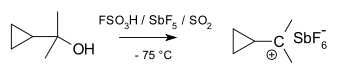
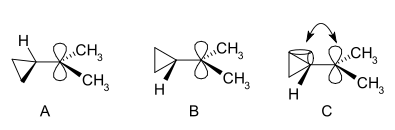
En karbokation er en ion med et positivt ladet kulstofatom. Det ladede kulstofatom mangler to valenselektroner og beskrives ofte som en "sekstet" – det har altså kun seks elektroner i sin ydre valensskal i stedet for de ideelle otte ifølge oktetreglen. Derfor er karbokationer generelt reaktive, fordi de søger at udfylde oktetten og genvinde neutralitet.
Struktur og hybridisering
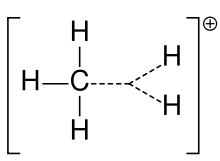
I de fleste tilfældes foretrækker et karbokation en trigonal plan struktur med geometri svarende til 3sp²-hybridisering: tre sigma-bindinger ligger i et plan, og der er en tom, uhybridiseret p-orbital vinkelret på dette plan, hvor den positive ladning kan være delokaliseret. På trods af at man formelt kan tegne en enkelt positiv ladning på kulstoftet, viser eksperimenter og beregninger, at reaktiviteten og elektronfordelingen bedst forklares med sp²-hybridisering og en tom p-orbital.
Faktorer, der påvirker stabiliteten
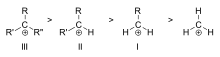
- Substitutionsgrad: Tertiære karbokationer stabiliseres mere end sekundære og primære på grund af hyperkonjugation og induktive donation fra alkylgrupper.
- Hyperkonjugation: Overlap mellem fyldte C–H sigma-orbitaler på nabogrupper og den tomme p-orbital stabiliserer kationen.
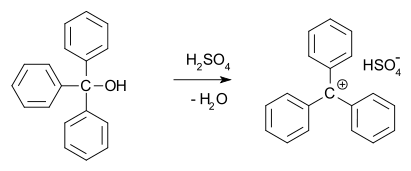
- Resonansstabilisering: Allyl- og benzylic-karbokationer er stærkt stabiliserede, fordi ladningen kan delokaliseres over et π-system.
- Induktive effekter: Elektron-donorer øger stabiliteten; elektrontrækkende grupper reducerer den.
- Solvent- og modion-effekter: Polære, protiske opløsningsmidler og svage eller svært koordinende modioner (f.eks. i super-sure medier) kan forlænge karbokationers levetid.
Dannelsesveje
- Ionisering af alkylhalider (SN1) – f.eks. ved opvarmning i polært opløsningsmiddel.
- Protonering af alkener eller alkoholer (syrekatalyserede additioner).
- Elektrofil addition til dobbeltbindinger, hvor en positivt ladet mellemliggende karbokation dannes.
- Fragmentering i massepektrometri og i visse eliminationsreaktioner.
Reaktivitet og almindelige reaktionstyper
Karbokationer er kraftige elektrofile mellemprodukter. De mest almindelige reaktioner er:
- Nukleofil angreb: Et nukleofilt reagent binder sig til det positive kulstof (eksempel: SN1-reaktioner).
- Elimination: Afgang af proton fra nabokulstof kan give alken (E1-reaktion).
- Rearrangementer: Hydrid- eller alkylskift (f.eks. 1,2-hydridshift) forekommer ofte for at danne mere stabile karbokationer.
- Additioner til π-systemer: I polyreagerende systemer kan karbokationer deltage i videre kædevækst eller ringdannelser.
Særlige tilfælde
- Benzylic og allyliske karbokationer: Disse er stærkt stabiliserede via resonans og er vigtige i mange synteser.
- Non-classical karbokationer: Eksempler som 2-norbornyl-kationen har delokaliseret ladning gennem brokoblede bindinger (debatteret historisk, men anerkendt i mange tilfælde).
- Superelektrofile forhold: I super-sure medier kan meget ustabile karbokationer isoleres og karakteriseres ved lav temperatur og specielle teknikker.
Observation og karakterisering
- NMR: Karbokationernes tilstedeværelse kan bekræftes ved karakteristiske kemiske skift; i nogle tilfælde identificeres metalstabilisede eller solvaterede kationer ved lavtemperatur NMR.
- IR/UV-Vis: Mindre direkte, men kan hjælpe ved konjugerede systemer.
- Trapping-eksperimenter: Reagerer man karbokationen hurtigt med en valgt nukleofil, kan produktet afsløre kationets struktur.
- Teoretiske beregninger: DFT og andre metoder bruges rutinemæssigt til at bestemme geometrier, energier og ladningsfordeling.
Betydning i organisk syntese
Karbokationer er centrale i mange klassiske reaktioner som Friedel–Crafts-alkylering, syrekatalyserede additions- og eliminationsreaktioner samt i mekanismer for SN1- og E1-processer. Evnen til at kontrollere kationens dannelse og skæbne (f.eks. undgå rearrangement) er ofte nøglen til selektiv syntese.
Kort opsummering: Karbokationer er kortelevende, elektronfattige intermediater med trigonal plan geometri og en tom p-orbital. Deres stabilitet bestemmes af hyperkonjugation, resonans, induktive effekter og omgivende medier, og deres høje reaktivitet gør dem både udfordrende og nyttige i organisk kemi.