Ædelgasserne er en gruppe af grundstoffer, der alle er gasser. Disse grundstoffer er alle i gruppe 18 i det periodiske system. De er alle monoatomære, hvilket betyder, at hvert molekyle består af et enkelt atom. De reagerer næsten aldrig med andre grundstoffer. Det skyldes, at de har en fuld ydre elektronskal (normalt 8 elektroner i yderste skal — undtagen helium, som har 2 i 1s-skallen). Der findes seks ædelgasser:
Grundlæggende fysiske egenskaber
Alle ædelgasser er ved almindeligt tryk og temperatur farveløse, lugtfrie og monoatomære gasser. Deres smelte- og kogepunkter stiger generelt, når man går ned gennem gruppen (fra helium mod radon), og deres atomradius og densitet øges tilsvarende. Elektronkonfigurationen kan skrives som ns2 np6 for de fleste (fx argon 3s2 3p6), mens helium er 1s2.
Forekomst i atmosfæren
Alle disse gasser findes i luft, men i meget varierende mængder. Ædelgasser udgør tilsammen ≈0,96 % af atmosfæren, hvor argon er den dominerende (~0,93 %). De øvrige forekommer i spormængder (fx neon og helium i få ppm-til-10'ere ppm, krypton og xenon i lavere ppm-områder). Radon forekommer kun i spor og er kortlivet, da det er radioaktivt.
Kemiske egenskaber og undtagelser
Ædelgassernes lave reaktivitet skyldes deres lukkede elektronkonfiguration, som gør dem stabilt elektronisk "udfyldte". Alligevel er gruppens inaktivitet ikke absolut:
- Xenon danner en række stabile forbindelser med kraftige oxidationsmidler — fx fluorider (XeF2, XeF4, XeF6) og oxider (XeO3, XeO4) — som blev fremstillet første gang i midten af 1900-tallet.
- Krypton kan danne enkelte forbindelser, fx KrF2 under kraftige forhold.
- Argon er normalt inert, men der er eksperimentelt fremstillet forbindelser som ArH+ i plasma og særlige matrix-forsøg, og der er rapporteret om Ar–F–H (HArF) stabiliseret ved meget lave temperaturer i matrixeksperimenter.
- Neon og helium danner praktisk talt ingen normale kemiske forbindelser under standardbetingelser. Dog er der ved ekstreme tryk eksperimentelt og teoretisk fundet eksotiske forbindelser: f.eks. blev et salt-lignende Na2He påvist teoretisk og eksperimentelt under meget højt tryk (2017), hvilket viser, at også disse "inerteste" atomer kan indgå i stabile enheder under usædvanlige forhold.
- Radon kan forventes at danne kemiske forbindelser (fx fluorider) men studier er begrænsede pga. dets radioaktivitet og kortere halveringstid.
Generelt øges muligheden for kemisk binding ned gennem gruppen, dels pga. lavere ioniseringsenergi og dels pga. relativistiske effekter i de tungeste atomer.
Anvendelser
Ædelgasser har mange tekniske og kommercielle anvendelser:
- Helium: køling (f.eks. til superconducting magneter i MR-scannere), ballon- og luftskibsgas, blande gasser til dykkermix (heliox), læse- og laboratoriebrug under inert atmosfære.
- Neon: lysrør og skilte (neonlys) — karakteristisk rød-orange emission i udladningsrør.
- Argon: bruges som beskyttende atmosfære ved svejsning og i produktion af metaller, fyldgas i glødelamper og ved opbevaring af luftfugtfølsomme materialer.
- Krypton: anvendes i visse typer fotolamper, i belysning og i nogle lasertyper; bruges også til isolering i nogle højisolerende ruder.
- Xenon: brugt i fotoblisser, kraftige gasudladningslamper, nogle bil-forlygter (HID), og som drivgas i ionmotorer til rumbåde; xenon har også været brugt som inhalationsanæstetikum i medicin.
- Radon: pga. radioaktivitet har det få praktiske anvendelser; det kendes mest som en sundhedsrisiko i lukkede bygninger, hvor radon fra undergrunden kan ophobe sig.
Farver i udladningsrør
Når ædelgasserne anvendes i kolde katoderør (gasudladningsrør) til at producere lys, har de hver især karakteristiske emissioner og derved forskellige farver i rørene. Radon bruges normalt ikke til belysning på grund af sin radioaktivitet. Herunder vises billeder af nogle af gasserne i udladningsrør:
· 
Helium
· 
Neon
· 
Argon
· 
Krypton
· 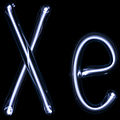
Xenon
Det tungeste medlem og nye elementer
Ununoctium (grundstof 118) er sandsynligvis den næste ædelgas efter radon, fordi det er den næste boks i samme gruppe. Den har dog en halveringstid på 0,89 ms i den oprindelige omtale, hvorefter den henfalder til Ununhexium (element 116). Det betyder, at dens anvendelse sandsynligvis er begrænset. Bemærk, at det midlertidige navn "Ununoctium" senere er blevet erstattet af det officielle navn og symbol (oganesson, Og), men eksperimentelle data er meget begrænsede og viser, at tunge 'ædelgas'-elementer kan få afvigende egenskaber pga. relativistiske effekter.
Historie
Ædelgasser blev opdaget gennem slutningen af 1800-tallet. Lord Rayleigh (John William Strutt) og Sir William Ramsay opdagede og identificerede nye, inerte gasser i atmosfæren; argon blev formelt identificeret i 1894, og Ramsay opdagede senere neon, krypton og xenon i 1898. Helium blev først observeret i solens spektrum i 1868, og isoleret på Jorden i 1895. Rayleigh modtog Nobelprisen i fysik i 1904 og Ramsay modtog Nobelprisen i kemi samme år, begge anerkendelse for deres arbejde med disse nye gasser.
Sikkerhed og sundhed
De fleste ædelgasser er forholdsvis ufarlige kemisk, men kan udgøre en kvælningfare i lukkede rum, da de kan fortrænge luftens ilt. Radon er undtagelsen: som radioaktiv gas udgør den en betydelig sundhedsrisiko ved indånding og er en kendt årsag til lungekræft; radonmåling og -afhjælpning i bygninger er derfor vigtig i mange områder. Håndtering af flydende ædelgasser (fx flydende helium) kræver særlige sikkerhedsforanstaltninger pga. ekstremt lave temperaturer.