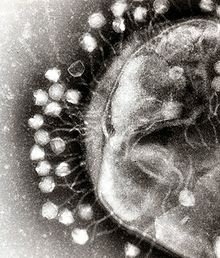
En bakteriofag (ofte kaldet en phage) er et virus, der inficerer bakterier. Bakteriofager er blandt de mest almindelige og mest forskelligartede biologiske enheder i biosfæren. Ligesom virus, der inficerer eukaryoter (fx planter, dyr og svampe), findes fager i mange former og med mange forskellige funktioner.
Struktur
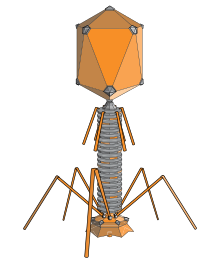
Mange bakteriofager har en karakteristisk opbygning med et ydre proteinskrog (kapsid), som indeholder fagets genetiske materiale. Kapsidet kan være icosahedrisk — det vil sige bestå af 20 trekantede flader og 30 kanter — og sidde øverst på en hale med benlignende fibre, som fagen bruger til at binde sig til bakterien. Andre fager kan have filamentøs eller kompleks morfologi og nogle mangler hale helt.
Fager består typisk af et ydre proteinskellet, og deres genetiske materiale kan være enkeltstrenget eller dobbeltstrenget DNA eller RNA (ssDNA, dsDNA, ssRNA eller dsRNA). Genomerne spænder bredt i størrelse — fra kun nogle få tusinde nukleotider til flere hundrede tusinde basepar — og kan være cirkulære eller lineære. Typiske størrelser ligger ofte mellem 20 og 200 nanometer i fysisk diameter, afhængigt af typen.
Genom og gener
Faggenomer kan være meget små og kode for så få som fire gener, eller de kan kode for hundredvis af gener. Generne kan instruere produktionen af kapsidproteiner, halestrukturer, replikationsenzymer og proteiner, der nedbryder bakterievæggen ved frigivelse. Nogle fager bærer også gener, som kan ændre bakteriens egenskaber (f.eks. toksinproduktion eller antibiotikaresistens) ved horisontal genoverførsel.
Livscyklus
Livscyklussen starter, når fagen binder sig til specifikke receptorer på bakteriens overflade ved hjælp af sine halefibre. Derefter injicerer fagen sit genom ind i værtscellen. De to hovedtyper af cyklus er:
- Lytisk cyklus: Fagens genom overtager bakteriens maskineri til at producere nye fagpartikler. Når nye virioner er samlet, producerer fagen ofte enzymer (fx endolysin), der svækker bakterievæggen, så cellen lyserer og frigiver de nye fager.
- Lysogen (temperat) cyklus: Nogle fager integrerer deres genom i bakteriens kromosom som et prophage. Her ligger fagens DNA latent og replikeres sammen med værts-DNA'et uden at dræbe cellen. Under visse forhold kan et prophage aktivere sig selv og gå ind i den lytiske cyklus.
Fagets livscyklus kan også føre til transduktion, hvor bakterielt DNA overføres fra én bakterie til en anden via en fag, hvilket er en vigtig mekanisme for horisontal genoverførsel.
Økologi og udbredelse
Fager findes overalt, hvor bakterier findes — i jord, fersk- og havvand, i dyrs tarme og i miljøer som biofilm. De er særligt talrige i marine miljøer: der er fundet op til 9×10 8virioner pr. milliliter i mikrobielle måtter ved overfladen, og op til 70 % af havbakterierne kan være inficeret af fager. Fager spiller en central rolle i økosystemernes stofkredsløb ved at dræbe bakterier og frigive organisk materiale (den såkaldte viral shunt), hvilket påvirker kulstof- og næringsstofcyklusser.
Studie og påvisning
Forskere studerer fager ved hjælp af forskellige metoder:
- Elektronmikroskopi til at visualisere virionernes struktur (Helmut Ruska var tidligt aktiv inden for dette felt).
- Pladevækst- og plaque-assays til at kvantificere og isolere lytiske fager.
- Metagenomisk sekventering for at kortlægge fagdiversitet i miljøprøver.
Historie
Fager blev opdaget i begyndelsen af 1900-tallet, og deres medicinske potentiale blev udforsket allerede for over 90 år siden. I det tidligere Sovjetunionen, Centraleuropa og enkelte steder i Frankrig har man traditionelt anvendt fag (fagterapi) som alternativ til antibiotika. Den sande natur af fager blev klart dokumenteret, da Helmut Ruska observerede dem i elektronmikroskopet i 1939.
Medicinsk og industriel anvendelse
Fagterapi og fagbaserede produkter vinder fornyet interesse på grund af stigningen i antibiotikaresistente bakteriestammer. Anvendelser omfatter:
- Direkte fagterapi: Brug af lytiske fag eller fagcocktails til at dræbe sygdomsfremkaldende bakterier hos mennesker, dyr eller planter. Fordele er høj specificitet (rammer kun målbakterier) og evnen til at formere sig ved infektionsstedet. Udfordringer inkluderer snæver værtsrange, udvikling af fagresistens og regulatoriske krav.
- Fagafledte enzymer: Endolysiner og depolymeraser, som nedbryder bakterievægge og biofilm, anvendes som antimikrobielle midler og til desinfektion.
- Biokontrol i fødevareindustrien: Fager og endolysiner bruges til at reducere bakteriel forurening i fødevarer og på overflader.
- Diagnostik og forskning: Phage display til antigen- og antistofopdagelse, samt anvendelse af fager som biosensorer.
Bakteriers forsvar og fagresistens
Bakterier udvikler flere forsvarsmekanismer mod faginvasion, herunder:
- CRISPR–Cas-systemer, som genkender og nedskærer fremmed DNA.
- Restriktions–modifikationssystemer, som kløver ikke-methyleret fremmed DNA.
- Ændringer i overfladereceptorer, så fag ikke længere kan binde sig.
På samme tid udvikler fager modforsvar, fx anti-CRISPR-proteiner, hvilket fører til en konstant evolutionsmæssig armsrace mellem fager og bakterier.
Kliniske og praktiske overvejelser
Selvom fagterapi har lovende resultater i flere studier, er udbredt klinisk anvendelse begrænset af behovet for:
- grundige sikkerheds- og effektstudier (randomiserede kontrollerede forsøg),
- standardiserede fremstillingsmetoder og kvalitetskontrol,
- strategier til at modvirke fagresistens (fx fagcocktails eller kombinationsterapier),
- regulatoriske rammer for godkendelse.
Særlige roller — biofilm og sygdom
Nogle fager kan være med til at nedbryde biofilm, hvilket hjælper med at bekæmpe persistente infektioner. Modsat kan andre fager fremme biofilmdannelse eller overføre gener, der styrker bakteriers evne til at danne biofilm — et problem i forbindelse med lungebetændelse, cystisk fibrose og kroniske sår, hvor biofilm beskytter bakterier mod lægemidler og immunsystemet.
Sammenfattende er bakteriofager nøgleaktører i mikrobiel økologi, molekylærbiologi og bioteknologi. De udgør både muligheder — fx som alternative antimikrobielle midler og biokontrol-agenter — og udfordringer, fx gennem deres rolle i genoverførsel og interaktioner med biofilm.