Inden for kemi og fysik forklarer atomteorien, hvordan vores forståelse af atomet har ændret sig gennem tiden. Engang troede man, at atomer var de mindste dele af stof. Nu ved man imidlertid, at atomer består af protoner, neutroner og elektroner. Disse subatomare partikler består af kvarker. Den første idé om atomet kom fra den græske filosof Demokrit. Mange af idéerne i den moderne teori kom fra John Dalton, en britisk kemiker og fysiker.
Teorien gælder for faste stoffer, væsker og gasser, men den gælder ikke på samme måde som for plasmaer eller neutronstjerner.
Historisk udvikling
- Antikken: Demokrit foreslog idéen om udelelige partikler — «atomos» — som byggesten i alting.
- 1800-tallet — Dalton: John Dalton formulerede en videnskabelig atommodel: elementer består af ensartede atomer, elementernes atomer har fast masse, og kemiske forbindelser dannes ved sammensætning af atomer.
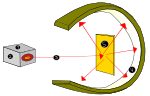
- Slutningen af 1800-tallet — elektronen: Eksperimenter med katodestråler førte til opdagelsen af elektronen (J. J. Thomson), som viste, at atomet ikke var udeleligt.
- 1911 — Rutherford: Geiger og Marsden udførte guldfolie-eksperimentet under Rutherford, hvilket viste, at atomets positive masse er koncentreret i en lille kerne.
- 1913 — Bohr: Niels Bohrs model introducerede kvantiserede elektronbaner for at forklare spektrallinjer.
- 1920'erne — kvantemekanik: Schrödingers bølgefunktion og Heisenbergs matrixmekanik gav en probabilistisk model af elektrontæthed og orbitaler.
- 1930'erne: James Chadwick opdagede neutronen, og opdagelsen af kvarker senere viste, at protoner og neutroner selv er sammensat af endnu mindre partikler.
Atomets opbygning og størrelse
Et atom består af en central kerne (nukleus) med protoner og neutroner, omgivet af en sky af elektroner. Antallet af protoner i kernen (atomnummeret) bestemmer grundstoffet, mens summen af protoner og neutroner (masse tallet) afgør isotopen. Atomer har typisk en størrelse i området 0,1–0,5 nanometer (10⁻¹⁰–10⁻¹⁰ m), mens kerner er ~10⁻¹⁵ m (femtometer) – altså mange størrelsesordener mindre.
Protoner og neutroner består af kvarker bundet sammen af gluoner via den stærke kernekraft. De vigtigste kræfter i atomet er:
- Elektromagnetisk kraft: styrer tiltrækning mellem protoner og elektroner og bestemmer kemiske egenskaber.
- Stærk kernekraft: holder kvarkerne sammen i protoner og neutroner og binder nukleoner i kernen.
- Svag kraft: involveret i radioaktive henfaldsprocesser.
Moderne kvantemekanisk forståelse
Den moderne model beskriver elektroner som bølgefunktioner, hvor sandsynligheden for at finde en elektron i et område afgøres af orbitalernes form og kvantetal. Grundlæggende begreber omfatter:
- Orbitaler: regioner med høj sandsynlighed for elektrontæthed (s, p, d, f osv.).
- Elektronkonfiguration: måde elektroner er fordelt på orbitalerne; den bestemmer atomets kemiske reaktivitet og placering i det periodiske system.
- Pauli-eksklusionsprincippet: ingen to elektroner i et atom kan have samme sæt kvantetal, hvilket forklarer opbygningen af elektronisk struktur i grundstoffer.
- Spektroskopi og fotoner: emission og absorption af lys ved bestemte energiskift beviser kvantiserede energiniveauer.
Isotoper, ioner og nuklear fysik
Isotoper er varianter af samme grundstof med forskelligt antal neutroner; nogle isotoper er ustabile og gennemgår radioaktivt henfald. Ioner dannes, når et atom mister eller optager elektroner, hvilket ændrer ladningen og ofte kemisk opførsel.
Nuklear fysik studerer kernebinding, masse-defekt og bindingsenergi — principper der forklarer, hvorfor masse kan omdannes til energi i kernereaktioner (fission og fusion).
Anvendelser og begrænsninger
- Teknologi og industri: forståelsen af atomer ligger til grund for materialeforskning, halvledere, nanoteknologi og kemisk syntese.
- Energi og medicin: kernenergi, medicinsk billeddannelse og stråleterapi bygger på atomare og nukleare principper; radioisotoper bruges til diagnostik og behandling.
- Forskning: partikelacceleratorer og spektroskopi afdækker stadig finere detaljer om subatomare processer og kræfter.
- Begrænsninger: Ved høje temperaturer og ioniseringsgrader (som i plasmaer) gælder ikke længere klassiske atommodeller direkte, og i ekstremt kompakte objekter som neutronstjerner kan stof antage former, hvor individuelle atomer ikke længere eksisterer som sådan (f.eks. neutronrigt eller degenere materie, evt. kvark-materie under ekstreme forhold).
Afsluttende bemærkninger
Atomteorien er et resultat af århundreders observationer og eksperimenter og har udviklet sig fra enkle modeller til en kompleks, kvantemekanisk forståelse. Modellerne, vi bruger i dag, er ekstremt succesfulde til at forudsige kemiske og fysiske fænomener i almindelige forhold, men forskningen fortsætter for at udforske grænsetilfælde og dybere lag af materiens opbygning.