En cycloaddition er en kemisk reaktion mellem reaktanter med dobbeltbindinger, der erstattes af en ringstruktur. Det er en pericyklisk kemisk reaktion, hvor "to eller flere umættede molekyler (eller dele af det samme molekyle) kombineres med dannelse af et cyklisk addukt, hvor der sker en nettoreduktion af bindingsmultipliciteten". Det er en cykliseringsreaktion: den laver ny ring af atomer.
Cycloadditioner er navngivet efter grundstørrelsen af de molekyler, der samles. Dette ville gøre Diels-Alder-reaktionen til en [4 + 2]cycloaddition og 1,3-dipolar cycloaddition til en [3 + 2]cycloaddition. Denne type reaktion er en upolær additionsreaktion.
Mekanisme og karakteristika
De fleste cycloadditioner foregår ved en koncerted mekanisme: to nye sigmabindinger dannes samtidigt i et enkelt, stereospecifikt overgangstrin uden isolerbare intermediater. Reaktionen er drevet af overlapningen af π-orbitaler, og derfor spiller orbital-symmetri (f.eks. Woodward–Hoffmann-reglerne) en central rolle for, om en given cycloaddition er tilladt termisk eller fotokemisk.
- Koncerted vs. stepwise: Selvom mange cycloadditioner er concerted, kan nogle forløbe via stepwise-mekanismer med radikal- eller ioniske mellemtrin, især under visse betingelser eller med særligt substituerede substrater.
- Termisk vs. fotokemisk: Orbital-symmetri bestemmer, hvilke cycloadditioner er termisk tilladt (fx [4+2] Diels–Alder) og hvilke ofte kræver fotokemisk excitation (fx mange [2+2] cycloadditioner).
Orbital-symmetri og Woodward–Hoffmann
Woodward–Hoffmann-reglerne forklarer hvilke pericykliske processer, der er symmetri-allowed. For eksempel er en [4+2] (Diels–Alder) termisk tilladt, idet begge komponenter kan reagere suprafacialt. En [2+2] cycloaddition er termisk ofte forbudt (på grund af fasemodifikation af π-orbitalerne), men bliver tilladt ved fotokemisk excitation, som ændrer orbitalbesætningen.
Typer af cycloadditioner (udvalgte)
- Diels–Alder ([4+2]): Reaktion mellem en 1,3-dien og en alken (dienofil). Ofte meget nyttig til at skabe seksledede ringe. Klassisk eksempel: butadien + ethen → cyclohexen-derivat; mere praktisk: maleinsyreanhydrid + cyclopentadien → endo-cycloaddukt.
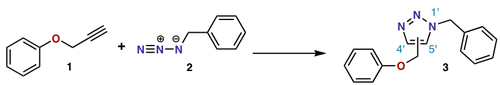
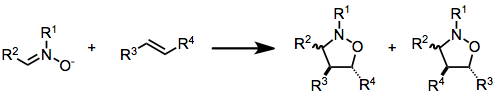
- 1,3-dipolar cycloaddition ([3+2]): En 1,3-dipol (f.eks. nitrone, azid) reagerer med en dipolarofil (fx en alken eller alkyn) og danner femledede ringe. Et vigtigt eksempel er azid-alkyn cycloaddition (Huisgen), som ved Cu(I)-katalyse bliver særligt effektiv og regioselektiv (”click”-reaktion).
- [2+2] cycloaddition: Danner fireledede ringe (cyclobutaner). Termisk ofte forbudt, men fotokemisk tilladt.
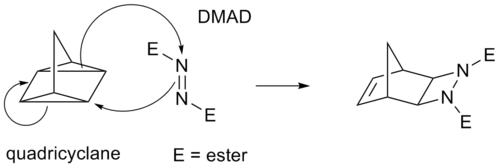
- Inverse electron demand Diels–Alder: En variant hvor diene er elektronfattige og reagerer med elektronrige dienofiler (fx tetraziner reagerer hurtigt med alken- eller alkin-donorer).
Stereokemi, regiokontrol og endo/exo
Cycloadditioner er ofte højt stereospecifikke: konfigureringen af substituenter på reaktanterne overføres direkte til produktet. Regioselektivitet afhænger af elektroniske og steriske effekter (HOMO/LUMO-komplementaritet). I Diels–Alder-reaktioner er der ofte en endo/ exo-selektivitet; endo-produktet favoriseres ofte kinetisk på grund af sekundære orbitalinteraktioner (fx maleinsyreanhydrid + cyclopentadien).
Katalyse og reaktionsbetingelser
- Lewis-syre-katalyse: Koordination af en Lewis-syre til dienofilen sænker dens LUMO og øger reaktionens hastighed og ofte selektiviteten.
- Solvent og temperatur: Polære opløsningsmidler og temperatur kan påvirke hastighed og pathways (termisk vs. fotokemisk). Mange Diels–Alder-reaktioner kræver opvarmning, mens [2+2] ofte kræver UV-lys.
- Asymmetrisk katalyse: Chiral katalyse (organokatalyse eller metal-baserede chiral Lewis-syrer) gør det muligt at få høj enantioselektivitet i cycloadditioner.
Anvendelser
Cycloadditioner er fundamentale i organisk syntese og anvendes til at konstruere komplekse ringstrukturer i naturlige produkter, farmaka og materialer. Diels–Alder er et vigtigt værktøj i totalsynteser, og 1,3-dipolar cycloaddition (især CuAAC) er central i biokonjugering og materialekemi.
Eksempler
- Maleinsyreanhydrid + cyclopentadien → bicyklisk produkt med stor endo-selectivitet (klassisk Diels–Alder).
- Azid + terminal alkyn → 1,2,3-triazol (Huisgen 1,3-dipolar cycloaddition). Cu(I)-katalyse giver næsten udelukkende 1,4-regioisometret (”click chemistry”).
- Fotokemisk [2+2] mellem to alkener → cyclobutan-derivat (bruges i syntese og fotoskrivning af polymerer).
Begrænsninger og undtagelser
Ikke alle kombinationer leder til cycloaddition; elektroniske mismatch, sterisk hindring eller orbital-symmetri kan forhindre reaktionen, og nogle systemer favoriserer stepwise pathways eller konkurrerende side‑reaktioner. Valg af katalysator, opløsningsmiddel og temperatur kan ofte overvinde sådanne problemer.
Samlet set er cycloadditioner en kraftfuld klasse af reaktioner i organisk kemi, kendetegnet ved effektiv ringdannelse, høj stereokontrol og brede anvendelsesmuligheder i syntese og materialer. For mere detaljerede eksempler og mekanistiske studier kan man se litteraturen om Diels–Alder, 1,3-dipolare cycloadditioner og Woodward–Hoffmann-reglerne.
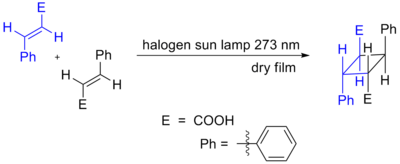
.png)
![Intermolecular Formal [3+3] Cycloaddition Reaction](https://www.alegsaonline.com/image/600px-3+3-cycloaddition.svg.png)