I organisk kemi sker en additionsreaktion, når to molekyler mødes for at danne et større molekyle. Dette kan kun ske, når et af molekylerne allerede har en dobbelt- eller trippelbinding. Der kan være tale om kulstof-kulstof-bindinger eller endda kulstof-ilt, kulstof-kvælstof og andre. Det ene af de to molekyler kaldes nukleofil, og det er det molekyle, der giver elektronerne til det andet for at skabe den nye binding. Det andet molekyle kaldes elektrofilen, og det er det, der får elektronerne.
En additionsreaktion er det modsatte af en eliminationsreaktion. Almindelige eksempler på additionsreaktioner er addition af vand på tværs af en dobbeltbinding og nukleofilt angreb på en carbonyl.
Mekanismer og hovedtyper
Additionsreaktioner kan forløbe via flere forskellige mekanismer afhængigt af reaktanter og betingelser. De vigtigste typer er:
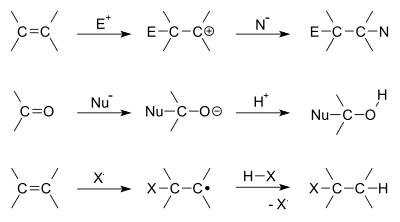
- Elektrofil addition: En elektrofil (f.eks. H+, Br+) angriber en π-binding, hvilket ofte danner en positivt ladet mellemform (f.eks. et carbokation) eller en cyclic halonium-ion. Et nukleofil angriber derefter det positive center og danner produktet. Eksempel: hydrohalogenering (addition af HBr) til alkener.
- Nukleofil addition: Særligt almindelig ved carbonylgrupper (C=O). En nukleofil (f.eks. hydride, alkoxid, grignard-reagens) angriber det elektronegative carbon i carbonylen og danner et alkoxidanion, som ofte protoneres senere. Eksempel: dannelsen af alkohol ved angreb af en R-MgBr på en aldehyd/keton.
- Radikal addition: Radikaler tilføjes til π-systemer, typisk initieret ved varme eller lys. Bruges fx i fri radikal polymerisation af alkenmonomerer.
- Concerted cykloaddition (pericykliske reaktioner): Addition sker i én trin uden separate ladede mellemformer, f.eks. Diels–Alder-reaktionen (4+2 cykloaddition).
Regio- og stereokemi
- Regioselektivitet: Hvor på dobbeltbindingen substituenterne rammer. For eksempel følger mange elektrofile additioner alkener Markovnikov-reglen: hydrogen binder sig til det kulstof med flest hydrogenatomer i forvejen, og elektrofilen til det andet kulstof. Undtagelser: anti-Markovnikov-additioner (fx hydroboration-oxidation af alken giver anti-Markovnikov-produkt; HBr i nærvær af peroxider giver også anti-Markovnikov).
- Stereoselektivitet: Additioner kan være syn (begge atomer binder fra samme side af dobbeltbindingen) eller anti (fra modsatte sider). Eksempler: katalytisk hydrogenation giver typisk syn-addition; halogenation (Br2) går gennem en bromonium-ion og fører til anti-addition mellem bromatomerne.
- Carbocation-rearrangementer: Ved mekanismer med carbokationer kan rearrangementer (hydride- eller alkylvandring) forekomme, hvilket ændrer produktets struktur.
Typiske eksempler og korte mekanismeoversigter
- Hydrering af alkener (acid-katalyseret): H+ addere til dobbeltbindingen → carbokation → vand angriber → protonoverførsel → alkohol. Ofte følger Markovnikov-selectivitet.
- Hydrohalogenering (HBr, HCl): H+ danner carbokation → halidion angriber. Peroxider kan ændre forløbet og give anti-Markovnikov-produkt via radikal mekanisme.
- Halogenation (Br2, Cl2): Dannelsen af en halonium-ion (f.eks. bromonium) efterfølges af nukleofilt angreb fra modsatte side → anti-addition.
- Katalytisk hydrogenation (H2, metalkatalysator som Pd/C): H-atomer adsorberes på metaloverfladen og addere simultant til samme side af dobbeltbindingen → syn-addition og mættet produkt (alkane).
- Hydroboration-oxidation: BH3 addere syn til alkenen, giver organoborane; oxidation med H2O2/HO– giver alkohol med anti-Markovnikov regiokontrol og syn-stereokemi.
- Nukleofil addition til carbonyl: Reaktioner med grignardreagenser, hydridreduktioner (NaBH4, LiAlH4) eller dannelse af cyanohydriner. Karakteriseret ved dannelsen af alkoxidanioner, som senere protoneres til alkoholer eller relaterede produkter.
- Fri radikal polymerisation: Initiation danner radikal, som addere til alkens π-system og starter kædevækst — vigtig industriel anvendelse af additionsreaktioner.
Katalyse, betingelser og kinetik
Additionsreaktioner kan fremmes af syrer, baser, metal-katalysatorer eller radikalinitiativer (lys, peroxider). Kinetisk set afhænger reaktionsordenen af den specifikke mekanisme: elektrofile additioner kan vise blandede ordener (fx hastighedsbestemmende trin er ofte angreb af elektrofilen), mens bimolekylære radikaladditioner kan følge andenordens kinetik. Temperatur, opløsningsmiddel og koncentrationer påvirker også regiokontrol og tendensen til rearrangementer.
Betydning og anvendelser
- Fremstilling af alkoholer, halogenforbindelser, aminer og andre funktionelle grupper.
- Polymerisation (f.eks. produktion af polyethylen, polypropylen) baseret på gentagen additionsreaktion af alkenmonomerer.
- Syntetisk opbygning af komplekse molekyler i farmaceutisk og materialekemi.
Praktiske tips til genkendelse
- Søg efter reaktanter med π-bindinger (C=C, C≡C eller C=O) og en anden reagent, der kan fungere som nukleofil eller elektrofil.
- Overvej om reaktionen kan give carbokation eller haloniumion — dette forudsiger ofte stereokemi (syn vs anti) og om rearrangement er muligt.
- Vælg betingelser (syre, base, radikalinitiator, metal) ud fra ønsket regiokemi og stereokemi.
Samlet set er additionsreaktioner en af de mest centrale reaktionstyper i organisk kemi, fordi de tillader opbygning af nye bindinger og funktionelle grupper på forudsigelige måder. For dybere forståelse kan man studere specifikke mekanismer (f.eks. elektrofilt additionsforløb med overgangstilstande eller orbitalsymmetri i pericykliske additioner) og gennemgå eksperimentelle eksempler og spektroskopiske data (NMR, IR) for at bestemme produktstruktur og stereokemi.