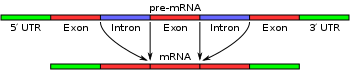
RNA-splejsning er en fase i gentranskriptionen. Messenger RNA (mRNA), som overfører koden fra DNA til proteiner, opbygges i to faser.
I den første fase oversættes hvert gen til et præ-mRNA. Derefter forbindes exonerne i præ-mRNA'erne ved splejsning, som foregår i splejsosomerne.
Det er nødvendigt, fordi genet er opdelt i kodeafsnit, kaldet exoner, og ikke-kodede afsnit, kaldet introner. Exonerne samles ved splejsning.
I molekylærbiologi er splejsning altså en proces, hvor introner fjernes og exoner sammenføjes. Dette giver det endelige mRNA. Dette messenger-RNA bruges derefter til at producere et korrekt protein ved hjælp af translation.
Hvordan foregår splejsning mekanisk?
Splejsning sker i et stort ribonukleoprotein-kompleks kaldet splejsosomet. Splejsosomet består af små nukleære ribonukleoproteiner (snRNP'er) og mange hjælpende proteiner. De hyppigst involverede snRNP'er betegnes U1, U2, U4, U5 og U6.
Processen kan kort beskrives i to transesterificeringsreaktioner:
- Først genkender snRNP'er specifikke signalsekvenser ved intronets begyndelse (ofte med et 5'-GU) og ved en intern branch point (ofte et adenin, "A").
- En nukleofil angreb fra branch point‑A på 5'-splice‑stedet skaber en lariat‑struktur (en "løkke").
- Derefter forbindes de to exoner via en anden transesterificering, intronet fjernes som en lariat, og de to exoner sammensmeltes til et kontinuerligt mRNA-segment.
Vigtige signaler i præ-mRNA
For at splejsning skal ske præcist, kræver maskineriet flere kortfattede sekvenselementer i RNA:
- 5'-splice-site (ofte starter med GU),
- branch point (et A-nukleotid omgivet af en bestemt kort sekvens),
- polypyrimidin‑tract før 3'-splice-site, og
- 3'-splice-site (ofte slutter med AG).
Alternative splejsnings betydning
Alternative splejsning betyder, at ét præ-mRNA kan splejses på forskellige måder, så forskellige kombinationer af exoner indgår i det modne mRNA. Det er en vigtig mekanisme til at øge organismers proteindiversitet uden at øge antallet af gener.
Typer af alternativ splejsning omfatter blandt andet:
- Exon-skipping (et exon udelades),
- Mutually exclusive exons (enten‑eller valg mellem exoner),
- Alternative 5' eller 3' splice‑sites (forkortelse eller forlængelse af eksontætheder),
- Intron retention (et intron bevares i det modne mRNA).
Regulering af splejsning
Splejsningsvalg styres af en række proteiner og regulatoriske RNA'er:
- SR-proteiner fremmer brugen af bestemte splice-sites.
- hnRNP'er kan hæmme eller ændre splejsningsmønstre.
- Transkriptionshastighed, kromatinstruktur og co‑transkriptionel rekruttering af splejsningsfaktorer påvirker også, hvilke exoner der inkluderes.
Fejl i splejsning og sygdom
Mutationen i splice‑sites eller i regulerende factorers gener kan føre til fejl i splejsning og sygdom. Kendte eksempler:
- Spinal muskelatrofi (SMA): mutationer i SMN1 genet påvirker snRNP-sammensætning; behandling med antisense-oligonukleotider (fx Spinraza) kan ændre splejsning i SMN2 og forbedre sygdomsforløb.
- Beta-thalassæmi: mange tilfælde skyldes splice-site-mutationer i beta-globin-genet, som fører til defekt hæmoglobin.
- Splejsningsfejl og ændret splejsningsmønster ses ofte i kræft, hvor de kan skabe onkogene isoformer eller slå tumorhæmmere fra.
Andre varianter og biologisk betydning
Udover det store, almindelige splejsosom findes et minoritært splejsosom, som genkender en mindre gruppe introner med lidt forskellige konsensussekvenser (fx U11/U12 snRNP'er). Mindre fejl eller ændringer i disse systemer kan have betydelige biologiske konsekvenser.
Sammenfattende er RNA-splejsning en central proces i molekylærbiologien, der sikrer korrekt sammensætning af mRNA og samtidig giver cellen fleksibilitet til at generere flere proteinvarianter fra samme gen. Kendskab til splejsningens mekanismer er afgørende for forståelsen af mange biologiske processer og sygdomme og udgør et vigtigt felt for terapeutisk udvikling.