Orthomyxoviridae (orthos, græsk for "lige"; myxa, græsk for "slim") er en familie af RNA-vira, karakteriseret ved at være enveloped og have et segmenteret, negativ-sense enkeltkædet RNA-genom. De omfatter fem slægter: Influenzavirus A, Influenzavirus B, Influenzavirus C, Thogotovirus og Isavirus. De tre første slægter indeholder vira, der forårsager influenza hos hvirveldyr, herunder fugle (se også fugleinfluenza), mennesker og andre pattedyr. Isavirus inficerer laks (forårsager infektiøs lakse-anæmi); Thogotovirus inficerer hvirveldyr og hvirvelløse dyr — vektorer er ofte ektoparasitter som tæger, selvom beslægtede fund også er rapporteret i andre arthropoder (f.eks. myg og sølus).
Genom og struktur
Orthomyxoviridae har et segmenteret, negativ-sense RNA-genom. Segmenteringen gør det muligt for vira i samme vært at udveksle genomsegmenter (reassortment), hvilket især er vigtigt for influenza A og er en mekanisme bag store genotypiske ændringer (antigenic shift). Generelt gælder:
- Influenza A og influenza B har typisk otte RNA‑segmenter.
- Influenza C har normalt syv segmenter og adskiller sig ved at udtrykke et enkelt overfladeprotein med både receptorbinding og enzymatisk aktivitet (HEF i stedet for separate HA og NA).
- Isavirus og thogotovirus har også segmenterede genomer, men antal og organisering varierer mellem arter.
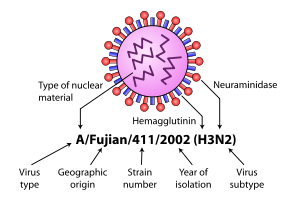
Virionerne er envelopede og ofte pleomorfe (varierende form), med overfladiske glykoproteinspidser. Influenza A og B udtrykker hemagglutinin (HA) og neuraminidase (NA) som de vigtigste overfladeantigener; influenza C har et fælles hemagglutinin-esterase-fusion (HEF)-protein.
Replikationscyklus
Orthomyxoviridae replikerer usædvanligt i værtscellens cellekerne. Centrale træk i replikationen:
- Indtrængning via receptor‑medieret endocytose og fusion af viral membran med endosommembranen.
- Transskription af negativ-sense genom til mRNA udføres af et viruskodet RNA-afhængigt RNA-polymerasekompleks (f.eks. PB2, PB1, PA hos influenza A/B).
- Virus benytter en "cap‑snatching"-mekanisme: polymerasen skærer 5'-cap-strukturer fra værts-mRNA og bruger dem som primers til viral mRNA-syntese.
- Ny syntese af genomisk vRNA og proteiner fører til samling af nukleokapsider, som transporteres ud af kernen og pakkes i membranbærende virioner ved afsnøring fra værtscellens plasmamembran.
- Non-strukturelle proteiner som NS1 modvirker værts immunsvar (f.eks. interferonrespons).
Slægter og værtsspektrum
- Influenzavirus A: Naturligt reservoir i vandfugle; kan krydse artsbarrierer til pattedyr (f.eks. svin, hest, sæl, menneske). Influenza A er årsag til epidemier og pandemier pga. både antigenic drift og shift. Subtyper defineres af kombinationen af HA- og NA‑typer (f.eks. H1N1, H5N1).
- Influenzavirus B: Primært humant patogen med mindre grad af dyrehostsammenblanding; står for sæsonmæssige influenzaepidemier men ikke pandemier på samme måde som A.
- Influenzavirus C: Forårsager typisk mildere luftvejsinfektioner hos mennesker og nogle andre pattedyr; antigenisk struktur og genom adskiller sig fra A og B.
- Thogotovirus: Fundet hos dyr og vektorer; nogle arter er vektorassocierede (typisk tæger) og kan i sjældne tilfælde forårsage sygdom hos mennesker og dyr.
- Isavirus: Inkluderer det patogene virus der giver infektiøs lakse-anæmi (ISA) hos opdrættet atlantisk laks, hvilket har stor betydning for akvakulturindustrien.
Kliniske manifestationer og epidemiologi
Hos mennesker spænder sygdomsbilledet fra asymptomatisk eller milde luftvejsinfektioner til svære influenzasygdomme med feber, hoste, myalgi og risiko for komplikationer som sekundær bakteriel lungebetændelse og akut respiratorisk svigt. Højrisikogrupper omfatter ældre, spædbørn, gravide og personer med kroniske sygdomme.
Influenza A's evne til reassortment mellem fugle, svin og mennesker gør den særlig vigtig i zoonoseovervågning; overvågning af dyrepopulationer (One Health-tilgang) er central for at opdage nye stammer med pandemipotentiale.
Isavirus hos laks fører til anæmi, blødninger, ascites og høj dødelighed i inficerede bestande; spredning i akvakultur forebygges med streng biosikkerhed og kontrolforanstaltninger.
Diagnose, behandling og forebyggelse
- Diagnose: RT‑PCR på respiratoriske prøver er den mest brugte metode for influenza hos mennesker; hurtig antigen-test, virusdyrkning og serologi anvendes også. For isavirus anvendes molekylær diagnostik og histopatologi.
- Behandling: Primært understøttende. Antiviraler inkluderer neuraminidase‑hæmmere (f.eks. oseltamivir, zanamivir) for influenza A og B; resistens kan forekomme. M2‑hæmmere (amantadin, rimantadin) er stort set ineffektive mod mange moderne stammer pga. resistens.
- Forebyggelse: Sæsonvaccination mod influenza A og B (inaktiverede eller levende, svækkede vacciner) anbefales til prioriterede grupper. Infektionskontrol, handhygiejne, hosteetikette og overvågning i både menneske- og dyrepopulationer er vigtige. I akvakultur anvendes biosikkerhed, overvågning og i nogle tilfælde smittebegrænsende foranstaltninger som destruktion af inficerede bestande.
Samfunds‑ og forskningsmæssige perspektiver
Orthomyxoviridae er af stor betydning for folkesundhed og økonomi — influenzaepidemier medfører betydelig sygelighed og dødelighed, mens sygdomme som infektiøs lakse‑anæmi påvirker fødevareproduktionen. Fortsat forskning i virusbiologi, antiviraler, bredspektrede vacciner og overvågningssystemer (herunder genetisk sekventering af cirkulerende stammer) er afgørende for at reducere sygdomsbyrden og opdage nye trusler tidligt.