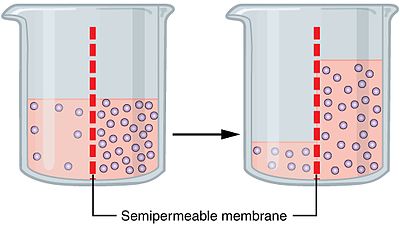
Osmose (/ɒzˈmoʊ.sɪs/) er bevægelsen af opløsningsmiddelmolekyler (typisk væske såsom vand) gennem en membran fra en opløsning til en anden uden påvirkning af en ydre mekanisk kraft. Kort sagt sker osmosen som et resultat af forskelle i koncentration af opløste stoffer på hver side af en semipermeabel membran: opløsningsmidlet bevæger sig mod den side, der har en højere koncentration af opløste partikler (og dermed en lavere koncentration af opløsningsmidlet), indtil en ligevægt eller et andet modtryk opnås.
Mekanisme
Den semipermeable membran slipper normalt små, upolære molekyler (som vand i stor udstrækning kan krydse) igennem, men blokerer større eller ladede opløste stoffer. Molekylerne bevæger sig i tilfældige termiske bevægelser; nettoresultatet er en vandstrøm mod den side med flest opløste partikler. Denne bevægelse mindsker forskellen i kemisk potentiale mellem siderne. I levende celler sker dette både som simpel diffusion gennem lipidlaget og gennem særlige vandkanaler kaldet aquaporiner, som tillader hurtig transport af vand uden at større opløste ioner følger med.
Osmotisk tryk
Det osmotiske tryk er det ydre tryk, der skal påføres for at forhindre nogen nettobevægelse af opløsningsmiddel gennem membranen. Osmotisk tryk er en colligativ egenskab: den afhænger af antallet af opløste partikler pr. volumen, ikke af deres kemiske art. For ideale, fortyndede opløsninger kan den omtrentlige sammenhæng beskrives af van ’t Hoffs lov:
Π ≈ i·C·R·T
- Π = osmotisk tryk
- i = van ’t Hoff-faktor (antal partikler ét opløst stof deler sig i)
- C = molær koncentration af opløste partikler
- R = gaskonstanten
- T = absolut temperatur (kelvin)
I praksis kan ikke-ideelle forhold, ioniske interaktioner og membranens partikelpermeabilitet gøre sammenhængen mere kompleks. Osmotisk tryk måles ofte i pascal (Pa) eller atmosfærer (atm).
Typer af opløsninger og cellulære konsekvenser
Man beskriver ofte miljøet omkring en celle som:
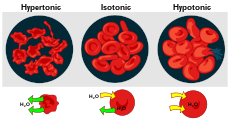
- Isotonisk: samme osmotiske tryk som cellens indre — der er ingen netto vandbevægelse.
- Hypotonisk: omgivelserne har lavere koncentration af opløste stoffer — vand bevæger sig ind i cellen, hvilket kan føre til opsvulmning eller i dyriske celler lysere (sprængning).
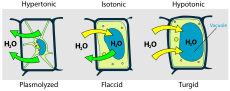
- Hypertonisk: omgivelserne har højere koncentration af opløste stoffer — vand bevæger sig ud af cellen, hvilket kan føre til skrumpning eller plasmolyse i planteceller.
I planter giver osmose turgortryk i cellerne, som hjælper planten med at opretholde stivhed og vækst. I dyr og mennesker reguleres cellevolumen og væskebalance gennem osmoregulerende mekanismer i nyrer, hjerne og hormonelle systemer (fx antidiuretisk hormon).
Biologisk betydning og eksempler
Osmose er central for mange biologiske processer:
- Optagelse og udskillelse af vand i celler og organer — fx nyrernes koncentration af urin.
- Transport af næringsstoffer og opretholdelse af ionbalancer i blod og væv.
- Planteceller bruger osmose til at opbygge turgor, som giver mekanisk støtte.
- Fødevareprocesser og cellekultur: forkert salt- eller sukkerkoncentration kan dræbe celler via osmose.
Aquaporiner er eksempler på membranproteiner, der regulerer vandpermeabilitet og dermed hastigheden af osmose i mange celletyper. I nogle organismer bruges osmotiske principper også som energikilde eller signalmekanisme.
Anvendelser og eksperimentelle metoder
Osmose udnyttes teknisk og medicinsk:
- Omvendt osmose er en filtreringsteknik, hvor et eksternt tryk overgår det osmotiske tryk og presser opløsningsmidlet (fx frisk vand) gennem en membran fra en koncentreret opløsning til den anden side — anvendt til vandrensning.
- Medicin: intravenøse væsker vælgeres med omhu (isotoniske vs. hypotoniske) for at undgå skadelig osmose i patientens celler.
- Laboratoriemetoder: osmometre og U-rør med semipermeable membraner bruges til at demonstrere og måle osmose og osmotisk tryk.
Begrænsninger og særlige forhold
Virkelige biologiske systemer afviger fra idealmodellen: opløsninger kan være ikke-ideelle, membraner kan have varierende selektivitet, og celler kan aktivt transportere ioner (energi-krævende processer) for at modvirke eller skabe osmose. Derfor skal man altid overveje både passive (osmose) og aktive transportmekanismer, når man analyserer væskebalance i levende organismer.
Samlet set er osmose et grundlæggende fysisk-kemisk fænomen, som forklarer mange dagligdags og biologiske processer fra plantevækst til nyrernes funktion og teknikker som vandrensning via omvendt osmose. Forståelse af osmosens mekanismer og begrænsninger er afgørende i biologi, medicin og teknik.