Tryptofan: essentiel aromatisk aminosyre – funktioner, kilder og serotonin
Lær om tryptofan — en essentiel aromatisk aminosyre, dens funktioner, kostkilder og rolle som forløber for serotonin og melatonin for bedre humør og søvn.
Tryptofan (Trp eller W) er kodet af kodonet UGG. Det er en α-aminosyre, der anvendes i biosyntesen af proteiner.
Tryptofan har en α-aminogruppe (som er i -NH3+ form under biologiske forhold) og en α-carboxylsyregruppe (som er i den deprotonerede -COO− form under biologiske forhold). Den har også en sidekæde indol, hvilket gør den til en upolær aromatisk aminosyre. Tryptofan er essentielt for mennesker: kroppen kan ikke syntetisere det, så det skal hentes gennem kosten.
Tryptofan er også en forløber for neurotransmitterne serotonin og melatonin.
Funktioner og biologisk betydning
- Proteinsyntese: Som en af de 20 standardaminosyrer indbygges tryptofan i proteiner og påvirker struktur og funktion, bl.a. via sin aromatiske indolring.
- Neurotransmitter- og hormonforløber: Tryptofan omdannes enzymatisk til 5-hydroxytryptofan (5-HTP) og videre til serotonin, som er vigtig for humør, appetit og søvn. Serotonin kan videre omdannes til melatonin i pinealkirtlen, der regulerer døgnrytmen.
- Kynureninvejen: Størstedelen af kroppens tryptofan nedbrydes via kynureninvejen, som fører til metabolitter som kynureninsyre (har neurobeskyttende egenskaber) og quinolinsyre (kan være neurotoksisk) samt syntese af NAD+ (et centralt koenzym i energimetabolismen).
- Immunregulation: Enzymer som indoleamin-2,3-dioxygenase (IDO) aktiveres under inflammation og øger nedbrydningen af tryptofan; dette kan hæmme bakterier og regulere T-celleaktivitet.
Metabolisme (kort)
- Tryptofan → (tryptophanhydroxylase) → 5-HTP → (aromatisk L-aminosyredecarboxylase) → serotonin.
- Serotonin → (N-acetyltransferase) → N-acetylserotonin → (hydroxyindol-O-methyltransferase) → melatonin.
- Tryptofan → (IDO eller TDO) → N-formylkynurenin → kynurenin → videre til kynureninsyre, quinolinsyre og NAD+.
Kilder i kosten
Fordi kroppen ikke kan lave tryptofan, er et varieret kostindtag nødvendigt. Fødevarer med relativt højt indhold af tryptofan omfatter:
- Fjerkræ (f.eks. kalkun, kylling)
- Æg og mejeriprodukter (mælk, yoghurt, ost)
- Fisk og skaldyr
- Sojaprodukter og andre bælgfrugter
- Nødder og frø (f.eks. chia, sesam, mandler)
- Havre, fuldkorn og bananer
- Mørk chokolade
Absorption og blod-hjerne-barrieren
Tryptofans adgang til hjernen begrænses af konkurrerende store neutrale aminosyrer (LNAA: fx valin, leucin, isoleucin, phenylalanin, tyrosin). Det er forholdet mellem tryptofan og disse LNAA (Trp/LNAA), der bestemmer hvor meget tryptofan der transporteres ind i hjernen. Kulhydratindtag kan indirekte øge Trp/LNAA-forholdet ved at udløse insulin, som fremmer optagelsen af mange LNAA i musklerne, men ikke tryptofan (da det er bundet til albumin), og dermed øge hjernens tryptofantilgængelighed.
Mangel, klinisk betydning og symptomer
- Mangel på tryptofan i kosten kan påvirke proteinsyntese og føre til lavere produktion af serotonin og melatonin, hvilket kan vise sig som søvnforstyrrelser, ændret humør og appetitændringer.
- Hvis både tryptofan og niacin (vitamin B3) mangler i kosten, kan kroppen have svært ved at danne nok niacin via kynureninvejen, hvilket kan bidrage til pellagra-lignende symptomer (dermatitis, diarré, demens).
- Øget nedbrydning af tryptofan via IDO under inflammation kan bidrage til træthed og humørpåvirkninger ved kronisk sygdom.
Kosttilskud og sikkerhed
- Tryptofan fås som kosttilskud og bruges nogle gange til støtte ved søvn- og humørproblemer. Evidensen er blandet; nogle studier viser effekt ved søvnforbedring og mildt nedsat angst/humørforstyrrelser, mens andre ikke gør.
- Interaktions- og sikkerhedshensyn: Kombinering af højdosis tryptofan med selektive serotoningenoptagshæmmere (SSRI), MAO-hæmmere eller andre serotonerge lægemidler kan øge risikoen for serotonin-syndrom — en alvorlig tilstand. Derfor bør man altid konsultere læge, især ved medicinsk behandling eller i graviditet/ammende.
- Almindelige bivirkninger ved høje doser omfatter kvalme, mavebesvær og døsighed.
Anbefalinger
Det daglige behov varierer med alder, vægt og fysiologisk tilstand. En ofte citeret minimumsanbefaling fra FAO/WHO er omkring 4 mg tryptofan pr. kg kropsvægt pr. dag som et estimat for at dække behov og understøtte proteinsyntese, men individuelle behov kan variere. En varieret kost med tilstrækkelige proteinkilder dækker normalt behovet i vestlige kostmiljøer.
Opsummering
- Tryptofan er en essentiel aromatisk aminosyre med en indol-sidekæde, indkodet af UGG, og indgår i proteiner.
- Det er forløber for vigtige signalstoffer som serotonin og melatonin, samt for metabolitter i kynureninvejen og NAD+-syntese.
- Fødevarer som fjerkræ, æg, mejeriprodukter, fisk, bælgfrugter, nødder og fuldkorn er gode kilder.
- Balance mellem tryptofan og andre store neutrale aminosyrer påvirker hjernens optagelse og dermed signalstofsyntese.
- Kosttilskud kan hjælpe i nogle tilfælde, men bør bruges med forsigtighed pga. interaktioner og bivirkninger.
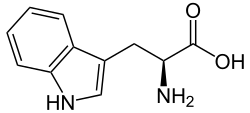
L-isomer af tryptofan
Spørgsmål og svar
Q: Hvad er tryptofan?
A: Tryptophan er en α-aminosyre, der bruges i biosyntesen af proteiner, og den har en indol-sidekæde, hvilket gør den til en upolær aromatisk aminosyre.
Q: Hvordan er tryptofan kodet?
A: Tryptofan er kodet af kodonet UGG.
Q: Hvad er de biologiske betingelser for tryptofan?
A: Under biologiske forhold har tryptofan en α-aminogruppe (som er i -NH3+-form) og en α-carboxylsyregruppe (som er i den deprotonerede -COO-form).
Q: Hvorfor er tryptofan essentielt for mennesker?
A: Tryptofan er essentielt for mennesker, fordi kroppen ikke kan syntetisere det, så det skal komme fra kosten.
Q: Hvilke neurotransmittere er tryptofan en forløber for?
A: Tryptofan er en forløber for neurotransmitterne serotonin og melatonin.
Q: Hvilken type aminosyre er tryptofan, og hvorfor?
A: Tryptofan er en upolær aromatisk aminosyre, fordi den har en indol-sidekæde.
Q: Hvordan bruges tryptofan i biosyntesen af proteiner?
A: Tryptofan bruges af kroppen i biosyntesen af proteiner. Det inkorporeres i proteiner under translation, hvor det kan danne hydrogenbindinger og deltage i pi-stacking-interaktioner i proteiner.
Søge