Directed evolution (DE) er en eksperimentel metode inden for proteinteknik, som bruges til at udvikle og optimere enzymer og andre funktionelle proteiner eller RNA-molekyler til industrielle, miljømæssige og medicinske anvendelser. Metoden efterligner principperne for naturlig udvælgelse ved gentagne runder af mutation og selektion for ønskede egenskaber.
Grundidé og arbejdsflow
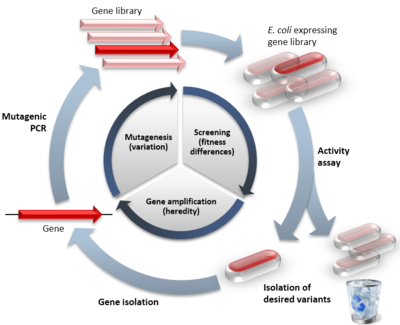
Den grundlæggende idé er at tage et udgangs-gen og udsætte det for gentagne mutationer for at skabe et stort bibliotek af varianter. Biblioteket af varianter screenes eller selekteres for forbedrede egenskaber, og de bedst fungerende varianter fungerer som en skabelon for næste runde. Efter flere iterationer kan man opnå betydelige forbedringer i aktivitet, stabilitet, specificitet eller andre ønskede træk.
Mutations‑ og biblioteksopbygning
Der findes flere teknikker til at skabe mangfoldighed i DNA-biblioteker:
- Fejlbehæftet PCR (error-prone PCR) — tilfældige punktmutationer introduceres under replikation.
- DNA-shuffling — rekombination af homologe sekvenser for at kombinere gavnlige mutationer fra forskellige forældre.
- Saturationsmutagene — målrettet variation på udvalgte aminosyrepositioner for at undersøge alle eller mange mulige substitutioner.
- Inserts/deletions og syntetiske biblioteker — for at undersøge større sekvensændringer eller designede varianter.
Udvælgelse og screening
Efter at biblioteket er skabt, skal varianterne testes for funktion. To overordnede tilgange anvendes:
- Selektionssystemer, hvor kun ønskede varianter overlever eller giver et målbart signal. Eksempler er kobling af enzymaktivitet til cellevækst eller brug af binder-associationer (f.eks. phage display).
- High-throughput screening, hvor individuelle varianter måles direkte i store skalaer ved hjælp af assays, flow-cytometri (FACS), mikrodrops-sortering eller automatiserede spektroskopiske systemer.
Valget mellem selektion og screening afhænger af, om der findes et robust output der kan kobles til overlevelse eller et højt gennemløbsassay, som kan måle den ønskede funktion.
In vivo vs. in vitro evolution
DE kan udføres in vivo eller in vitro, og valget påvirker både muligheder og begrænsninger:
Under in vivo-evolutionen transformeres hver celle (normalt bakterier eller gær) med et plasmid, der indeholder et andet medlem af variantbiblioteket. Kun det pågældende gen er forskelligt fra celle til celle, mens alle andre gener forbliver de samme. Cellerne udtrykker proteinet enten i cytoplasmaet eller i overfladen, hvor dets funktion kan testes. Dette format har den fordel, at der kan udvælges egenskaber i et cellulært miljø, hvilket er nyttigt, når det udviklede protein eller RNA skal anvendes i levende organismer.
Når DE udføres uden celler, anvendes in vitro-transskription og translation til at producere proteiner eller RNA frit i opløsning eller i kunstige mikrodråber. Dette har den fordel, at der er flere betingelser (f.eks. temperatur, opløsningsmidler) og at man kan udtrykke proteiner, som ville være giftige for celler. Desuden kan in vitro evolutionseksperimenter generere langt større biblioteker (op til 1015 varianter), fordi biblioteks-DNA'et ikke behøver at blive indsat i cellerne — noget som ofte begrænser, hvad der kan gøres in vivo.
Anvendelser
Directed evolution har ført til en lang række anvendelser:
- Optimering af industrielle enzymer til høj temperatur, ekstreme pH-forhold, eller nye substrater (f.eks. i vaskemidler, fødevareproduktion og biobrændstoffer).
- Udvikling af terapeutiske enzymer og antistoffer med forbedrede egenskaber og specificitet.
- Skabelse af biosensorer, nye katalytiske funktioner og biokemiske værktøjer til forskning (f.eks. forbedrede fluorescerende proteiner).
- Forståelse af evolutionære principper og proteinstruktur-funktionsforhold ved at kortlægge "fitness landskaber".
Fordele og begrænsninger
Fordele:
- Kræver ikke detaljeret viden om proteinets struktur eller mekanisme for at opnå forbedringer.
- Kan optimere komplekse træk (stabilitet, tolerance overfor opløsningsmidler, aktivitetsprofil) samtidigt.
Begrænsninger:
- Succes afhænger af kvaliteten og størrelsen af biblioteket samt af et egnet selektions- eller screeningsassay.
- Stigende kompleksitet: enkelte forbedringer kan medføre trade-offs (f.eks. øget stabilitet men nedsat aktivitet ved lave temperaturer).
- Praktiske og tekniske begrænsninger in vivo (toxicitetsproblemer, transformations-effektivitet) og ressourcemæssige krav til højt throughput in vitro.
Sikkerhed og etiske overvejelser
Directed evolution involverer genetiske manipulationer og skal udføres under relevante laboratorie‑ og biosikkerhedsregler. Når produkter er beregnet til medicinsk brug eller frigivelse i miljøet, kræves omhyggelig risikovurdering, regulering og tests for at sikre sikkerhed og etik.
Fremtidsperspektiver
Kombinationen af directed evolution med beregningsbaseret design (in silico‑modellering, AI og maskinlæring), automatiserede laboratorieplatforme og avancerede screeningsmetoder (mikrofluidik, next‑generation sequencing‑drevet analyse) gør det muligt at accelerere udviklingen af nye biomolekyler. Denne integration vil sandsynligvis gøre processerne mere effektive og målrettede, samtidig med at mulighederne for at løse komplekse bioteknologiske udfordringer udvides.
Samlet set er directed evolution et fleksibelt og kraftfuldt værktøj til at skabe og forfine biologiske katalysatorer og bindende molekyler, og metoden fortsætter med at udvikle sig i takt med nye teknologier og anvendelser.