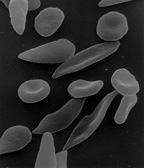
Balancerende selektion henviser til selektive processer, hvorved forskellige alleler (forskellige versioner af et gen) bevares i en populations genpulje med en frekvens, der er højere end genmutationens.
Dette sker normalt, når heterozygoten for et gen har en højere relativ fitness end homozygoten. På denne måde bevares den genetiske polymorfi.
Beviset for balancerende selektion kan findes i antallet af alleler i en population, som opretholdes over mutationsfrekvenserne. Al moderne forskning har vist, at denne betydelige genetiske variation er almindelig i panmictiske populationer. Det er Darwins, Wallaces og andres erfaring fra felten, at naturlige populationer i naturen er usædvanligt varierede. Museumssamlinger af enkelte arter fortæller den samme historie.
Der er flere måder, hvorpå balancerende selektion fungerer for at bevare polymorfisme. De to vigtigste og mest undersøgte er heterozygote fordele og frekvensafhængig selektion.
Hvordan balancerende selektion virker
Balancerende selektion dækker flere forskellige mekanismer, men fælles for dem er, at de modvirker tab af alleler ved tilfældig drift og vedrørende ensrettende (directional) selektion. De vigtigste mekanismer er:
- Heterozygot fordel (overdominans): Heterozygote individer (to forskellige alleler) har højere fitness end begge homozygote genotyper. Dette fører til et stabilt ligevægtspunkt, hvor begge alleler bevares.
- Frekvensafhængig selektion: Fitness afhænger af allelens frekvens i populationen. Ved negativ frekvensafhængighed har sjældne alleler en fordel netop fordi de er sjældne, hvilket fremmer vedvarende polymorfi. Ved positiv frekvensafhængighed kan derimod almindelige varianter blive favoriseret.
- Spatial og temporær heterogenitet: Forskellige miljøer (rumligt eller over tid) kan favorisere forskellige alleler. Migration mellem subpopulationer kan herefter opretholde flere alleler i den samlede population.
- Antagonistisk pleiotropi: En allel kan være fordelagtig i én biologisk funktion eller miljø og skadelig i en anden; hvis fordelene og ulemperne afvejer hinanden, kan begge alleler bestå.
- Selv-inkompatibilitet og flervalgs-systemer: I mange planter bevares et stort antal alleler i de gener, der styrer selv-inkompatibilitet, fordi sjældne alleler er fordelagtige (negativ frekvensafhængighed) for at undgå selvbestøvning.
Heterozygot fordel: matematisk simpelt eksempel
For to alleler A og a med fitness
- AA: 1 − s
- Aa: 1
- aa: 1 − t
er ligevægtsfrekvensen af A givet ved p̂ = t / (s + t) og af a ved q̂ = s / (s + t). Dette viser, at selv ved stærk selektion mod begge homozygote former kan begge alleler holdes ved mellemstore frekvenser, hvis heterozygoten er bedst.
Frekvensafhængig selektion — eksempler og virkninger
Negativ frekvensafhængighed er en af de mest effektive mekanismer til at opretholde polymorfi. Typiske eksempler:
- Pattedyrs immunsystem (f.eks. MHC/HLA): sjældne MHC-varianter kan være fordelagtige, fordi patogener er mindre tilpasset dem.
- Batesiansk og Mülleriansk mimicry hos insekter: predatorpræferencer og læring kan gøre sjældne farveformer mindre sårbare eller i visse systemer mere fordelagtige.
- Adfærdsmæssige strategier: fx forskellige parringsstrategier eller spisestrategier, hvor sjældne strategier kan have fordel, indtil de bliver almindelige.
- Selv-inkompatibilitet i planter, hvor sjældne alleler øger chancen for at finde en kompatibel partner.
Genomiske signaturer og hvordan man opdager balancerende selektion
Balancerende selektion efterlader kendetegn i DNA, som forskere kan søge efter:
- Øget lokal genetisk variation og høj heterozygositet omkring det selekterede locus.
- Intermediate allelfrekvenser (ikke kun meget sjældne eller faste alleler).
- Positive værdier af statistikker som Tajima's D (eksempelvis et skift mod flere mellem-frekvente varianter end neutralt forventet).
- Trans-species polymorphism: de samme alleler eller dybt forgrenede allelude varianter findes i nært beslægtede arter, hvilket tyder på meget gamle polymorfier bevaret gennem artsdannelser.
- Reduceret divergence men øget polymofismis omkring locus (på grund af langvarig bevarelse af forskellige haplotyper).
Moderne genomiske metoder (genome scans, population-genetiske tests, coalescent-modeller) kombineres ofte med økologiske data for at skelne balancerende selektion fra andre processer som demografi eller genflow.
Kendte biologiske eksempler
- Sickle-cell og malaria: Personer heterozygote for sickle-cell-allelen har nedsat risiko for alvorlig malaria, hvilket forklarer vedvarende høj frekvens af denne allel i malariaramte områder.
- MHC/HLA-locus hos vertebrater: ekstremt høj variation, ofte forklaret ved pathogen-medieret selektion og heterozygot fordel.
- Self-incompatibility gener i blomsterplanter: tusinder af forskellige alleler kan opretholdes pga. negativ frekvensafhængighed.
- Farvemønstre og adfærd i insekter og fisk: polymorfier i skaldyrsfarve, vinge-mønstre og adfærdsstrategier viser ofte tegn på frekvensafhængig selektion.
Begrænsninger, kompleksitet og evolutionær betydning
Balancerende selektion er ikke altid let at dokumentere entydigt; demografiske begivenheder, geniskombination og genetisk drift kan efterligne nogle signaturer. Men hvor den er veldokumenteret, bidrager den til:
- Langvarig bevarelse af genetisk variation, som kan være vigtig for populationers evne til at tilpasse sig nye udfordringer (fx nye patogener eller ændringer i miljøet).
- Øget kompleksitet i selektionsdynamikken, fordi fordelene ved en allel kan afhænge af genetisk og miljømæssig kontekst.
Konklusion
Balancerende selektion er et centralt koncept i evolutionsbiologi, der forklarer, hvordan og hvorfor flere genetiske varianter kan opretholdes i en population over lange tidsskalaer. Mekanismer som heterozygot fordel, negativ frekvensafhængig selektion, og rumlig/temporal heterogenitet virker ofte sammen og efterlader karakteristiske mønstre i genomet, som moderne metoder kan afsløre. Forståelsen af disse processer er vigtig for både grundforskning i evolution og anvendelser som bevarelsesbiologi og sygdomsgenetik.