Plumpuddingmodellen: Thomsons tidlige atommodel — forklaring og historie
Lær om Thomsons plumpuddingmodel: historien, idéen om elektroner i et positivt medium og hvorfor modellen blev forkastet — klar, kort forklaring og historisk kontekst.
Plum pudding-modellen var en tidlig (og ukorrekt) model af et atom fra det 20. århundrede. Den blev foreslået af J.J. Thomson i 1904, efter opdagelsen af elektronen, men før opdagelsen af atomkernen. På det tidspunkt vidste forskerne, at der var en positiv ladning i atomet, som udlignede elektronernes negative ladninger, hvilket gjorde atomet neutralt, men de vidste ikke, hvor den positive ladning kom fra. Thomsons model viste et atom, der havde et positivt ladet medium eller rum med negativt ladede elektroner inde i mediet. Kort efter forslaget blev modellen kaldt "plum pudding"-modellen, fordi det positive medium lignede en budding med elektroner, eller blommer, indeni.
Hvordan modellen var tænkt
Thomsons idé var at forklare atomet som en samlet, kontinuerlig positiv substans, hvor de negative elektroner var indlejret som enkeltdelene i en frugtbuding. Modellen søgte at forklare to centrale observationer:
- Atomer optrådte elektrisk neutrale i makroskopisk målestok, hvilket krævede en positiv modvægt til elektronerne.
- Elektroner var allerede påvist som partikler med negativ ladning, men deres placering i atomet var ukendt.
I Thomsons billede var den positive ladning spredt ud over atomets volumen i en næsten kontinuerlig fordeling, og elektronerne kunne bevæge sig rundt inden i denne positive "suppe". Modellen var intuitiv og enkel, og den forsøgte at kombinere kendte eksperimentelle fakta uden at antage en koncentreret kerne.
Begrænsninger og hvorfor modellen blev forkastet
Plum pudding-modellen havde flere teoretiske og eksperimentelle problemer:
- Manglende forklaring på røntgen- og emissionspektre: Modellen kunne ikke tilfredsstillende forklare de skarpe linjer i atomers spektrallinjer, som krev et system med veldefinerede energiniveauer for elektronerne.
- Stabilitetsproblemer: En jævnt fordelt positiv ladning med bevægelige elektroner gav ingen naturlig forklaring på, hvorfor elektroner ikke ville blive trukket sammen eller accelerere ud af systemet.
- Modstridende eksperimentelle resultater: Den mest afgørende modbevisning kom fra Geiger–Marsden-eksperimentet (ofte kaldet guldfolie-eksperimentet) udført af Hans Geiger og Ernest Marsden under ledelse af Ernest Rutherford omkring 1909. Når α-partikler blev skudt mod en tynd guldfolie, blev nogle få α-partikler spredt i meget store vinkler — noget der var umuligt at forklare med en jævnt fordelt positiv ladning.
Rutherford tolkningsmæssigt viste resultaterne, at næsten al massen og den positive ladning måtte være koncentreret i et meget lille område — en tæt, positivt ladet kerne — med elektroner roterende langt udenom. Denne atommodel blev publiceret omkring 1911 og afløste dermed plum pudding-billedet.
Efterfølgende udvikling
- Rutherfords atommodel (ca. 1911): Introducerede en kompakt, positiv kerne i centrum og elektroner i omløb omkring den—en model der forklarede spredningsdataene.
- Bohrs model (1913): Niels Bohr byggede videre på Rutherford ved at indføre kvantiserede elektronbaner, hvilket kunne forklare mange af de observerede spektrallinjer for brint og dermed løse et vigtigt problem, som plum pudding-modellen ikke kunne håndtere.
- Moderne kvantemekanik: Senere udviklinger førte til kvantemekaniske modeller, hvor elektroner beskrives af bølgefunktioner og sandsynlighedstæthed i konkrete orbitaler — langt fra Thomsons oprindelige “budding”-billede.
Historisk betydning
Selvom plum pudding-modellen i dag betragtes som forkert, var den vigtig af flere grunde:
- Den repræsenterer et kritisk skridt i udviklingen af atomteorien ved at forsøge at indarbejde den nye opdagelse af elektronen i en samlet model.
- Modellen lagde grund for diskussion og eksperimenter, som førte til afgørende opdagelser (som atomkernen) og hurtig fremgang i forståelsen af atomstrukturen.
- Historisk viser den, hvordan videnskabelige modeller testes og forbedres i lyset af nye eksperimentelle data — et centralt element i den videnskabelige metode.
Nøglepunkter (kort)
- Foreslået af J.J. Thomson i 1904 som et forsøg på at forklare atomets neutralitet efter opdagelsen af elektronen.
- Forestillede sig en positiv "suppe" med indlejrede negative elektroner — deraf navnet "plum pudding".
- Modellen blev modbevist af guldfolie-eksperimentet og erstattet af Rutherfords atommodel, og senere af Bohrs og kvantemekaniske beskrivelser.

Eksempel på Thomsons model
Udvikling til en moderne atommodel
Rutherfords model
I 1909, ikke længe efter at Thomsons model var blevet foreslået, foretog Hans Geiger og Ernest Marsden et eksperiment med tynde guldplader for at teste Thomsons model. Deres professor, Ernest Rutherford, forventede, at resultaterne ville bevise, at Thomson havde ret, men deres resultater var ekstremt anderledes end forventet. I 1911 opdagede Rutherford, at de positive ladninger kommer fra små partikler kaldet protoner, og at protonerne befandt sig i et lille center kaldet kernen, og at elektronerne kredsede rundt om kernen.
Bohr-modellen
Rutherfords model var ganske enkel, men den var forkert, fordi elektroner har en ladning, og de burde tiltrækkes af den positivt ladede kerne. I 1913 tilføjede Niels Bohr "energiniveauer" til den atomare model. Elektroner falder ikke ned i kernen, fordi de er indeholdt i energiniveauer, og for at skifte til højere energiniveauer er der brug for ekstra energi, og for at skifte til lavere energiniveauer er der brug for frigivelse af energi. Det er ikke muligt at ændre energitilstand uden at ændre elektronens energi. Hvis en elektron bliver ramt af en foton (en partikel, der bærer elektromagnetisk stråling), vil den få ekstra energi og gå op på et højere energiniveau (den skifter tilstand), hvorefter den springer tilbage til et lavere energiniveau og frigiver den energi, den indeholder. Denne nye model blev kaldt Bohr-modellen eller Rutherford-Bohr-modellen. Dermed blev der tilføjet en helt ny gren af videnskaben: Kvantefysik.
Kvantemodel
I 1926 brugte Erwin Schrödinger ideen om, at elektroner både optrådte som en bølge og som en partikel, hvilket kaldes bølge-partikel-dualitet. Dette tilføjede et helt nyt lag til atommodellen og kvantefysikken. Med en partikel kan man vide, hvor den befinder sig i rummet, hvis man observerer (ser) på den. Men med en bølge er den over det hele, så man kan ikke definere, hvor den præcist befinder sig. Dette er kendt som kvanteusikkerhed. Med en elektron kan du kun kende sandsynligheden for, at den befinder sig et sted, fordi den både er en bølge og en partikel. (Se diagrammet ovenfor)
Et billede, der viser en elektron, der skifter energiniveau og får og afgiver energi i form af fotoner.
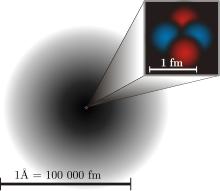
Dette viser den aktuelle atomare model. Den sorte skravering omkring atomet viser sandsynligheden for at finde en elektron der. Jo mørkere den er, jo større er chancen for at finde en elektron på det pågældende sted.
Relaterede sider
Søge