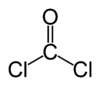
Fosgen er den kemiske forbindelse med formlen COCl2 . Denne gas har ingen farve. Gassen blev brugt som våben under Første Verdenskrig. Den er ansvarlig for de fleste dødsfald i forbindelse med giftgas under krigen. I dag bruges fosgen som et værktøj. Det bruges til organisk syntese. Når der er en lille mængde i luften, ligner lugten den den af nyslået hø eller græs. Nogle soldater under Første Verdenskrig har udtalt, at det lugtede lidt som majblomst. Når nogle klorforbindelser brænder eller nedbrydes, afgives der små mængder fosgen.
Egenskaber
Fosgen (ofte også kaldet carbonylchlorid) er en farveløs gas ved stuetemperatur med formel COCl2. Den har en molekylvægt på cirka 98,9 g/mol og et kogepunkt omkring 8 °C, hvilket betyder, at den kan kondensere til væske ved lave temperaturer eller under tryk. Gassen er tungere end luft og kan derfor samle sig i lavtliggende områder. Fosgen reagerer med vand under hydrolyse og danner kuldioxid (CO2) og saltsyre (HCl): COCl2 + H2O → CO2 + 2 HCl.
Fremstilling
Industrielt fremstilles fosgen typisk ved at føre carbonmonoxid (CO) og chlor (Cl2) over en katalysator (fx aktivt kul). Fosgen kan også dannes uønsket ved forbrænding eller termisk nedbrydning af klorerede organiske forbindelser, f.eks. ved brande i materialer, der indeholder klor.
Toksicitet og sundhedseffekter
Fosgen er højt giftigt. Det angriber især lungerne ved at reagere med proteiner og lipider i de fineste luftveje (alveoler), hvilket kan føre til væskeophobning (pulmonært ødem) og åndedrætsbesvær. En karakteristisk egenskab er, at eksponering kan give en latent periode — let irritation eller ingen symptomer umiddelbart efter eksponering, mens alvorlige respiratoriske symptomer først udvikler sig efter timer.
Typiske symptomer ved eksponering:
- irritation af øjne, næse og hals
- hoste og åndenød
- brystsmerter og svær træthed
- i svære tilfælde: akut respirationssvigt og død
Der findes ingen specifik antidot; behandlingen er understøttende: straks fjernelse fra eksponering, friskt luft, overvågning i mindst 24 timer (fordi symptomer kan forsinkes), administration af ilt og ved behov mekanisk ventilation. Hospitalisering er ofte nødvendig ved tegn på respirationspåvirkning.
Anvendelser
Fosgen er vigtig i den kemiske industri som reagens til fremstilling af:
- isocyanater (vigtige råmaterialer til polyurethaner)
- fenolformaldehyd-polycarbonater og andre polymerer
- syrechlorider og mellemprodukter i farmaceutisk og agro-kemisk produktion
I laboratorier foretrækkes ofte sikrere alternativer som triphosgen (et fast stof, der frigiver fosgen under reaktion) for at undgå håndtering af den farlige gas.
Historie
Under Første Verdenskrig blev fosgen anvendt som kemisk våben og var ansvarlig for et stort antal dødsfald blandt soldater udsat for giftgas. Dens evne til at forårsage senil opstået lungeødem gjorde den særligt farlig.
Sikkerhed, forebyggelse og detektion
Fosgen er stærkt reguleret, fordi det er en giftig industri-kemikalie og samtidig klassificeret som en kemisk kampagent i internationale konventioner. Arbejde med fosgen kræver strenge sikkerhedsforanstaltninger:
- automatiske gasdetektorer og alarmudstyr
- lukket procesudstyr og sekundære opsamlingssystemer
- personlig beskyttelse: åndedrætsværn (SCBA) og kemikaliebestandigt tøj ved uheld
- beredskabsplaner for lækager, inkl. evakuering og dekontamination
Bemærk: lugtesansen er en dårlig indikator for sikkerhed, fordi lavkoncentrationer kan være uden påviselig lugt eller fordi lugtgrænser kan overskrides før man registrerer noget. Specialudstyr er nødvendigt for sikker overvågning.
Miljø og nedbrydning
Fosgen hydrolyserer i kontakt med fugtighed eller vand til CO2 og HCl, hvilket betyder, at den ikke er langtidsholdbar i fugtige omgivelser, men HCl kan medføre lokal korrosion og forsuring. Som tung gas kan den ophobe sig i lave områder og udgøre en fare for personer og dyr i nærheden af udslip.
Håndtering ved uheld
Ved mistanke om lækage: evakuer område, adskaf kilder til antændelse, tilkald beredskab, anvend professionelt udstyr til opsamling/neutralisation. Ved eksponering: flyt personen til frisk luft, sørg for ilt og tilkald akut lægehjælp. Selv personer uden umiddelbare symptomer bør overvåges medicinsk i mindst 24 timer.
Samlet set er fosgen et kemisk nyttigt, men farligt stof, som kræver omhyggelig håndtering, korrekt teknisk sikring og beredskabsplaner for at forhindre alvorlige skader ved uheld eller misbrug.