I kemi er van der Waals-kræfter en type af intermolekylær kraft. En intermolekylær kraft er en relativt svag kraft, der holder molekyler sammen. Van der Waals-kræfter er den svageste type af intermolekylære kræfter. De er opkaldt efter den hollandske videnskabsmand Johannes Diderik van der Waals (1837-1923).
Hvad skaber van der Waals-kræfter?
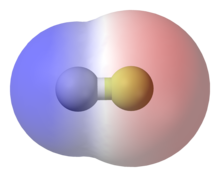
Negativt ladede elektroner kredser om molekyler eller ioner. Elektronerne skaber lidt forskellige ladninger fra den ene ende af molekylet til den anden. Disse små forskelle kaldes partielle ladninger, som δ - eller δ +.
Ud over permanente dipoler opstår også øjeblikkelige (inducerede) dipoler på grund af konstante kvantemekaniske udsving i elektronfordelingen. Når et øjeblikkeligt dipol dannes i et atom eller molekyle, kan det inducere et tilsvarende dipol i et nabomolekyle, og det er netop denne vekselvirkning der giver anledning til van der Waals-tiltrækning.
Typer af van der Waals-kræfter
- London-dispersionskræfter (også kaldet dispersionskræfter): Opstår mellem alle atomer og molekyler som følge af øjeblikkelige dipoler. De er ofte dominerende i ikke-polære stoffer og vokser med partiklens polariserbarhed og størrelse.
- Dipol–dipol-kræfter (Keesom): Opstår mellem molekyler med permanente dipoler, hvor positive og negative ender tiltrækker hinanden.
- Dipol–induceret dipol-kræfter (Debye): Opstår når et permanent dipol polariserer et nabomolekyle og derved inducerer en dipol i det.
- Hydrogenbinding omtales nogle gange separat, fordi den er betydeligt stærkere end typiske van der Waals-kræfter, men den har samme elektrostatiske ophav og indgår ofte i diskussioner om intermolekylære kræfter.
Rækkevidde og styrke
Van der Waals-kræfter falder hurtigt med afstand; den attraktive komponent for dispersionskræfter skalerer typisk med afstanden som cirka r-6, mens den kortdistante frastødning (på grund af elektronoverlap) vokser meget hurtigt ved korte afstande. En enkel model der ofte bruges til at beskrive denne balance er Lennard-Jones-potentialet (ofte kaldt 12–6 potentialet), som kombinerer en r-12-repulsion og en r-6-attraktion.
Betydning i kemi, biologi og materialer
Udtrykket bruges undertiden løst som et synonym for alle intermolekylære kræfter. Van der Waals-kræfter er relativt svage sammenlignet med kovalente bindinger, men spiller en grundlæggende rolle i supramolekylær kemi, enzymer, polymervidenskab, nanoteknologi, overfladevidenskab og fysik af kondenseret stof. Van der Waals-kræfterne definerer mange af organiske forbindelsers egenskaber, herunder deres opløselighed.
Eksempler på betydning:
- Flydende ædelgasser og lavt kogepunkt for små ikke-polære molekyler skyldes London-dispersionskræfter.
- Proteinfoldeprocesser, molekylær genkendelse og ligandbinding i enzymer påvirkes stærkt af disse svage interaktioner.
- Overfladeadhæsion og friktion ved nanoskalering (fx geckofødder, grafen-lag, smøremidler) afhænger af vdw-kræfter.
- Lagdelte materialer som grafit holdes sammen mellem lagene primært af van der Waals-kræfter.
Afhængighed af størrelse, polariserbarhed og temperatur
Større atomer og molekyler er mere polariserbare, hvilket øger dispersionskræfterne. Derfor har lange kulbrinter typisk højere kogepunkter end kortere på grund af stærkere vdw-interaktioner. Øget temperatur svækker typisk de organiserende virkninger af vdw-kræfter, fordi termisk bevægelse modvirker ordning og binding mellem partikler.
Måling og teoretisk behandling
Van der Waals-kræfter kan kvantificeres ved hjælp af teoretiske metoder (kvantemekaniske beregninger, molekylær dynamik) eller estimeres eksperimentelt via mål som kohæsion, overfladespænding, kogepunkter og bindingsenergier. I materialeteknik bruges ofte Hamaker-konstanten til at beskrive styrken af vdw-interaktioner mellem makroskopiske legemer.
Sammenfattende: selv om van der Waals-kræfter er relativt svage enkeltvis, er deres kollektive virkning afgørende for mange fysiske og kemiske egenskaber i naturen og i teknologiske materialer.

