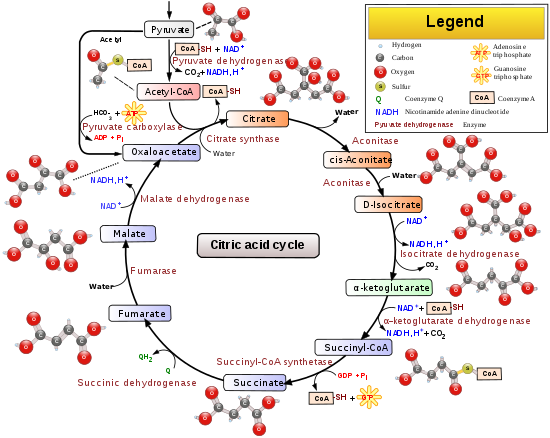
Krebs-cyklus (opkaldt efter Hans Krebs) er en del af celleatmningen. Dens andre navne er citronsyrecyklus og tricarboxylsyrecyklus (TCA-cyklus).
"Krebs-cyklus" er en række kemiske reaktioner, som alle aerobe organismer anvender i deres energiomsætningsprocesser. Den er vigtig for mange biokemiske forløb. Det tyder på, at det var en af de tidligste dele af det cellulære stofskifte, der udviklede sig.
Krebs-cyklussen kommer efter linkreaktionen og leverer den hydrogen og de elektroner, der er nødvendige for elektrontransportkæden. Den finder sted i mitokondrier.
Hvad er formålet med Krebs-cyklus?
Krebs-cyklusens hovedfunktion er at oxydere acetylgruppen fra acetyl-CoA fuldstændigt til CO2 og samtidig overføre energi i form af reducerede elektronbærere (NADH og FADH2) og et højtenergimolekyle (GTP/ATP). De reducerede coenzymer fører elektroner videre til elektrontransportkæden, hvor størstedelen af cellens ATP dannes. Cyklussen fungerer også som central metabolisk hub, fordi flere mellemliggende forbindelser bruges som byggesten i syntese af aminosyrer, nukleotider, heme m.m.
Trin i cyklussen (kort oversigt)
- Acetyl-CoA + oxaloacetat → citrat (enzym: citrate synthase)
- Citrat → isocitrat (aconitase)
- Isocitrat → α-ketoglutarat + CO2 + NADH (isocitrat dehydrogenase)
- α-Ketoglutarat → succinyl-CoA + CO2 + NADH (α-ketoglutarat dehydrogenase)
- Succinyl-CoA → succinat + GTP (eller ATP) (succinyl-CoA synthetase)
- Succinat → fumarat + FADH2 (succinat dehydrogenase)
- Fumarat → malat (fumarase)
- Malat → oxaloacetat + NADH (malat dehydrogenase)
Oxaloacetat genbruges i starten af cyklussen, så nettoprocessionen er cyklisk.
Energiproduktion — hvad får cellen ud af én acetyl-CoA?
- Reducerede coenzymer: 3 NADH og 1 FADH2
- Højtenergimolekyle: 1 GTP (eller i nogle celler direkte 1 ATP)
- Kuldioxid: 2 CO2 (de frigives som affaldsprodukt)
Når NADH og FADH2 oxidere i elektrontransportkæden, omdannes energien til ATP. Moderne beregninger bruger typisk omtrent 2,5 ATP per NADH og 1,5 ATP per FADH2, så ét gennemløb af cyklussen pr. acetyl-CoA giver groft regnet omkring ~10 ATP-ekvivalenter (7,5 fra NADH + 1,5 fra FADH2 + 1 fra GTP/ATP).
Regulering og tilpasning
Krebs-cyklussen er stærkt reguleret, så den svarer til cellens energibehov:
- Citrate synthase hæmmes af høje niveauer af ATP, NADH og citrate (tilbagekobling).
- Isocitrat dehydrogenase aktiveres af ADP og NAD+, hæmmes af ATP og NADH — dermed reagerer den på cellens energistatus.
- α-Ketoglutarat dehydrogenase hæmmes af NADH og succinyl-CoA og aktiveres af Ca2+ i muskler under arbejde.
- Pyruvat dehydrogenase-komplekset (linkreaktionen) kontrollerer tilførslen af acetyl-CoA fra pyruvat og reguleres via fosforylering og allosteriske effekter (ATP/NADH/acetyl-CoA).
Amfibolisk rolle og forbindelser til andre veje
Krebs-cyklus er amfibolisk — både katabolsk (nedbrydning til energi) og anabolsk (leverer forstadier til biosyntese). Eksempler:
- Citrate kan eksporteres til cytosolen og omdannes til acetyl-CoA for fedtsyresyntese via ATP-citrate lyase.
- Oxaloacetat kan bruges til gluconeogenese (nydannelse af glukose) i leveren.
- Succinyl-CoA er forbrugt ved syntese af heme.
- Intermediater kan fyldes op (anaplerotiske reaktioner) f.eks. ved karboxylering af pyruvat til oxaloacetat.
Hvor i cellen og i hvilke organismer?
Hos eukaryoter foregår Krebs-cyklen i mitokondriernes matrix. I prokaryoter (fx bakterier) finder de tilsvarende reaktioner ofte sted i cytoplasmaet eller knyttet til plasmamembranen. Enkelte organismer har modificerede eller delvise cyklusser afhængig af metaboliske behov.
Klinisk og biologisk relevans
Fejl i enzymer i Krebs-cyklus eller i tilhørende veje kan give metaboliske sygdomme, nedsat ATP-produktion og ophobning af intermediater. Endvidere er cyklussens aktivitet central ved cellulær respons på skift mellem hvilende og aktiv tilstand (fx muskelarbejde) og i kræftcelletilpasning af stofskiftet.
Opsummering
Krebs-cyklus er et centralt, cyklisk metabolsk forløb, der fuldstændigt oxiderer acetylgruppen fra acetyl-CoA til CO2, producerer reducerede elektronbærere (NADH, FADH2) og GTP/ATP, og forsyner cellen med byggesten til biosyntese. Den er afgørende for effektiv energiproduktion via elektrontransportkæden og for integrationen af kulhydrat-, fedt- og proteinmetabolisme.