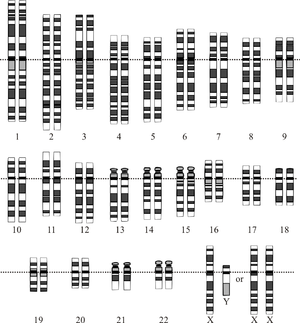
Det menneskelige genom er gemt på 23 kromosompar i cellekernen og i det lille mitokondrie-DNA. Man ved nu meget om de DNA-sekvenser, der findes på vores kromosomer. Hvad DNA'et egentlig gør, er nu delvis kendt. Anvendelsen af denne viden i praksis er kun lige begyndt.
Det menneskelige genomprojekt (HGP) har frembragt en referencesekvens, som anvendes i hele verden inden for biologi og medicin. Nature offentliggjorde rapporten om det offentligt finansierede projekt, og Science offentliggjorde Celeras artikel. Disse artikler beskrev, hvordan udkastet til sekvensen blev udarbejdet, og gav en analyse af sekvensen. Der blev offentliggjort forbedrede udkast i 2003 og 2005, som udfyldte ≈92 % af sekvensen.
Det seneste projekt ENCODE undersøger den måde, hvorpå generne styres.
Hvad indeholder det menneskelige genom?
Det menneskelige genom rummer cirka 3,2 milliarder basepar. Tidlige estimater pegede på 20.000–25.000 proteinkodende gener, men det meste af genomet består af ikke-kodende DNA: regulatoriske elementer, introner, gentagne sekvenser (transposoner) og strukturelle regioner som telomerer og centromerer. Disse ikke-kodende dele har ofte vigtige funktioner i genregulering og kromosomstruktur.
Mitokondrie-DNA (mtDNA) er et lille, cirkulært genom på omkring 16.6 kilobaser, der findes i cellens mitokondrier. Det arves typisk maternelt, koder for få proteiner, rRNA og tRNA, og spiller en væsentlig rolle i energiomsætning og visse arvelige sygdomme.
Kortlægning og referencesekvenser
Det menneskelige genomprojekt var et fælles internationalt initiativ, hvor offentlige forskningscentre og private aktører samtidig arbejdede for at fastlægge en referencesekvens. Projekterne benyttede forskellige metoder (bl.a. hierarkisk sekventering og shotgun-sekventering). Efter de første udkast fulgte forbedrede samlinger; siden da er referencen løbende opdateret (fx GRCh37, GRCh38).
I 2022 offentliggjorde Telomere-to-Telomere (T2T) konsortiet en næsten komplet, gap‑fri human referencesekvens (T2T‑CHM13), som fyldte mange af de tidligere udeladelser i svære, gentagne regioner. Samtidig er der store indsamlingsprojekter som 1000 Genomes, gnomAD og nationale biobanker, som kortlægger genetisk variation i befolkninger verden over.
Geners funktion og regulering
At kende DNA-sekvensen er kun første skridt. Mange funktioner afhænger af, hvor og hvornår et gen bliver aktiveret. Projekter som ENCODE kortlægger:
- promotere og enhancere
- transkriptionsfaktor-bindingssteder
- kromatinmodifikationer og åbne kromatinregioner
- ikke-kodende RNA og alternative transskripter
Der har været debat om, hvor meget af genomet man skal betegne som "funktionelt", fordi mange biokemiske tegn på aktivitet ikke nødvendigvis betyder biologisk betydning for organismen som helhed.
Genetisk variation og evolution
Inden for arten findes millioner af genetiske varianter: SNP'er, insertioner/deletioner (indels), kopiantalvariationer og strukturelle omrokeringer. Nogle variationer er neutrale, mens andre påvirker sygdomsrisiko, respons på medicin eller fysiologiske træk. Populationgenetik bruger denne variation til at forstå menneskets oprindelse, migrationer og befolkningsstruktur.
Medicinsk betydning
Genomforskningen har allerede revolutioneret medicin på flere områder:
- Diagnostik: Sekventering af hele exomet eller genomet afdækker årsager til mange arvelige sygdomme.
- Kræftgenomik: Tumorer kan sekventeres for at finde drivende mutationer, som kan være mål for præcisionsbehandling.
- Farmakogenetik: Genetiske varianter påvirker lægemiddelrespons og bivirkninger, hvilket kan guide dosis og valg af behandling.
- Prænatal og neonatal screening: Ikke-invasiv fostervandsprøve og nyfødtscreening bruger genetisk information til tidlig påvisning af sygdomme.
- Genterapi og genredigering: Metoder som CRISPR/Cas giver nye behandlingsmuligheder, men rejser også sikkerheds‑ og etiske spørgsmål.
Etiske, juridiske og sociale spørgsmål
Stigende tilgængelighed af genomdata rejser vigtige problemstillinger:
- fortrolighed og datasikkerhed
- risiko for genetisk diskrimination (fx forsikring, arbejde)
- samtykke og håndtering af utilsigtede fund
- behov for repræsentative genetiske databaser for at undgå biased medicinsk viden
Fremtidige retninger
Fremtidens genomforskning fokuserer på at:
- forbinde sekvensdata med funktion (single-cell omics, epigenetik, spatial transcriptomics)
- forstå samspillet mellem gener og miljø
- udvikle sikre og retfærdige genom-baserede behandlinger
- udvide referencer til at omfatte flere befolkningsgrupper og fuldt komplette haplotyper
Konklusion: Vi har i dag en dyb viden om DNA-sekvenserne i det menneskelige genom og kraftfulde værktøjer til at bruge denne viden i forskning og klinik. Alligevel er der fortsat store udfordringer i at oversætte sekvensinformation til fuldt ud forståelige biologiske mekanismer og sikre, at anvendelsen bliver etisk, retfærdig og gavnlig for hele befolkningen.