Overfladespænding — definition, årsager og eksempler i væsker
Overfladespænding: klar og enkel forklaring på definition, årsager og konkrete eksempler i væsker — fra vanddråber til insekter. Lær fysikken bag overfladen.
Overfladespænding er en egenskab ved væsker, hvor væskens overflade opfører sig som en elastisk hinde. Overfladen kan bære små vægte, og en vanddråbe bevarer sin runde form fordi overfladen forsøger at minimere arealet. Nogle små genstande kan derfor flyde på en væskeoverflade, selv om de i et vakuum eller under vand normalt ville synke. Enkelte insekter (f.eks. vandløbere) kan gå eller løbe på vandoverfladen takket være denne egenskab. Forklaringen ligger i, at molekylerne i væsken tiltrækker hinanden (kohæsion), og denne indre tiltrækning bestemmer meget af væskers opførsel.
Definition og måleenheder
Overfladespænding er både en kraft pr. længdeenhed (typisk N/m) og en energi pr. arealenhed (J/m²). De to måder at betragte fænomenet på er ækvivalente: en høj overfladespænding betyder både en større kraft langs en rand og mere energi for at skabe et nyt overfladeareal. Når man taler om faste materialer bruges ofte udtrykket overfladeenergi, som dækker det samme fænomen i en mere generel forstand og gælder derfor også for faste stoffer.
Årsager til overfladespænding
Overfladespænding skyldes, at væskemolekyler inde i væsken oplever tiltrækninger fra alle sider, mens molekyler ved overfladen mangler naboer i den ene retning. Denne ubalance giver en nettoindadrettet kraft på overflademolekylerne, som får overfladen til at stramme sig sammen. Ud over kohæsion spiller også adhesion (tiltrækning mellem væsken og et andet materiale), molekylær struktur, og hydrogenbindinger (i fx vand) en væsentlig rolle.
Eksempler og anvendelser
- Vanddråber og dråbeform: Overfladespænding får dråber til at antage sferiske former for at minimere overfladearealet.
- Insekter på vand: Små dyr som insekter og især vandløbere udnytter overfladespænding til at bevæge sig uden at bryde overfladen.
- Vaskemidler og overfladeaktive stoffer: Sæbe og andre surfaktanter reducerer overfladespændingen, så vand bedre spreder sig og trænger ind i porer og fibre — grundlaget for rengøring.
- Kapillærbevægelse: Små rør eller porøse materialer kan trække væsker opad mod tyngdekraften på grund af en kombination af overfladespænding og adhæsion.
- Teknologi og forskning: Mikrofluidik, tryksårbehandling, bejdsning og coating-processer samt mange biomedicinske anvendelser afhænger af styring af overfladespænding.
Faktorer der påvirker overfladespænding
- Temperatur: Overfladespændingen falder normalt, når temperaturen stiger.
- Tilsætningsstoffer: Opløste stoffer som sæbe, alkoholer eller tensider kan dramatisk nedsætte overfladespændingen.
- Opløste salte og urenheder: Kan enten øge eller mindske overfladespændingen afhængig af typen og koncentrationen.
- Gas-/væskekontakt: Omgivende gasarter og adsorption af molekyler fra luften kan ændre overfladeegenskaberne.
Matematik og måling
Overfladespænding betegnes ofte med det græske bogstav γ (gamma). I mange sammenhænge indgår den i Young–Laplace-ligningen, som beskriver trykforskellen ΔP over en krum væskeoverflade: ΔP = γ(1/R1 + 1/R2), hvor R1 og R2 er principalradierne for krumningen. Praktisk måles overfladespænding ved metoder som du Noüy-ring eller Wilhelmy-plate, hvor man måler kraften der kræves for at trække en ring eller plade gennem en væskeoverflade.
Overfladespænding i materialeforskning
Inden for materialevidenskab anvendes begrebet både om klassisk overfladespænding i væsker og om fri energi på overfladen for faste materialer. Forståelse af disse overfladeegenskaber er vigtig ved fremstilling af belægninger, limning, trykning og nanoteknologi.
Kort sagt: Overfladespænding er en central fysisk egenskab, som forklarer en række velkendte fænomener fra vanddråbers form til insektets gang på vandet, og som har mange praktiske anvendelser i både hverdag og teknologi.
Årsager
De sammenhængende kræfter mellem væskemolekylerne forårsager overfladespænding. I hovedparten af væsken trækkes hvert molekyle lige meget i alle retninger af de tilstødende væskemolekyler, hvilket resulterer i en nettokraft på nul. Molekylerne i overfladen har ikke andre molekyler på alle sider af dem og trækkes derfor indad. Dette skaber et vist indre tryk og tvinger væskeoverfladerne til at trække sig sammen til det minimale areal.
Overfladespænding er ansvarlig for væskedråbernes form. Selv om vanddråberne er lette at deformere, har de en tendens til at blive trukket i kugleform af de kohæsive kræfter i overfladelaget. Hvis der ikke var andre kræfter, herunder tyngdekraften, ville dråber af stort set alle væsker være perfekt kugleformede. Den sfæriske form minimerer den nødvendige "vægspænding" i overfladelaget i henhold til Laplace's lov.
En anden måde at se det på er i form af energi. Et molekyle i kontakt med en nabo er i en lavere energitilstand, end hvis det var alene (ikke i kontakt med en nabo). De indre molekyler har så mange naboer som muligt, men grænsemolekylerne mangler naboer (i forhold til de indre molekyler). Så grænsemolekylerne har en højere energi. For at væsken kan minimere sin energitilstand, skal antallet af grænsemolekyler med højere energi minimeres. Den minimerede mængde af grænsemolekyler resulterer i et minimeret overfladeareal.
Som følge af minimering af overfladearealet vil en overflade antage den mest glatte form, den kan. Enhver krumning i overfladens form resulterer i et større areal og en højere energi. Overfladen vil derfor skubbe tilbage mod enhver krumning på samme måde som en bold, der skubbes op ad bakke, vil skubbe tilbage for at minimere sin potentielle tyngdeenergi.
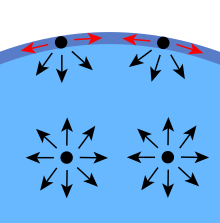
Diagram over kræfterne på molekyler i væske

Overfladespændingen forhindrer papirclipsen i at komme ned i vandet.
Virkninger i hverdagen
Vand
Undersøgelse af vand viser flere virkninger af overfladespænding:
A. Regnvand danner perler på overfladen af en voksagtig overflade, f.eks. et blad. Vand klæber svagt til voks og stærkt til sig selv, så vandet samler sig til dråber. Overfladespændingen giver dem deres næsten kugleform, fordi en kugle har det mindst mulige forhold mellem overfladeareal og volumen.
B. Dråbedannelse opstår, når en væskemasse strækkes. Animationen viser, at vand, der klæber til vandhanen, vokser i masse, indtil det strækkes til et punkt, hvor overfladespændingen ikke længere kan binde det til vandhanen. Dråben skiller sig så ad, og overfladespændingen danner dråben til en kugle. Hvis der løb en vandstrøm fra vandhanen, ville strømmen blive splittet op i dråber under faldet. Tyngdekraften strækker strømmen, hvorefter overfladespændingen klemmer den sammen til kugler.
C. Genstande, der er tættere end vand, flyder stadig, når genstanden ikke kan vædes, og dens vægt er lille nok til at blive båret af de kræfter, der opstår som følge af overfladespænding. F.eks. bruger vandløbere overfladespændingen til at gå på overfladen af en dam. Vandets overflade opfører sig som en elastisk film: insektets fødder forårsager indtryk i vandets overflade, hvilket øger dets overfladeareal.
D. Adskillelse af olie og vand (i dette tilfælde vand og flydende voks) skyldes en spænding i overfladen mellem forskellige væsker. Denne type overfladespænding kaldes "grænsefladespænding", men fysikken er den samme.
E. Vinens tårer er dannelsen af dråber og risler på siden af et glas med en alkoholholdig drik. Årsagen er et komplekst samspil mellem de forskellige overfladespændinger mellem vand og ethanol. Den fremkaldes af en kombination af en ændring af vands overfladespænding ved hjælp af ethanol sammen med, at ethanol fordamper hurtigere end vand.
· 
A. Vandperler på et blad
· 
B. Vand, der drypper fra en vandhane
· 
C. Vandstriderne forbliver oven på væsken på grund af overfladespændingen
· 
D. Lavalampe med vekselvirkning mellem forskellige væsker; vand og flydende voks
· 
E. Foto, der viser fænomenet "tårer af vin".
Overfladeaktive stoffer
Overfladespændingen er synlig i andre almindelige fænomener, især når der anvendes overfladeaktive stoffer til at mindske den:
- Sæbebobler har meget store overfladearealer med meget lidt masse. Bobler i rent vand er ustabile. Tilsætning af overfladeaktive stoffer kan dog have en stabiliserende virkning på boblerne (se Marangoni-effekten). Bemærk, at overfladeaktive stoffer faktisk reducerer vandets overfladespænding med en faktor tre eller mere.
- Emulsioner er en type opløsning, hvor overfladespænding spiller en rolle. Små oliefragmenter, der er suspenderet i rent vand, vil spontant samle sig til meget større masser. Men tilstedeværelsen af et overfladeaktivt stof mindsker overfladespændingen, hvilket gør det muligt at stabilisere de små oliedråber i en stor mængde vand (eller omvendt).
Grundlæggende fysik
To definitioner
Overfladespænding, repræsenteret ved symbolet γ, er defineret som kraften langs en linje med en længdeenhed, hvor kraften er parallel med overfladen, men vinkelret på linjen. En måde at forestille sig dette på er at forestille sig en flad sæbefilm, der på den ene side er afgrænset af en stram tråd af længde L. Tråden vil blive trukket mod filmens indre af en kraft svarende til 2 
En tilsvarende definition, som er nyttig i termodynamikken, er arbejde udført pr. arealenhed. For at øge overfladen af en væskemasse med en mængde, δA, skal der således udføres en mængde arbejde, 
Det kan påvises ved hjælp af dimensionsanalyse, at der er ækvivalens mellem måling af energi pr. arealenhed og kraft pr. længdeenhed.
Overfladekrumning og tryk
Hvis der ikke virker nogen kraft normalt på en spændt overflade, skal overfladen forblive flad. Men hvis trykket på den ene side af overfladen er forskelligt fra trykket på den anden side, resulterer trykforskellen gange overfladearealet i en normalkraft. For at overfladespændingskræfterne kan ophæve den kraft, der skyldes trykket, skal overfladen være krum. Diagrammet viser, hvordan overfladekrumning af en lille plet overflade fører til en nettokomponent af overfladespændingskræfter, der virker normalt på plettens centrum. Når alle kræfterne er afbalanceret, er den resulterende ligning kendt som Young-Laplace-ligningen:
hvor:
· Δp er trykforskellen.
· 
· Rx og Ry er krumningsradier i hver af de akser, der er parallelle med overfladen.
Den i parentes stående størrelse på højre side er faktisk (dobbelt) overfladens gennemsnitlige krumning (afhængig af normalisering).
Løsningerne til denne ligning bestemmer formen af vanddråber, vandpytter, menisker, sæbebobler og alle andre former, der er bestemt af overfladespændingen. (Et andet eksempel er formen af de aftryk, som en vandløberfødders fødder laver på overfladen af en dam).
Tabellen nedenfor viser, hvordan det indre tryk i en vanddråbe stiger med faldende radius. For ikke særligt små dråber er virkningen subtil, men trykforskellen bliver enorm, når dråbestørrelsen nærmer sig molekylestørrelsen. (Ved grænsen til et enkelt molekyle bliver begrebet meningsløst).
| Δp for vanddråber med forskellig radius ved STP | ||||
| Dråbernes radius | 1 mm | 0,1 mm | 1 μm | 10 nm |
| Δp (atm) | 0.0014 | 0.0144 | 1.436 | 143.6 |
Flydende overflade
Det er svært at finde formen på den minimale overflade, der er afgrænset af en vilkårlig formet ramme, ved hjælp af matematik alene. Men ved at lave en ramme af ståltråd og dyppe den i sæbeopløsning vil der i løbet af få sekunder opstå en lokal minimal overflade i den resulterende sæbefilm.
Årsagen hertil er, at trykforskellen over en væskegrænseflade er proportional med den gennemsnitlige krumning, som det fremgår af Young-Laplace-ligningen. For en åben sæbefilm er trykforskellen nul, og derfor er middelkrumningen nul, og minimale overflader har den egenskab, at middelkrumningen er nul.
Kontaktvinkler
Overfladen af enhver væske er en grænseflade mellem væsken og et andet medium. Overfladen på en dam er f.eks. en grænseflade mellem vandet i dammen og luften. Overfladespænding er således ikke en egenskab ved væsken alene, men en egenskab ved væskens grænseflade med et andet medium. Hvis en væske befinder sig i en beholder, er der ud over grænsefladen mellem væske og luft på overfladen også en grænseflade mellem væsken og beholderens vægge. Overfladespændingen mellem væsken og luften er normalt forskellig (større end) dens overfladespænding i forhold til væggene i beholderen. Hvor de to overflader mødes, vil geometrien afbalancere alle kræfter.
Hvor de to overflader mødes, danner de en kontaktvinkel, 


I diagrammet skal både de lodrette og vandrette kræfter ophæve hinanden nøjagtigt i kontaktpunktet, hvilket kaldes ligevægt. Den horisontale komponent af 

Den vigtigste styrkebalance er dog i den lodrette retning. Den lodrette komponent af 

| Flydende | Solid | Kontaktvinkel | |||
| vand |
| 0° | |||
| diethylether | |||||
| tetrachlormethan | |||||
| glycerol | |||||
| eddikesyre | |||||
| vand | paraffinvoks | 107° | |||
| sølv | 90° | ||||
| methyljodid | sodakalkglas | 29° | |||
| blyglas | 30° | ||||
| smeltet kvarts | 33° | ||||
| sodakalkglas | 140° | ||||
| Nogle kontaktvinkler mellem væske og fast stof | |||||
Da kræfterne står i direkte forhold til deres respektive overfladespændinger, har vi også:
hvor
· 
· 
· 
· 
Det betyder, at selv om forskellen mellem overfladespændingen mellem væske og faststof og mellem faststof og luft, 


Det samme forhold findes i diagrammet til højre. Men i dette tilfælde ser vi, at fordi kontaktvinklen er mindre end 90°, skal forskellen i overfladespænding mellem væske og fast stof/faststof/luft være negativ:
Særlige kontaktvinkler
Bemærk, at i det særlige tilfælde af en grænseflade mellem vand og sølv, hvor kontaktvinklen er lig med 90°, er forskellen i overfladespænding mellem væske og fast stof/faststof og luft nøjagtig nul.
Et andet særligt tilfælde er, når kontaktvinklen er præcis 180°. Vand med specielt forberedt teflon nærmer sig dette. Kontaktvinkel på 180° opstår, når overfladespændingen mellem væske og fast stof er nøjagtig lig med overfladespændingen mellem væske og luft.
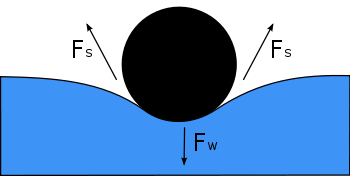
Diagrammet viser et tværsnit af en nål, der flyder på vandoverfladen. Dens vægt, Fw , trykker overfladen ned og afbalanceres af overfladespændingskræfterne på begge sider, Fs , som hver især er parallelle med vandets overflade på de punkter, hvor de kommer i kontakt med nålen. Bemærk, at de horisontale komponenter af de to Fs -pile peger i modsatte retninger, så de ophæver hinanden, men de vertikale komponenter peger i samme retning og summerer derfor op til balance Fw .
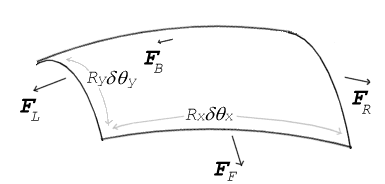
Overfladespændingskræfter, der virker på en lille (differentiel) plet af overfladen. δθx og δθy angiver bøjningsgraden i forhold til plettens dimensioner. Afbalancering af spændingskræfterne med trykket fører til Young-Laplace-ligningen

Minimal overflade
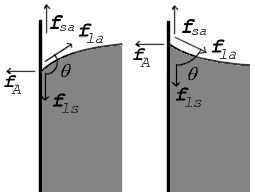
Kræfter i kontaktpunktet vist for en kontaktvinkel større end 90° (venstre) og mindre end 90° (højre)
Målemetoder
Da overfladespændingen viser sig i form af forskellige virkninger, er der flere måder at måle den på. Hvilken metode der er den optimale afhænger af arten af den væske, der skal måles, de betingelser, hvorunder dens spænding skal måles, og overfladens stabilitet, når den deformeres.
- Du Noüy Ring-metoden: Den traditionelle metode, der anvendes til at måle overflade- eller grænsefladespænding. Overfladens eller grænsefladens fugtighedsegenskaber har kun ringe indflydelse på denne måleteknik. Der måles det maksimale træk, som overfladen udøver på ringen.
- Du Noüy-Padday-metoden: En minimeret version af Du Noüy-metoden anvender en metalnål med lille diameter i stedet for en ring i kombination med en mikrobalance med høj følsomhed til at registrere det maksimale træk. Fordelen ved denne metode er, at meget små prøvevolumener (ned til nogle få tiendedele mikroliter) kan måles med meget høj præcision, uden at det er nødvendigt at korrigere for opdrift (for en nål eller snarere en stang med korrekt geometri). Endvidere kan målingen udføres meget hurtigt, mindst på ca. 20 sekunder. De første kommercielle flerkanals tensiometre [CMCeeker] blev for nylig bygget på grundlag af dette princip.
- Wilhelmy-plademetoden: En universel metode, der er særlig velegnet til at kontrollere overfladespændingen over lange tidsintervaller. En lodret plade med kendt omkreds fastgøres til en vægt, og den kraft, der skyldes vædepåvirkning, måles.
- Metode med spindedråber: Denne teknik er ideel til måling af lave grænsefladespændinger. Diameteren af en dråbe i en tung fase måles, mens begge faser roterer.
- Metode med nedfald af vedhæng: Overflade- og grænsefladespænding kan måles med denne teknik, selv ved forhøjede temperaturer og tryk. Dråbens geometri analyseres optisk. For nærmere oplysninger, se dråbe.
- Bobletrykmetoden (Jaeger-metoden): En måleteknik til bestemmelse af overfladespænding ved korte overfladealdre. Det maksimale tryk i hver enkelt boble måles.
- Dråbevolumenmetoden: En metode til bestemmelse af grænsefladespænding som en funktion af grænsefladens alder. Væske med en massefylde pumpes ind i en anden væske med en anden massefylde, og tiden mellem de dannede dråber måles.
- Kapillarstigningsmetoden: Enden af en kapillær nedsænkes i opløsningen. Den højde, hvor opløsningen når ind i kapillæret, er relateret til overfladespændingen ved hjælp af nedenstående ligning.
- Stalagmometrisk metode: En metode til vejning og aflæsning af en væskedråbe.
- Metoden med siddende dråber: En metode til bestemmelse af overfladespænding og tæthed ved at placere en dråbe på et substrat og måle kontaktvinklen (se "sessile drop technique").
- Vibrationsfrekvens af svævende dråber: Overfladespændingen i superfluid4 He er blevet målt ved at studere den naturlige frekvens af vibrationssvingninger af dråber, der holdes i luften ved hjælp af magnetisme. Denne værdi anslås at være 0,375 dyn/cm ved T = 0° K.

Overfladespændingen kan måles ved hjælp af metoden med hængende dråber på et goniometer.
Virkninger
Væske i et lodret rør
Et gammelt kviksølvbarometer består af et lodret glasrør med en diameter på ca. 1 cm, der er delvist fyldt med kviksølv og med et vakuum (kaldet Torricellis vakuum) i det ufyldte rum (se diagrammet til højre). Bemærk, at kviksølvniveauet i midten af røret er højere end i kanterne, hvilket gør den øverste overflade af kviksølvet kuppelformet. Massecentret for hele kviksølvsøjlen ville være lidt lavere, hvis kviksølvsoverfladen var flad over hele rørets tværsnit. Men den kuppelformede overside giver lidt mindre overfladeareal til hele kviksølvmassen. Igen kombinerer de to virkninger sig for at minimere den samlede potentielle energi. En sådan overfladeform er kendt som en konveks menisk.
Vi betragter overfladearealet af hele kviksølvmassen, herunder den del af overfladen, der er i kontakt med glasset, fordi kviksølv slet ikke klæber til glas. Kviksølvets overfladespænding virker altså på hele dets overfladeareal, også der, hvor det er i kontakt med glasset. Hvis røret i stedet for glas var lavet af kobber, ville situationen være helt anderledes. Kviksølv klæber aggressivt til kobber. Så i et kobberrør vil kviksølvniveauet i midten af røret være lavere end i kanterne (dvs. der vil være tale om en konkav menisk). I en situation, hvor væsken klæber til beholderens vægge, betragter vi den del af væskens overfladeareal, der er i kontakt med beholderen, som havende en negativ overfladespænding. Væsken arbejder så for at maksimere kontaktoverfladen. Så i dette tilfælde mindskes den potentielle energi ved at øge arealet i kontakt med beholderen snarere end at øge den potentielle energi. Dette fald er tilstrækkeligt til at kompensere for den øgede potentielle energi, der er forbundet med at løfte væsken tæt på beholderens vægge.
Hvis et rør er tilstrækkeligt smalt, og væskens vedhæftning til væggene er tilstrækkelig stærk, kan overfladespændingen trække væske op ad røret i et fænomen, der kaldes kapillær virkning. Den højde, som søjlen løftes op til, er givet ved:
hvor
· 
· 
· 
· 
· 
· 

Vandpytter på en overflade
Når kviksølv hældes på en vandret flad glasplade, opstår der en vandpyt, som har en tykkelse, der er mærkbar. Pytten breder sig kun ud til det punkt, hvor den er lidt under en halv centimeter tyk, og ikke tyndere. Dette skyldes igen kviksølvs stærke overfladespænding. Den flydende masse flader ud, fordi det bringer så meget af kviksølvet ned på et så lavt niveau som muligt, men overfladespændingen virker samtidig til at reducere det samlede overfladeareal. Resultatet er et kompromis i form af en pyt med en næsten fast tykkelse.
Den samme demonstration af overfladespænding kan udføres med vand, kalkvand eller endda saltvand, men kun hvis væsken ikke klæber til det flade overflademateriale. Voks er et sådant stof. Vand, der hældes på en glat, flad, vandret voksoverflade, f.eks. en vokset glasplade, vil opføre sig på samme måde som kviksølv, der hældes på glas.
Tykkelsen af en væskepøl på en overflade, hvis kontaktvinkel er 180°, er givet ved:
hvor
|
|
|
|
|
|
|
|
I virkeligheden vil vandpytternes tykkelse være lidt mindre end det, der forudsiges af ovenstående formel, fordi meget få overflader har en kontaktvinkel på 180° med en væske. Når kontaktvinklen er mindre end 180°, er tykkelsen givet ved:
For kviksølv på glas er γHg = 487 dyn/cm, ρHg = 13,5 g/cm3 og θ = 140°, hvilket giver hHg = 0,36 cm. For vand på paraffin ved 25 °C er γ = 72 dyn/cm, ρ = 1,0 g/cm3 , og θ = 107°, hvilket giver hH2O = 0,44 cm.
Formlen forudsiger også, at når kontaktvinklen er 0°, vil væsken sprede sig ud i et mikro-tyndt lag over overfladen. En sådan overflade siges at være fuldt opvredet af væsken.
Opsplitning af vandløb i dråber
I dagligdagen kan vi alle se, at en vandstrøm, der kommer ud af en vandhane, vil blive opløst i dråber, uanset hvor jævnt vandstrømmen kommer ud af vandhanen. Dette skyldes et fænomen kaldet Plateau-Rayleigh-instabilitet, som udelukkende skyldes virkningerne af overfladespænding.
Forklaringen på denne ustabilitet begynder med eksistensen af små forstyrrelser i strømmen. Disse er altid til stede, uanset hvor glat strømmen er. Hvis forstyrrelserne opløses i sinusformede komponenter, finder vi, at nogle komponenter vokser med tiden, mens andre aftager med tiden. Blandt dem, der vokser med tiden, vokser nogle hurtigere end andre. Hvorvidt en komponent aftager eller vokser, og hvor hurtigt den vokser, er udelukkende en funktion af dens bølgetal (et mål for hvor mange toppe og lavpunkter pr. centimeter) og radiuserne i den oprindelige cylindriske strøm.
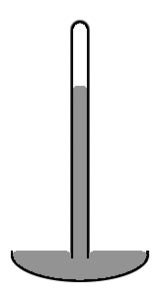
Diagram af et kviksølvbarometer
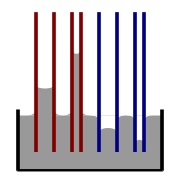
Illustration af kapillarstigning og -fald. Rød = kontaktvinkel mindre end 90°; blå = kontaktvinkel større end 90°.
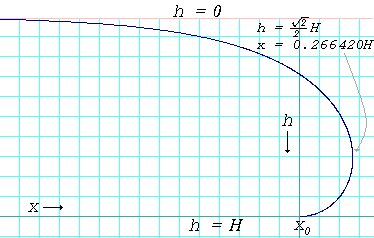
Profilkurve for kanten af en vandpyt, hvor kontaktvinklen er 180°. Kurven er givet ved formlen: 

Små vandpytter på en glat, ren overflade har en mærkbar tykkelse.
Illustration af, hvordan en lavere kontaktvinkel fører til en reduktion af vandpyttens dybde
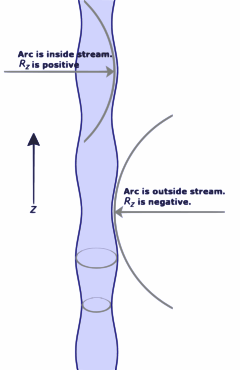
Mellemstadiet af en jet, der bryder op i dråber. Kurveringsradier i aksial retning er vist. Ligningen for strømmenes radius er 




Datatabel
| Overfladespænding af forskellige væsker i dyn/cm mod luft | ||
| Flydende | Temperatur °C | overfladespænding, γ |
| Eddikesyre | 20 | 27.6 |
| Eddikesyre (40,1 %) + vand | 30 | 40.68 |
| Eddikesyre (10,0 %) + vand | 30 | 54.56 |
| Acetone | 20 | 23.7 |
| Diethylether | 20 | 17.0 |
| Ethanol | 20 | 22.27 |
| Ethanol (40%) + vand | 25 | 29.63 |
| Ethanol (11,1 %) + vand | 25 | 46.03 |
| Glycerol | 20 | 63 |
| n-Hexan | 20 | 18.4 |
| Saltsyre 17,7 M vandig opløsning | 20 | 65.95 |
| Isopropanol | 20 | 21.7 |
| Flydende kvælstof | -196 | 8.85 |
| 15 | 487 | |
| Methanol | 20 | 22.6 |
| n-Oktaan | 20 | 21.8 |
| Natriumchlorid 6.0M vandig opløsning | 20 | 82.55 |
| Saccharose (55%) + vand | 20 | 76.45 |
| Vand | 0 | 75.64 |
| Vand | 25 | 71.97 |
| Vand | 50 | 67.91 |
| Vand | 100 | 58.85 |
Galleri af effekter
· 
Opbrud af en vandplade i bevægelse, der preller af på en ske.
· 
Foto af rindende vand, der klæber til en hånd. Overfladespændingen skaber vandlaget mellem strømmen og hånden.
· 
En sæbeboble balancerer overfladespændingskræfter mod det indre pneumatiske tryk.
· 
Overfladespænding forhindrer en mønt i at synke: Mønten er ubestrideligt tættere end vand, så den skal fortrænge et volumen, der er større end dens eget, for at opdriften kan afbalancere massen.
· 
En tusindfryd. Hele blomsten ligger under niveauet af den (uforstyrrede) frie overflade. Vandet stiger jævnt op omkring dens kant. Overfladespændingen forhindrer, at vandet fylder luften mellem kronbladene og eventuelt nedsænker blomsten.
· 
En papirclips af metal flyder på vand. Flere kan normalt forsigtigt tilsættes, uden at vandet løber over.
· .jpg)
En aluminiumsmønt flyder på vandoverfladen ved 10 °C. Enhver ekstra vægt vil få mønten til at falde til bunden.
Spørgsmål og svar
Q: Hvad er overfladespænding?
A: Overfladespænding er en effekt, hvor overfladen af en væske er stærk og kan holde en vægt op. Den bevirker, at nogle små ting kan flyde på overfladen, selv om de normalt ikke ville kunne det, og den gør det muligt for nogle insekter (f.eks. vandløbere) at løbe på vandets overflade.
Spørgsmål: Hvad forårsager overfladespænding?
A: Overfladespænding skyldes, at molekylerne i væsken tiltrækkes af hinanden (kohæsion).
Spørgsmål: Hvilke dimensioner har overfladespænding?
A: Overfladespænding har dimensionen kraft pr. længdeenhed eller energi pr. arealenhed. De to er ækvivalente, men når der henvises til energi pr. arealenhed, bruger man udtrykket overfladeenergi - som er et mere generelt udtryk i den forstand, at det også gælder for faste stoffer og ikke kun for væsker.
Spørgsmål: Hvordan påvirker overfladespænding materialevidenskaben?
A: Inden for materialevidenskab anvendes overfladespænding enten for overfladespænding eller fri overfladeenergi.
Spørgsmål: Hvordan bidrager kohæsion til overfladespænding?
Svar: Kohæsion bidrager til overfladespændingen ved at få molekyler i en væske til at blive tiltrukket af hinanden, hvilket skaber en stærk binding på overfladen, som kan holde vægten og gøre det muligt for visse genstande eller væsener (f.eks. vandstridere) at interagere med væsken på en anden måde, end de ellers ville kunne gøre.
Spørgsmål: Hvordan adskiller denne egenskab sig fra andre egenskaber ved væsker?
A: Denne egenskab adskiller sig fra andre egenskaber ved væsker, fordi den påvirker, hvordan objekter interagerer med dem på deres overflader i stedet for i dem eller gennem deres adfærd som helhed.
Søge